时间:2021-01-21 11:28 编辑:全球肿瘤医生网
晚期卵巢癌CAR-T细胞治疗,CAR-T疗法全面打击晚期卵巢癌脆弱防线
乳腺癌、宫颈癌、乳腺癌被认为是威胁女性健康的三大肿瘤杀手。对比乳腺癌、宫颈癌,卵巢癌这种恶性妇科肿瘤好像我们在新闻报道中极其少见。据近期一项调查发现,居然有高达70%的受访者不知道卵巢癌是妇科肿瘤中致死率最高的类型。
无癌家园的专家进一步解释道,有70%的卵巢癌患者被诊断时已是晚期。在过去的10年间,我国卵巢癌发病年龄越来越年轻,发病率增长30%,死亡率增加18%。其在妇科恶性肿瘤中5年生存率最低,仅为39%,5年复发率最高,达到70%。
近年来,嵌合抗原受体T(CAR-T)细胞疗法在卵巢癌治疗中起着重要的作用,目前也是研究人员们关注的焦点。
百花齐放,不同靶点CAR-T疗法全面打击晚期卵巢癌
CARs靶向的表面抗原主要是蛋白质和糖脂。在关于卵巢癌的CAR-T细胞疗法中,最常见的靶抗原包括间皮素(MSLN)、MUC-16、FESR和NKG2D等。
1、靶点:间皮素(MSLN)
间皮素是免疫疗法中有希望和潜在的特异性靶标。在基于间皮素的CAR-T细胞研究的实验阶段已经获得了令人鼓舞的结果,并且已经批准了针对多种肿瘤的临床试验。此外医学研究者们还进行了间皮瘤、卵巢癌和肺癌移植的皮下或原位小鼠模型中基于间皮素的CAR-T细胞的临床前研究。
2018年7月,MaxCyte宣布,公司基于mRNA非病毒技术开发的治疗实体瘤的CAR细胞疗法已被FDA批准开始临床试验,同时,这也是MaxCyte全资拥有的第一个CAR项目MCY-M11,靶点正是间皮素(MSLN),通过腹腔内注射治疗复发/难治性卵巢癌和腹膜间皮瘤患者。
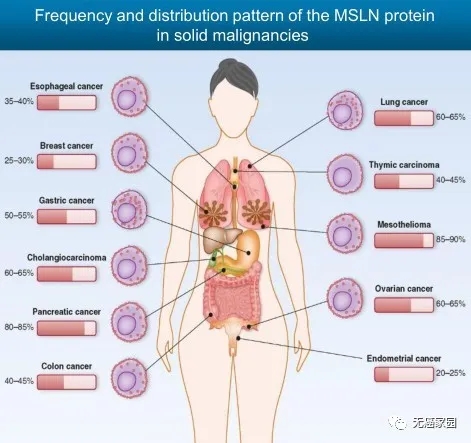
间皮素高表达于多种肿瘤组织,比如胰腺癌、卵巢癌、乳腺癌、子宫内膜癌、前列腺癌以及胆管癌等(图片来源 PNAS)
国内CAR-T细胞治疗卵巢癌临床研究进行中
目前,有一项靶向MSLN的CAR-T疗法治疗复发难治上皮性卵巢癌的临床试验正在招募中,癌友们若想申请可以咨询无癌家园医学部。
如果您符合下述条件,即可与我们联系:
1) 年龄为18~70 岁(含18 和70 周岁);
2) 由组织学或细胞学确诊的晚期上皮性卵巢癌(包括输卵管癌和原发性腹膜癌)的女性受试者;
3) 影像学检查表明有可评估的肿瘤病灶;
4) 既往接受过充分标准治疗,治疗失败或不能耐受。
2、靶点:MUC16
MUC16通常在角膜、呼吸道和生殖上皮中表达,主要是为了保护上皮免受外部病原体入侵。MUC16的表达异常增加后,它可以帮助受影响组织中的癌细胞逃脱人体的免疫监视。MUC16的过表达总是在卵巢癌、胰腺癌、宫颈癌和肺癌中发现。据相关研究显示,80%以上的卵巢癌患者存在MUC16的过表达,此靶抗原与CA-125均可作为卵巢癌早期诊断的重要指标。
在《Clin Cancer Res》上发布的一项关于以 MUC-CD靶向的T细胞在带有腹膜人MUC-CD+肿瘤细胞系的SCID-Beige小鼠中的体内抗肿瘤功效。
全身静脉输注后,靶向MUC-CD的4H11-28z+T细胞流向腹膜OV-CAR3(MUC-CD / GFP-FFLuc)肿瘤,从而产生有效的抗肿瘤功效。
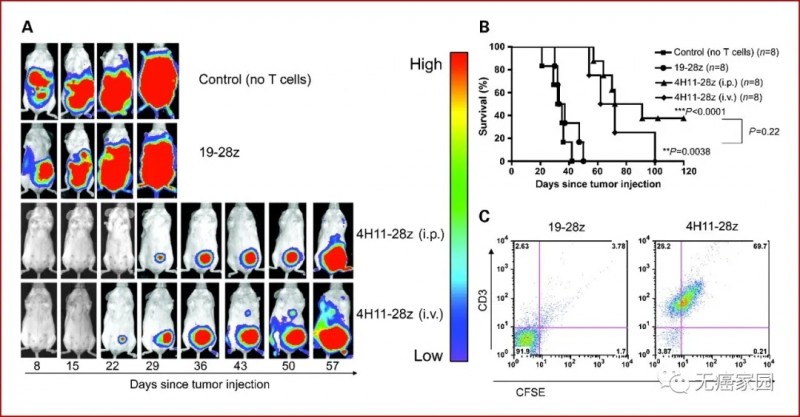
腹腔输注4H11-28z+ T细胞可根除SCID-Beige小鼠的蓝激光成像(BLI)明显的OV-CAR3(MUC-CD)肿瘤。
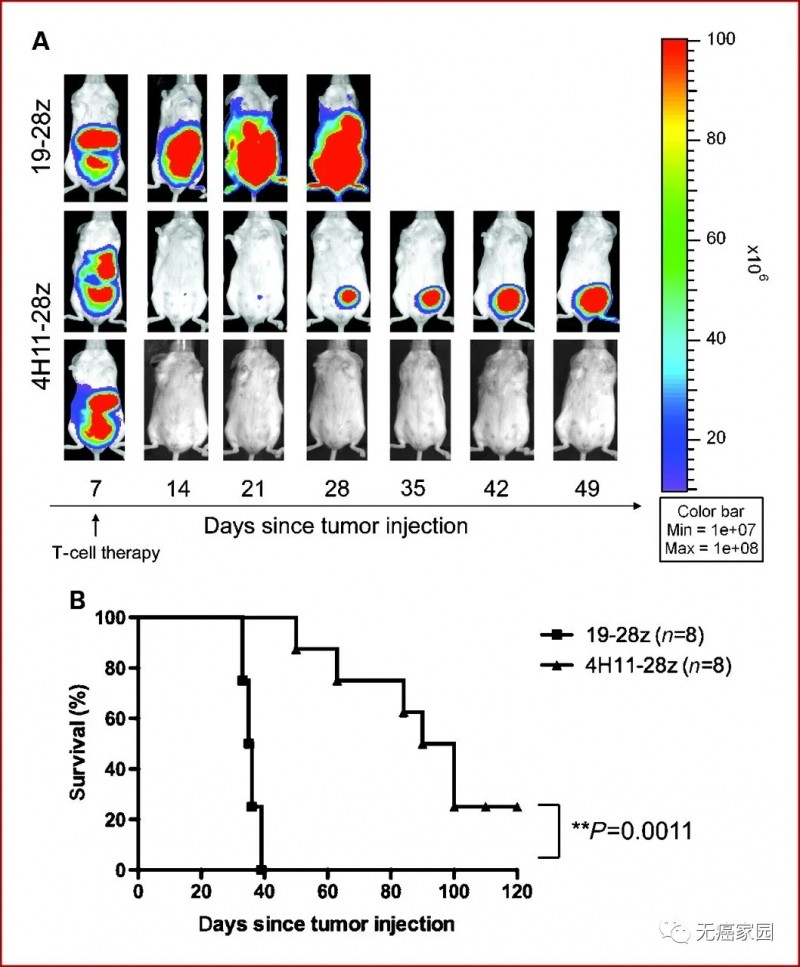
这项临床前研究证明了进一步研究靶向MUC-CD的T细胞是高危MUC16+卵巢癌患者的潜在治疗方法。
3、新型UltraCAR-T细胞疗法
2019年8月5日,Precigen公司宣布,评估新型UltraCAR-T细胞疗法PRGN-3005治疗晚期实体瘤的I期临床研究(临床试验标识符:NCT03907527)已完成首例晚期卵巢癌患者给药治疗。
PRGN-3005是一种首创(first-in-class)疗法,利用了Precigen公司UltraCAR-T治疗平台开发。PRGN-3005 UltraCAR-T是一种自体嵌合抗原受体T(CAR-T)细胞疗法,利用非病毒基因递送技术制造,目前正被评估治疗晚期复发性铂耐药卵巢癌、输卵管癌或原发性腹膜癌的治疗。


绿色代表肿瘤细胞。左侧:UltraCAR-T细胞,右侧:常规CAR-T细胞
常规CAR-T细胞在长期的体外培养中努力抑制侵袭性实体瘤细胞的生长(以绿色荧光蛋白表示),这与它们因疲惫而导致的持久存留能力有限有关。与之形成鲜明对比的是,UltraCAR-T细胞表现出对肿瘤细胞的持续杀伤并抑制肿瘤的生长,从而突出了其持久的抗肿瘤反应的潜力。
4、靶点:NKG2D
Celyad公司研发的CAR-T NKR-2疗法也是一种CAR-T细胞疗法,但是与通常的CAR-T细胞疗法不同的是这些T细胞中表达的CAR不含有识别肿瘤表面抗原的抗体片段,而是包含着完整的人类NKG2D (Natural Killer Group 2D) 受体。
NKG2D受体的配体在正常细胞中不表达或者表达量非常少,但是当细胞受到感染或者发生癌变时,这些配体的表达量会大幅度上升。CAR-T NKR-2细胞中表达的CAR将NKG2D受体与CD3融合,导致当NKG2D受体与它的配体结合时会激活T细胞。
2017年3月,该公司宣布FDA已经批准其在美国开展NKR-2 CAR-T 的代号为THINK的临床试验。主要包含7种适应症:5种实体瘤(结直肠癌、卵巢癌、膀胱癌、三阴性乳腺癌以及胰腺癌)和2种恶性血液瘤(急性髓系白血病以及多发性骨髓瘤)。
小编有话说
近年来,科学家们已经做出了相当大的努力来开发新的方法攻克实体瘤的障碍,并采用优化策略用于针对关于卵巢癌等肿瘤的CAR-T疗法,并且还在TCR-T疗法领域倾注更多的心血。我们期待着,越来越多的临床前/临床试验数据能够拼凑出一幅完整的拼图,充分展示T细胞免疫疗法治疗实体瘤的真正实力。
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。