时间:2021-10-29 16:00 编辑:全球肿瘤医生网
速递|FDA接受诺华制药的CAR-T疗法(Kymriah、Tisagenlecleucel)治疗滤泡性淋巴瘤的优先审查资格
2021年10月28日,诺华发布的新闻稿中称,FDA已经接受了其研发的CAR-T制剂Tisagenlecleucel(Kymriah)的新适应症优先审查资格,用于复发或难治性滤泡性淋巴瘤的二线以上治疗。
该适应症得到了关键性的Ⅱ其ELARA试验结果的支持。在该实验当中,Tisagenlecleucel取得了非常优秀的完全缓解率,且安全性良好。
2021年ASCO大会上公布的结果显示,使用Tisagenlecleucel治疗,在可评估的94例患者当中,完全缓解率高达66%,整体缓解率86%。治疗6个月时,95%的患者仍保持着临床缓解,76%的患者抱持着无进展生存。
研究者表示,受试的患者当中,高达78%的患者对于之前接受的最后一次治疗没有任何响应。而Tisagenlecleucel的疗效是令人鼓舞的,它使包括这部分前线治疗无效的患者在内的绝大部分患者,都达到了临床缓解。
关于Tisagenlecleucel
Tisagenlecleucel是一款CAR-CD19 T细胞制剂,也曾经是首款获得FDA批准的CAR-T细胞疗法,目前已经在世界30余个国家获批了至少1种适应症。
这款CAR-T产品能够与CD19蛋白结合,对于部分白血病和淋巴瘤有非常出色的疗效。此前,Tisagenlecleucel已经获批了B细胞急性淋巴细胞白血病等适应症,并且投入临床使用。
关于CAR-T
CAR-T细胞疗法的名声,在新兴的免疫治疗领域可以说是非常的响亮,作为细胞免疫的代表之一而受到广泛的重视。
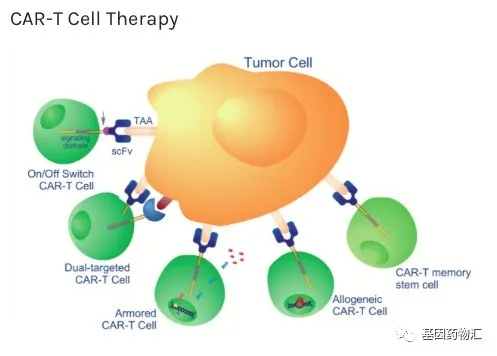
通常情况下,CAR-T细胞疗法的流程从提取患者自身免疫T细胞开始。通过分离患者自体免疫T细胞,并在体外对这些细胞进行基因改造,为它们装备能够识别癌细胞表面特定抗原的嵌合抗原受体(CAR),能够将这些抗癌能力普通的免疫细胞,改造成抗癌能力更加强大的CAR-T细胞。
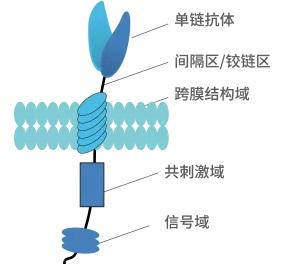
随后,在实验室中将这些接受了改造的CAR-T细胞大量扩增,再输注回患者体内。回到患者体内之后,这些特殊的T细胞就如同装备了新武器的军队,如虎添翼,能够对细胞进行更加有效的杀伤。
这样的特点与优势,使CAR-T细胞疗法成为了癌症治疗的一个全新的突破点、热点,获得了越来越多的认可,在更多的适应症上得到了应用。
治疗费用昂贵?参与临床试验,免费用药的机会来了
当然,这样一款新兴治疗方案的花费显然是不菲的。在三款已经获批的CAR-T细胞产品中,其中相对便宜的Yescarta费用为37.3万美元,Kymriah的费用更是高达47.5万美元。即使是在中国上市的价格,首款CAR-T制剂的价格也达到了120万元一针。
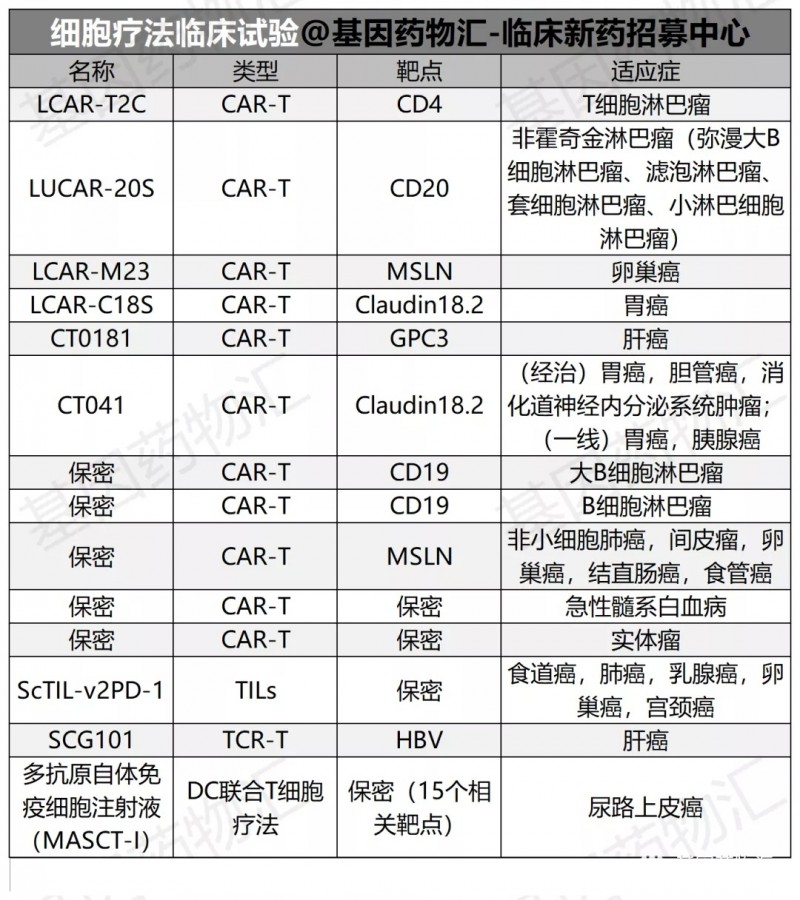
我国是CAR-T细胞疗法研究及临床试验项目最多的国家,大量国内中心的试验项目正在招募中国患者。对于符合适应症需求的患者来说,这是一个提前享受新药治疗且避免巨额开销的好渠道。
希望尝试CAR-T疗法以及其它免疫细胞疗法的患者,可以联系基因药物汇-临床新药招募中心了解详情,或将病历资料及联系方式发送至招募中心邮箱(doctorjona0404@gmail.com)进行申请。
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。