时间:2022-03-28 15:52 编辑:全球肿瘤医生网
TCR-T细胞疗法,TCRT细胞免疫疗法,TCR-T细胞治疗实体瘤有望迎来新突破
恶性肿瘤发病率逐年升高,已成为人类面临的共性问题。手术、传统化疗、放射治疗等传统治疗方法在癌症治疗中一直起着主导作用,然而这些疗法的效果较为局限,尤其是晚期患者很难从这些治疗中长期获益,也无法从根本上解决或改变其生存质量。因此,研究人员越来越多地将目光投注在免疫治疗领域。
免疫治疗为肿瘤的治疗带来了新的契机和希望,其中免疫检查点抑制剂、治疗性抗体、肿瘤疫苗、免疫调节剂、过继细胞治疗等显著改善了肿瘤患者的预后,部分晚期肿瘤患者获得了长期生存。
近两年来,众多细胞免疫疗法纷纷崛起,发展迅猛,无疑掀起了一场癌症治疗的热潮。
而细胞免疫疗法中的T细胞免疫疗法可谓是炙手可热的一块领域,之前无癌家园往期的文章经常提及的是CAR-T细胞疗法(嵌合抗原受体T细胞免疫疗法)。
CAR-T细胞疗法是通过识别膜表面抗原(如CD19,BCMA等)而发挥作用,对血液肿瘤疗效显著,但一直在努力尝试突破实体瘤方面的瓶颈。而今天要讲的主角则是TCR-T细胞疗法,即细胞受体基因工程改造的T细胞疗法。
新锐公司豪掷1.75亿美元开发新型TCR-T疗法,主攻KRAS突变实体瘤
最新研究数据表明,在世界范围内,实体肿瘤是男性和女性癌症死亡的主要原因,分别占94.4%和96.8%。尽管近年来肿瘤治疗的研究进展很快,但是恶性实体肿瘤仍然是一种严重威胁人类生命与健康的重大疾病。
CAR-T 细胞和TCR-T细胞都属于经基因工程技术改造的T细胞。与CAR-T疗法取得了卓越的成绩相比,TCR-T疗法可能不被大众所熟知,但是在治疗实体瘤方面,TCR-T细胞疗法可能比CAR-T疗法更有优势。
近期,TCR-T疗法在实体瘤领域内可谓是遍地开花!
2022年3月22日,国外知名生物技术公司Affini-T Therapeutics宣布完成1.75亿美元融资,旨在寻求推动多个靶向致癌基因的研发项目进入临床。
该公司致力于开发难治性实体瘤的相关药物,其专属平台有可能为携带KRAS突变的患者提供转化疗法,这是实体瘤中最普遍的致癌驱动突变。
KRAS突变我们并不陌生。大约30%的肿瘤都存在KRAS突变,包括90%的胰腺癌,30%~40%的结肠癌和15%~20%的肺癌。然而,KRAS靶向药却寥寥无几,KRAS一度成为无药可用的最难突变。
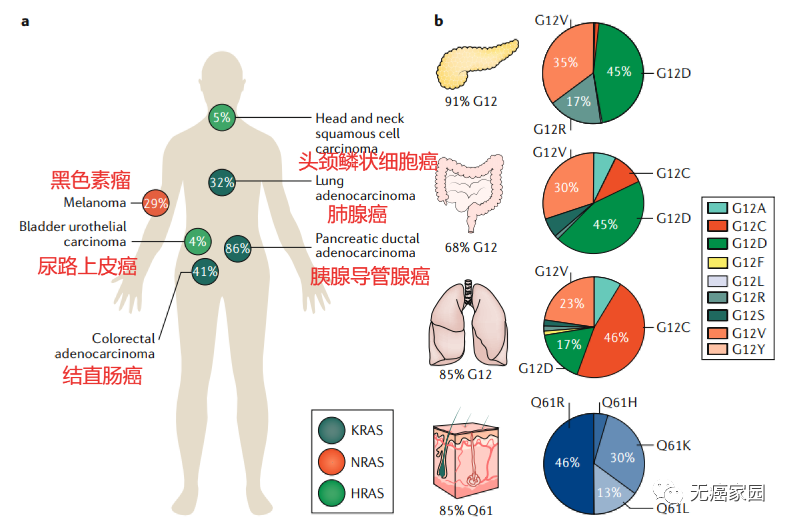
人类癌症中RAS基因突变的频率和分布
Affini-T公司旨在选择和改造正确的免疫细胞,产生持久和协调的免疫反应,而且其创新合成的生物学开关可以改写肿瘤微环境的规则,通过增加T细胞持久性,建立持续反应和增强肿瘤浸润,改良T细胞的功能。
治疗和预防癌症是核心重点领域之一,癌症仍然是当今最紧迫的健康问题之一,拜耳 Leaps 负责人 Juergen Eckhardt 医学博士说道:对于一些难治的实体瘤,如胰腺癌、肺癌或结直肠癌,尤其如此。靶向KRAS突变代表了开发有望解决先前无法治疗或治愈的癌症新疗法的独特机会。
如果您是以下类型的癌种,请速速联系我们
针对KRAS g12c突变的各类实体瘤患者,一款国产新药物D-1553已经正式开始招募患者了!
目前急招肠癌、胰腺癌、胆管癌、子宫内膜癌及卵巢癌的KRAS G12C患者,想要参加者可以咨询无癌家园医学部了解该试验。
细胞疗法新势力崛起,带你了解实体瘤的克星TCR-T疗法
近些年来,以基因修饰T细胞为中心的过继细胞疗法(ACT)引起全世界广泛的关注,其中包括大众熟知的CAR-T疗法和TCR-T疗法。CAR-T疗法在血液肿瘤中取得了卓越的疗效,但在实体瘤中的治疗效果却差强人意。在这方面,TCR-T治疗在实体肿瘤中具有非常大的发展潜力。
TCR-T细胞免疫疗法是继淋巴因子活化的杀伤细胞(LAK)和肿瘤浸润淋巴细胞(TIL)免疫疗法之后,针对性更强的一种细胞免疫治疗方法。
TCR-T技术主要机制是向普通T细胞中引入新的基因,使得改造过的T细胞能够表达有效识别肿瘤细胞的TCR(T cell receptor,T细胞抗原受体),从而引导T细胞杀死肿瘤细胞。

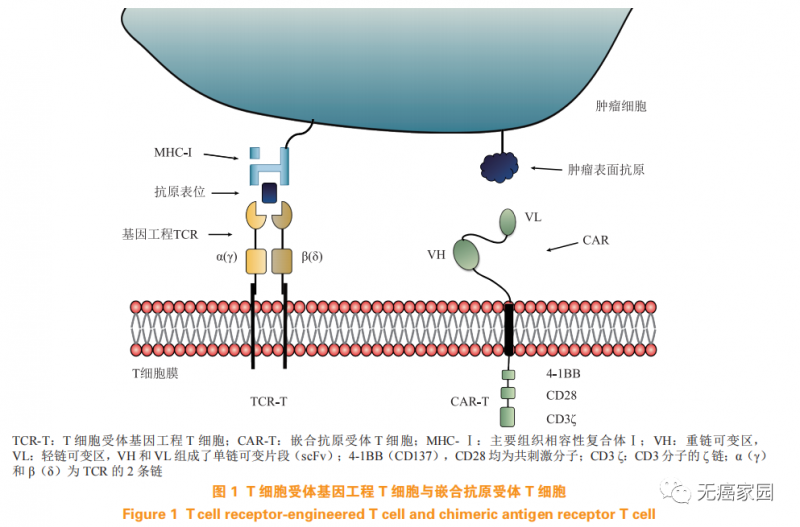
与CAR-T相比,TCR-T具有多个优势
●CAR-T治疗中由于膜蛋白数量有限,致使能够应用于实体瘤的靶点非常有限;而TCR-T治疗具有更广的靶标范围。
●部分肿瘤时由致癌病毒引起的,靶向癌病毒抗原同样可获得相应治疗效果,而大部分病毒抗原属于胞内蛋白,因此TCR-T治疗也是病毒性肿瘤细胞治疗中的优选方案。
●此外,每个CAR需要1000余个抗原来激活,而每个TCR-T仅需1~50个抗原激活,因此TCR-T可识别低丰度的肿瘤抗原。
●CAR-T主要分布在肿瘤周围以获取表面抗原,而TCR-T可以穿透肿瘤,这使得其在癌症治疗中更有效率。
●与CAR-T治疗相比,TCR-T治疗发生细胞因子释放综合征(CRS)的风险可能更低。
全球首款双特异性TCR-T疗法获得FDA批准上市,剑指实体瘤
今年对于TCR-T来说可谓是具有意义的一年,在年初就迎来了开门红!
2022年1月25日,FDA批准Kimmtrak(tebentafusp-tebn,IMCgp100)用于 HLA-A*02:01 阳性的无法切除或转移性葡萄膜黑色素瘤(mUM)成人患者。这是一种双特异性 gp100 肽-HLA导向的CD3-T细胞接合剂。
可喜可贺的是,Kimmtrak的获批成就了多个第一,成为具有里程碑意义的重大突破!
1.第一个获得FDA批准的TCR-T疗法;
2.第一个获批FDA监管批准的治疗实体瘤的双特异性T细胞接合器;
3.第一个也是目前唯一获得FDA批准治疗不可切除性或转移性葡萄膜黑色素瘤的疗法。
此次TCR-T疗法Kimmtrak获批的IMCgp100-202临床试验的积极数据,纳入378例HLA-A*02:01 基因型阳性的转移性葡萄膜黑色素瘤患者作为研究对象。分别对比TCR-T疗法Kimmtrak与pembrolizumab、ipilimumab 或达卡巴嗪等方案治疗的疗效。
试验的关键结果包括:
●中位总生存期:21.7个月 vs 16个月;
●中位无进展生存期(PFS):3.3个月 vs 2.9个月;
●1年总生存率:73.2% vs 58.5%;
●Kimmtrak单药治疗将死亡风险降低了49%,与研究者选定的方案相比,Kimmtrak治疗将疾病进展或死亡风险显著降低了27%。
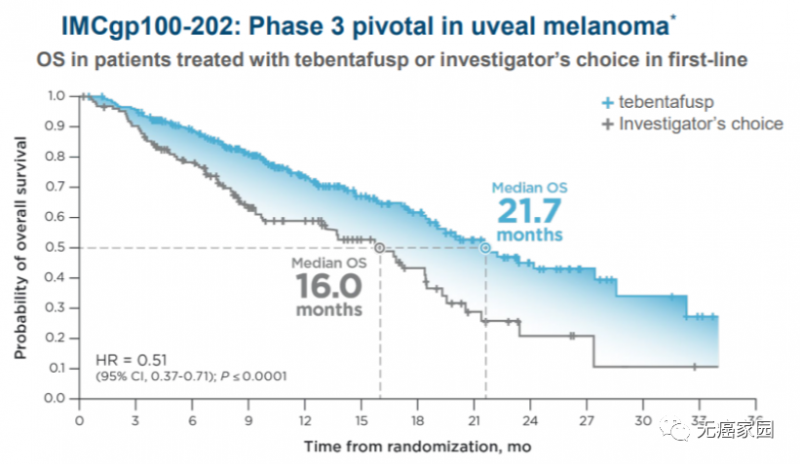
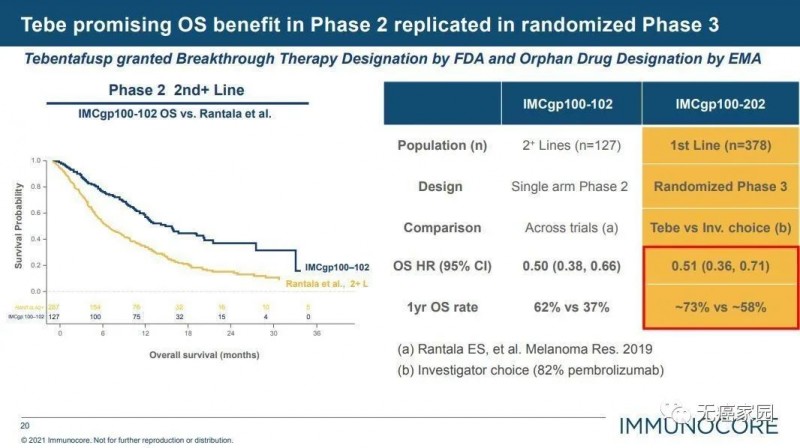
Kimmtrak治疗mUM 2期和3期临床数据
晚期肝癌迎来新曙光!TCR-T疗法让癌症患者完全缓解
目前,全球TCR-T开发处于临床验证阶段,国内也在不断突破创新。
2021年12月22日,CDE(药品审评中心)官网能够查询到SCG101自体T细胞注射液的临床申请,此产品是一款针对特定乙型肝炎病毒(HBV)表位的TCR-T细胞疗法,是治疗HBV相关肝细胞癌(HCC)的潜在新疗法。

▲ 图片来源:CDE官网
早在2020年国际肝病大会(ILC)上,一款基于T细胞的肝癌新型TCR-T疗法ADP-A2AFP引起了不小的轰动,也让肝癌的新疗法有了新的突破。
在纳入的患者中,有一名患者的癌细胞进程出现了完全缓解(CR)的表现,其余参与者的甲胎蛋白(AFP)也都出现了不同程度的下降,这意味着试验取得了进展,也说明该疗法针对晚期肝癌的治疗是有效果的。
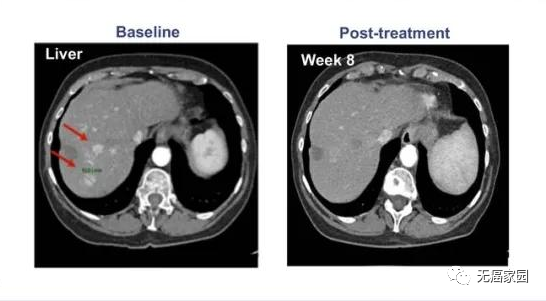
参与的9例患者均接受过手术及常规放化疗,但出现失败或不耐受的现象。在接受最高剂量治疗的4例患者中,有1例患者获得完全缓解,CT扫描显示,患者体内所有病变都消失了,而且完全缓解后已持续半年以上无任何复发的状态!
其他患者(队列1、队列2)最佳反应是病情稳定。队列2中的1例患者在治疗1个月后原发病灶体积未缩小,但纵膈淋巴结转移灶体积明显缩小!
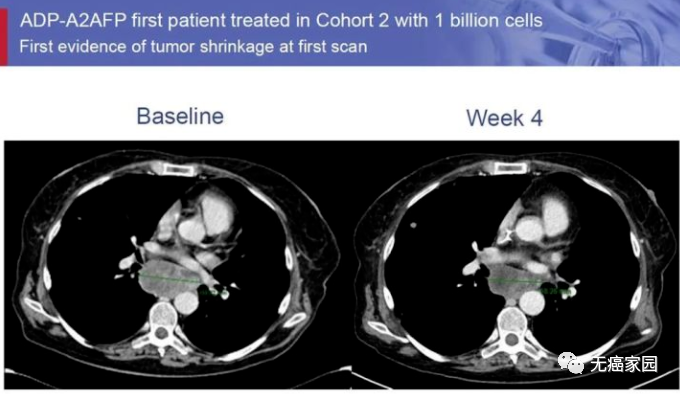
因此,靶向AFP(甲胎蛋白)的TCR-T疗法能够杀死表达AFP的肿瘤细胞,基于此项研究的积极结果,研究人员有望将最大剂量扩大至50亿个细胞治疗,我们期待这项研究更新的数据公开!
无癌家园TCR-T疗法招募
那么到底有没有机会尝试TCR-T疗法呢?小编这就带来了一个好消息,目前正有一项研发的TCR-T疗法在招募肝癌患者开展临床试验,想要参加的患者可以咨询无癌家园医学部了解详细入排标准。
TCR-T疗法在各癌种方面的临床研究进展
01、滑膜肉瘤
在2021年ASCO大会上,美国MD安德森癌症中心公布了一项关于新型过继性T细胞的疗法治疗滑膜肉瘤/圆细胞脂肪肉瘤的II期研究数据,疗效十分亮眼!
在这项研究中,专门采用针对MAGE-A4癌症抗原的TCR-T技术 afamitresgene autoleucel(afami-cel,以前称为ADP-A2M4),在多种实体瘤类型,包括滑膜肉瘤、头部肿瘤、宫颈癌和肺癌中均获得了缓解,并且多名患者出现持久反应,这意味着这种新型的基于TCR的新兴技术是未来攻破实体瘤的新希望。
共纳入45例晚期转移性滑膜肉瘤/圆细胞脂肪肉瘤患者,均符合HLA-A2阳性且肿瘤表达MAGE-A4的条件。截至2021年2月4日,32例患者接受了afami-cel治疗。这些中位年龄为43岁的患者有87.5%患有滑膜肉瘤,且之前接受过3次全身治疗。
(注:其中HLA-A2是最常见的HLA-I类分子,在汉族中大约占50%,MAGE-A4则在滑膜肉瘤中则有52.9%的阳性率。)
在数据截止时,25例患者可评估初步疗效,其中23例滑膜肉瘤患者,2例粘液样/圆细胞脂肪肉瘤(MRCLS)患者,其余患者随访不足。
结果显示:在25名可评估患者中,afami-cel总缓解率为40%(10/25)。其中2例完全缓解(CR)、8例部分缓解(PR)、11例疾病稳定(SD)和4例疾病进展(PD),疾病控制率为84%(21/25)。10例应答者中有9例在数据截止时有持续应答!
这些初步数据表明afami-cel在大量预处理的患者中有效且耐受性良好。在广泛的 MAGE-A4 抗原水平上报告了客观反应,并观察到了深度反应,最初的耐用性数据令人鼓舞。
02、上皮癌
2020年ASCO大会上还公布了E7 TCR-T细胞疗法的I期研究初步结果。该研究纳入了人乳头瘤病毒(HPV)相关的上皮癌患者,入组后收集患者血液中T细胞,由于E7癌蛋白在这类患者高表达,因此通过携带E7 TCR基因的病毒载体对T细胞进行工程化后,再次回输进入患者体内。
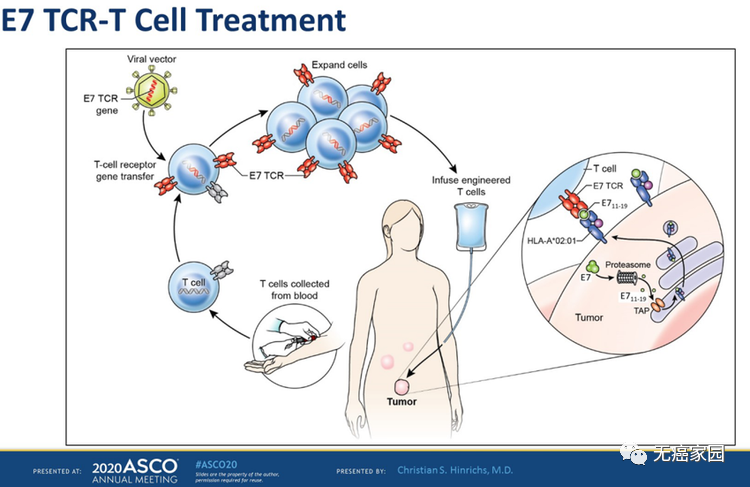
E7 TCR-T细胞治疗过程
此实验纳入的均为多线经治的晚期患者,也是首个用于人体的E7 TCR-T疗法,纳入的都是多线经治的晚期患者。结果显示,在既往至少接受过三线治疗方案的12例上皮癌患者中(主要有头颈鳞癌和宫颈癌),部分缓解(PR)6例,另外4例达到了疾病稳定(SD)。在达到PR的大部分患者中,都有一个或多个肿瘤病灶的持续完全缓解。
对于经多线治疗的患者,客观缓解率(ORR)达到50%,可以说疗效非常显著。此外,在8例既往使用过PD-1/PD-L1免疫治疗的患者中,4例出现肿瘤缓解。
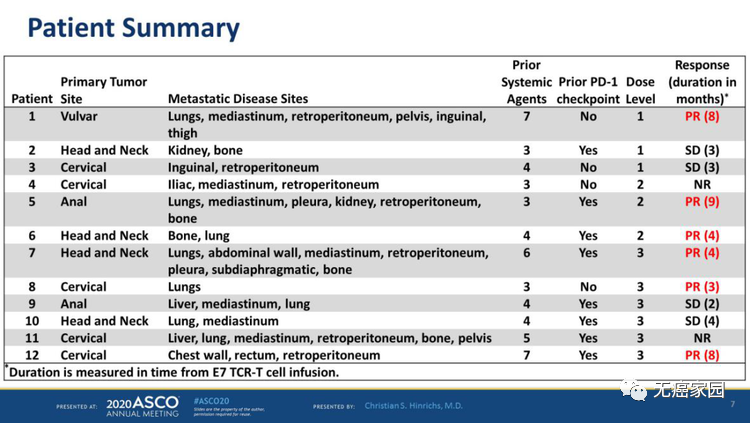
12例患者特征及疗效
【典型病例】
患者为一名49岁的老年女性,外阴癌。之前用过7次全身性化疗治疗。广泛的肺部、腹膜后、骨盆和大腿转移。经细胞产品治疗8个月后,大部分肿瘤缩小。
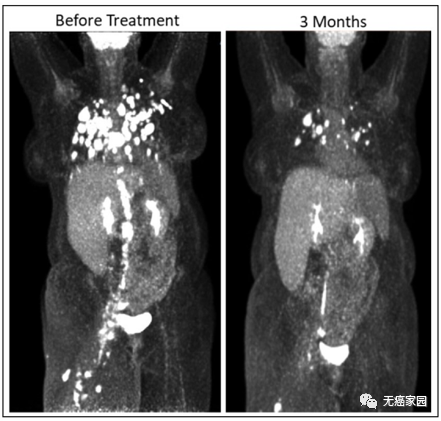
患者治疗前和治疗3个月后的PET-CT结果
03、实体瘤(滑膜肉瘤、卵巢癌、头颈鳞癌)
2019年12月,ADP-A2M4被美国药品监督管理局(FDA)授予医学先进疗法称号(RMAT),用于治疗滑膜肉瘤;这款疗法在2018年也被FDA授予孤儿药称号,用于治疗软组织肉瘤。值得一提的是,基于以上积极数据,该公司预计ADP-A2M4将于2022年在美国上市。
该研究共纳入了38例晚期实体瘤患者,既往中位治疗线数为3,主要包括18例滑膜肉瘤、9例卵巢癌、3例头颈鳞癌等。
结果显示,38例患者的客观缓解率(ORR)为23.7%,疾病控制率(DCR)为71.1%。其中,滑膜肉瘤的ORR为43.8%,非肉瘤的ORR为9.1%;头颈癌的ORR为33.3%,肺癌的ORR为50.0%。在不同的瘤种都观察到了疗效。
其中,本次试验可评估的16例滑膜肉瘤患者,客观缓解率(ORR)为43.8%(7名患者肿瘤缩小),疾病控制率为90%以上(14名患者响应)。
目前,靶向MAGE-A4的SPEAR T细胞疗法在开展全球多项临床试验,以评估进一步评估该疗法的疗效。
典型病例
一名67岁的老年男性,有4年的滑膜肉瘤患病史,心包复发,既往采用减瘤术和异环磷酰胺治疗,MAGE-A4高表达。输了9.95109的TCT细胞产品。基线扫描显示很高的疾病负担155mm,疾病在心包和肝脏。输液后扫描,在第12周时,靶向的肿瘤病灶大程度减少了45%。骨髓异常综合征方面在一段时间后继续减少了71%,由于新的不明靶向的病灶的出现,在第24周时发生了疾病进展。
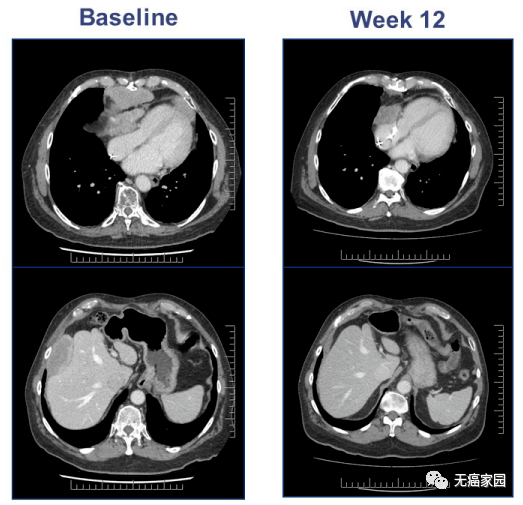
04、多发性骨髓瘤
在多发性骨髓瘤的 TCR-T 临床研究中,Rapoport 等研究学者将NY-ESO-1 癌睾丸抗原特异性的TCR基因转导入自体T细胞,用于治疗多发性骨髓瘤患者。
结果显示,70%(14/20)患者的病情得到接近完全缓解(nCR)或者完全缓解(CR),其他有2例患者病情达到 部分缓解(PR),1例患者病情稳定(stable disease,SD),1 例患者发生疾病进展(PD)。
05、食管癌
在食管癌的 TCR-T 临床研究中,Kageyama等研究学者将MAGE-A4 作为靶抗原的TCR 基因转导入T细胞,用于治疗10 例食管癌患者。
研究结果显示,其中3例患者存活时间超过 27 个月,7 例患者在治疗2个月内发生疾病进展(PD),但未观察到任何治疗相关性不良反应。
小编有话说
TCR-T 疗法治疗肿瘤是一个令人兴奋且发展迅速的新兴领域。它的使用开创了一种治疗癌症、病毒感染和其他免疫调节疾病的新方法。临床研究已经证明了使用TCR-T治疗癌症和病毒感染的不同程度的可行性、安全性和有效性。尽管有证据表明TCR-T可以是安全有效的,但如何最大限度地发挥其治疗潜力并将不良事件降至最低仍有待研究。
到目前为止,TCR-T 细胞免疫疗法已在部分实体肿瘤的治疗中取得了较好的疗效,特别是对肝癌、黑素瘤、滑膜细胞肉瘤的治疗效果很明显,但是对食管癌和多发性骨髓瘤等其他实体瘤的疗效尚有待进一步临床验证。希望在不久的将来,经过科研人员的不懈努力,选择到更合适的免疫靶标,并且优化TCR-T 的转染等方式。TCR-T疗法必将在癌症、传染病或自身免疫病等领域发挥重要作用。
如果您对于目前的治疗方案有疑问,或者想要咨询更合适的治疗方案,请联系无癌家园医学部申请国际会诊。
肝癌专家重磅推荐

参考文献
https://media.bayer.com/baynews/baynews.nsf/ID/C8DF31457159648EC125880C00375C74?Opendocument
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。