时间:2022-04-21 11:59 编辑:全球肿瘤医生网
速递|FDA授予Enhertu(DS-8201,Fam-trastuzumab deruxtecan-nxki)治疗HER2突变的非小细胞肺癌优先审查资格
2022年4月19日,阿斯利康发布的公告称,阿斯利康(AstraZeneca)和第一三共(Daiichi Sankyo)已经收到了FDA发送的Fam-trastuzumab deruxtecan-nxki(Enhertu,DS-8201)补充生物制剂许可申请接受通知,用于治疗HER2突变的不可切除或转移性非小细胞肺癌经治患者。FDA同时为这一适应症授予了优先审查资格。
目前,Enhertu已经获得了FDA批准用于治疗乳腺癌及胃癌患者,并且已经向中国提交了上市申请。如果此次的新适应症获得批准,Enhertu将成为针对HER2突变的转移性非小细胞肺癌的首个靶向治疗方案。
缓解率55%,存期17.8个月
去年的世界肺癌大会上,研究者公开了Enhertu治疗非小细胞肺癌的最新研究结果。DESTINY-Lung01试验(NCT03505710)的研究结果显示,接受治疗的患者整体缓解率为61.9%,其中完全缓解率为2.4%,疾病控制率达到了90.5%;中位随访8个月时,患者的中位无进展生存期为14个月,中位缓解持续时间及总生存期尚未达到。
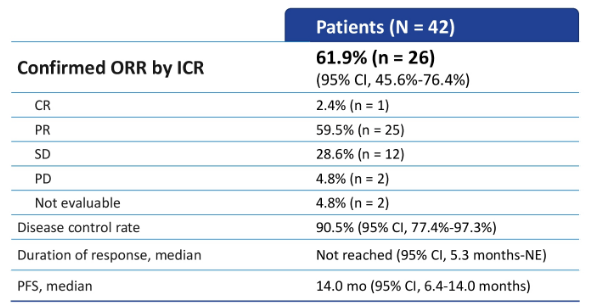
至今年,研究者再次更新了Ⅲ期DESTINY-Lung01试验的数据,随访时间已经达到13.1个月。在91例转移性HER2突变非小细胞肺癌患者当中,整体缓解率达到了55%,疾病控制率再次提升,达到92%。这些患者当中包括了一些比较难治的患者,例如脑转移的患者,以及接受过多种方案治疗的患者,包括各类免疫检查点抑制剂治疗。
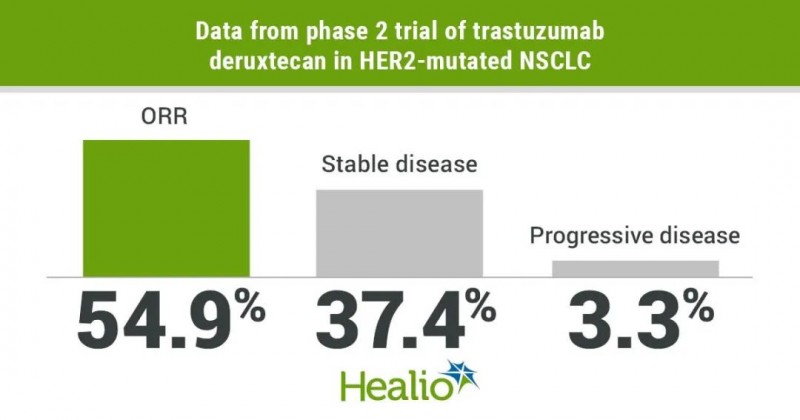
同样,这款药物有相应快、疗效持续时间较长的特点。患者的平均响应时间仅有1.5个月,中位缓解持续时间为9.3个月,中位无进展生存期8.2个月,中位总生存期17.8个月。
这是目前为止HER2抑制剂(包括ADC药物)治疗非小细胞肺癌的临床试验中,纳入患者数量较多、且疗效比较显著的一项。
在HER2扩增的患者当中,达克替尼方案、曲妥珠单抗+帕妥珠单抗方案、以及T-DM1方案治疗的整体缓解率,分别是0%、24%和43%,差距非常明显。此次公开新数据的DS-8201则是在T-DM1的基础上小有提升,发挥同样稳定且出色。
新一代的ADC药物,俨然已经成为了HER2非小细胞肺癌治疗的未来发展方向。
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。