时间:2022-04-25 15:57 编辑:全球肿瘤医生网
EGFR靶向药、KRAS突变靶向药、NTRK靶向药、MET靶点抑制剂,国内外多种肿瘤靶向药物再掀风暴
迄今为止,现代医学都尚未攻克众病之王癌症,人类在对癌细胞发起前三波(外科手术、放疗、化疗)进攻后,意识到杀死癌细胞的同时也杀伤了正常的细胞,开始不断找寻新的治疗方法。那么,如何才能精准打击癌细胞,把对正常细胞的伤害降到最低呢?
人类的第四波进攻靶向治疗便应运而生。靶向治疗的药物是根据靶点来设计的,像钥匙和锁一样,一把钥匙开一把锁,这就是靶向治疗。不同于放化疗,靶向治疗属于精准治疗,有靶点就可用相应的靶向药物,疗效比较可靠,有效率高,起效较快,通常一两周就能看到效果。如果把化疗那种杀敌一千自损八百的方式比作地毯式轰炸,那么靶向治疗就是精确制导的远程导弹!

图源摄图网
2005年,是靶向药进入中国的元年,自从易瑞沙(吉非替尼)进入中国市场后,十多年来,中国晚期肺癌患者中位生存期显著增长2.4倍,从此前的14.1个月延长到33.5个月,5年生存率从8%增长到18%,也是两倍之多。
更大的进步在于,靶向药物的副作用远远小于化疗,疗效则远胜化疗,提升患者生存期限的同时,生活质量也能得以维持。通俗来说,化疗是低效高毒,靶向药物则是高效低毒。
近期,癌症靶向治疗进展非常迅速,无论国内外,均有不少高效的靶向药纷纷获批上市或投入使用。就在2022年刚刚结束不久的美国肿瘤研究协会(AACR)年会上,众多备受癌友们关注的靶向药如雨后春笋般不断涌现,让无数癌友重新点燃生的希望。那么,今天无癌家园的小编就盘点下热门靶向药的最新临床研究。
钻石靶点NTRK
NTRK之所以被称为钻石基因,首先是因为它非常罕见,在中国常见的肺癌、乳腺癌、结直肠癌中,只有1%~5%的患者存在这种突变,而一些罕见的癌症,比如婴儿纤维肉瘤和分泌型乳腺癌,存在NTRK融合的频率却高达90%~100%。其次,针对NTRK融合突变上市的药物及在研的药物临床效果显著,接受治疗的患者通常都能快速起效,很多晚期患者在使用NTRK抑制剂后得到了重生,像钻石一样罕见又珍贵。
国产新一代不限癌种靶向药ICP-723势头强劲
2022年4月11日,诺诚健华公布了ICP-723的临床前数据。研究结果显示, ICP-723可有效抑制TRKA、TRKB和TRKC的激酶活性(IC50值小于1 nM) 。ICP-723不仅在TRK驱动的肿瘤中显示出强大的体外疗效,还克服了第一代TRK抑制剂治疗后经常出现的抗性突变,如TRKA G595R和TRKC G623R/E。
体内药效研究进一步证明了ICP-723在动物模型中的强大抗肿瘤作用。在1 mg/kg剂量下,ICP-723对KM12肿瘤模型的抑瘤率(TGI)为89.5%。ICP-723具有较高的口服生物利用度,药代动力学参数总体良好。
ICP-723是我国自主研发的新一代NTRK抑制剂,可以治疗携带NTRK融合基因的晚期或转移性实体瘤,包括乳腺癌、结直肠癌、肺癌、甲状腺癌等,以及对第一代NTRK抑制剂拉罗替尼和恩曲替尼耐药的患者。
2021年8 月31日InnoCare Pharma公司宣布其第二代泛 TRK 抑制剂 ICP-723 获得美国食品药品监督管理局(FDA)的研究性新药批准在美国开始 I 期临床试验。
在2022年诺诚健华发布的主要财务业绩报告中也对ICP-723的疗效进行了公布。
截至 2022 年 2 月11日,在 I 期剂量递增试验中,共有 17 例患者接受了 ICP-723 的治疗,剂量为 1~8 mg,每天一次。安全性良好,没有观察到 剂量限制毒性(DLT)。17例患者中,5例患者确认为NTRK基因融合阳性,客观缓解率(ORR)为80%,其中部分缓解4例,疾病控制率(DCR)为100%。在4毫克及以上剂量组中,客观缓解率为100%。
作为一种新型小分子第二代泛TRK抑制剂,ICP-723具有强活性和高选择性,有望克服对第一代TRK抑制剂的耐药性,更好地造福患者。
(注:目前这项临床试验仍在招募中,做了基因检测的病友可以拿出报告看看,一旦存在NTRK1/2/3融合,可以马上联系无癌家园医学部申请是否有机会接受新药治疗,看不懂的病友也可以致电无癌家园医学部解读报告。)
重磅!横扫21类癌种的传奇抗癌药拉罗替尼在中国上市
作为全球首个不分肿瘤来源用于初始治疗的靶向药,拉罗替尼于2018年11月26日被FDA批准上市,用于成人和小儿具有神经营养受体酪氨酸激酶(NTRK)基因融合的实体瘤治疗。
就在4月13日,我国的癌友们苦等了3年多的传奇抗癌药拉罗替尼(larotrectinib,硫酸拉罗替尼,商品名:Vitrakvi)终于获得中国国家药监局(NMPA)的批准上市,用于治疗携带NTRK融合基因的实体瘤成人和儿童患者。这表明,中国癌友们迎来了全球首款专为NTRK基因融合癌症患者设计的口服TRK抑制剂。

截图源于NMPA官网
据无癌家园之前的报道显示,这款治愈系抗癌药在2021年5月20日就已在国内递交上市申请并获受理,时隔近1年,这款抗癌药终于与国内的癌症患者见面,真的是可喜可贺!
截止到目前已发现NTRK融合存在于超过25类癌症中,包括乳腺癌、结直肠癌、肺癌、甲状腺癌等,成人和儿童患者都可以使用。
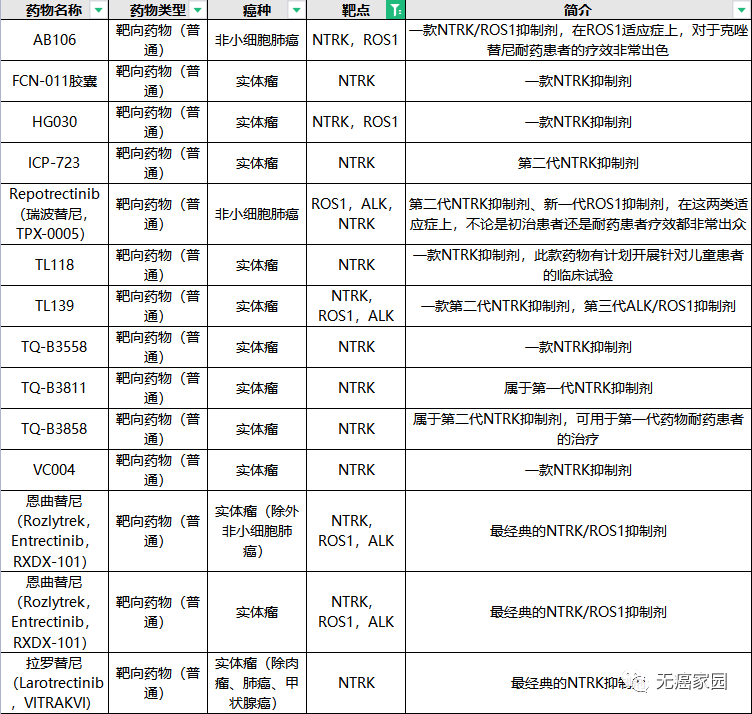
除了ICP-723、拉罗替尼外,目前全球对于NTRK药物的研发正在如火如荼地进行中,给更多患者带来新希望!无癌家园特地为各位癌友们整理了目前正在招募的NTRK抑制剂的信息,希望给各位急于寻医问药的患者更多的治疗选择!
钉子户靶点KRAS
KRAS是实体瘤中最常见的癌基因之一,大约30%的肿瘤都存在KRAS突变,包括90%的胰腺癌,30%~40%的结肠癌和15%~20%的肺癌。然而,KRAS靶向药却寥寥无几,KRAS一度成为无药可用的最难突变。
32.5%的患者生存超过两年!Sotorasib改写KRAS肺癌患者命运
Lumakras (sotorasib,AMG510)在2013年被研发成功,成为首个进入临床试验的KRAS抑制剂。又在2021年5月28日被FDA批准用于治疗携带KRAS G12C突变且至少接受过一次全身性治疗的非小细胞肺癌(NSCLC)患者。这是目前唯一一款获得批准用于KRAS突变的靶向药,也称为科学人员突破KRAS不可成药的里程碑!
在2022年AACR年会上,研究者报告了Sotorasib治疗KRAS G12C突变患者的最新长期随访数据,验证了Sotorasib对于患者的长期益处。
最新更新的数据截至2022年2月22日,中位随访时间为24.9个月。结果显示,患者的2年生存率达到了32.5%,全面超过了既往的治疗方案!
根据1/2期代号为CodeBreaK 100试验的数据更新,共有174例KRAS+非小细胞肺癌患者入组,值得一提的是,这些患者大部分已经接受了平均两种治疗方案,包括PD-1/L1和化疗。
结果显示
1. 40.7%的患者对sotorasib有部分或完全反应,疾病控制率为84%,中位反应持续时间为12.3个月。
2. 中位无进展生存期和总生存期分别为 6.3 个月和 12.5 个月。
3. 治疗一年后总生存率为50.8%,两年后总生存率为32.5%。
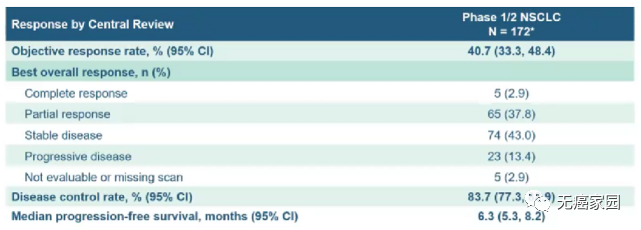
值得注意的是,两年总生存率接近 33%,与历史对照治疗相比非常有利。比如使用化疗药物多西他赛联合或不联合抗 ramucirumab 作为二线治疗的非鳞状 NSCLC 患者的两年总生存率预计在仅为15%~22%。
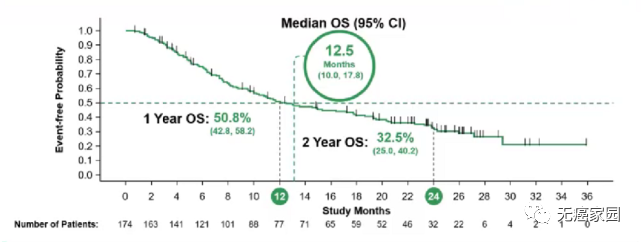
Sotorasib长期耐受性良好,不良事件轻微且可控,没有出现新的安全性事件。在不同PD-L1表达水平均能观察到患者的长期获益。不论是否存在STK11共存突变,也能观察到长期获益。相关文章:攻克不可成药的KRAS靶点,多款新药强势破局,宣战肺癌及胰腺癌等难治癌种!
疾病控制率85.7%,国产靶向药D-1553首次亮相AACR
D-1553是由益方生物自主开发的一款新型,高效且口服的KRAS G12C抑制剂。近日,在2022年美国肿瘤研究协会(AACR)年会上,益方生物首次公布了其口服KRAS G12C抑制剂D-1553在癌症患者中的临床I期数据,这使得D-1553成为了首个公布临床数据的国产KRAS抑制剂。
在一项针对携带KRAS G12C突变的晚期或转移性实体瘤患者的国际多中心一期研究中 ,D-1553在22例患者中耐受性良好,没有任何剂量限制性毒性。在21例可评估的患者中,观察到19.0%确认的肿瘤客观缓解率,达到了85.7%的疾病控制率。在剂量水平低至每天300mg时已观察到肿瘤缓解。
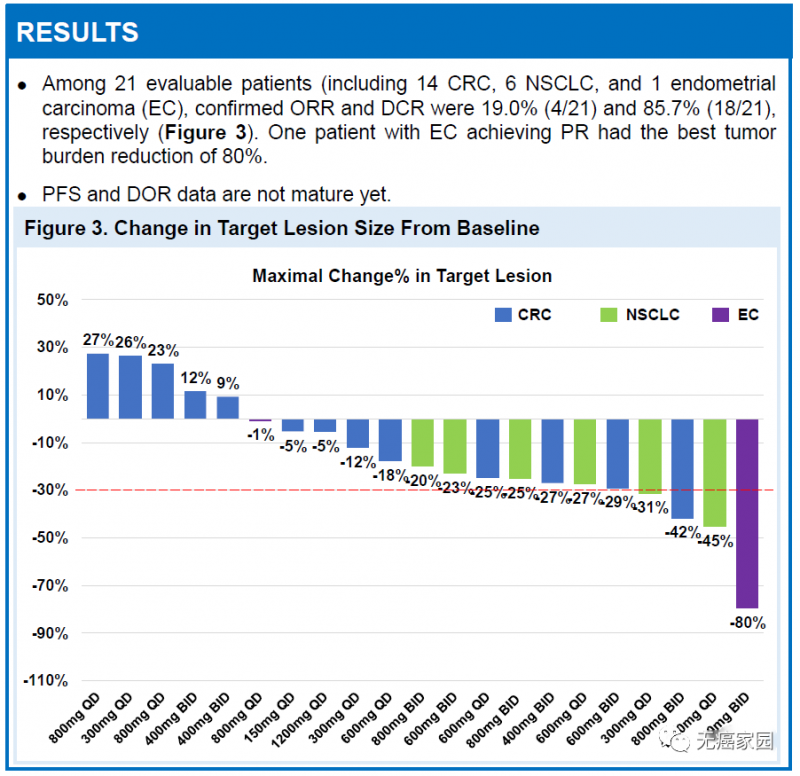
在另一项由上海胸科医院陆舜教授为主要研究者,针对携带KRAS G12C突变的非小细胞肺癌(NSCLC)患者的研究分析中包括了59例患者,其中52例为可评估患者,肿瘤客观缓解率达到40.4%,疾病控制率高达90.4%。这些患者均为晚期或转移性癌症患者,大多数已经接受了二线或二线以上的系统性抗癌药物治疗。
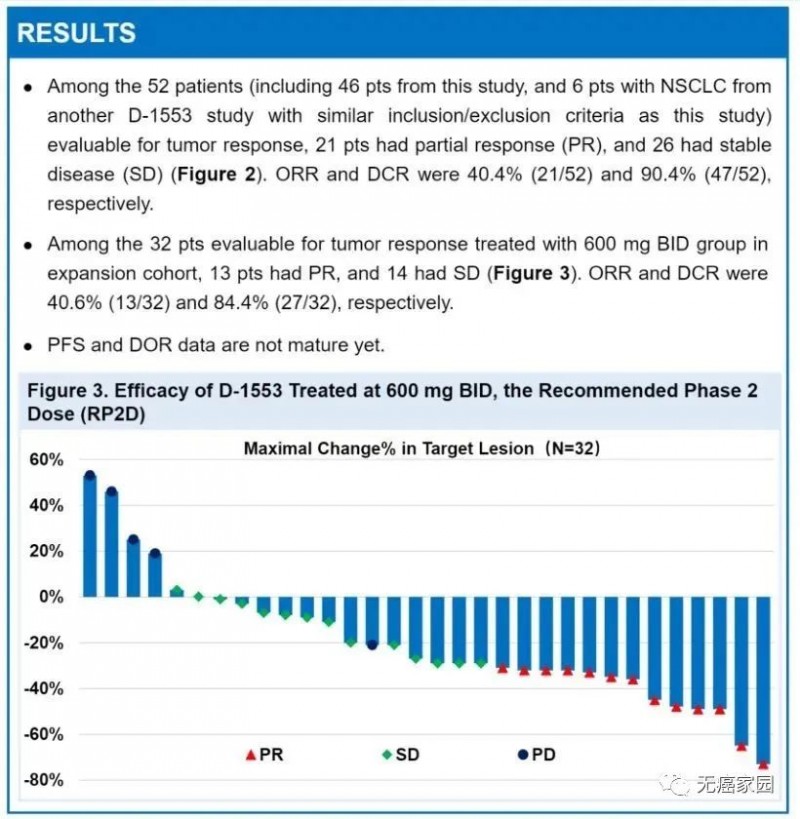
数据显示,在PR2D(600mg/BID,BID为一日两次)剂量下,D-1553在32例患者中评估的客观缓解率达到40.6%,疾病控制率为84.4%。安全性方面,D-1553耐受性良好,未达到剂量限制性毒性。
据悉,D-1553已于2020年10月获得美国FDA批准在美国、澳大利亚、中国台湾、韩国等国家和地区启动了国际多中心I/II期临床试验,目前进展顺利。并于2021年1月获得中国国家药品监督管理局药品审评中心批准开展 I/II 期临床试验。
好消息是,针对KRAS G12c突变的各类实体瘤患者,D-1553已经正式开始招募患者了!
如果您是以下类型的癌种,请速速联系我们
目前急招肠癌、胰腺癌、胆管癌、子宫内膜癌及卵巢癌的KRAS G12C患者,想要参加者可以咨询无癌家园医学部了解该试验。
除了Lumakras、D-1553外,在医学研究者们不断地努力之下,KRAS这座堡垒终于破防,多款新药不断涌现,并已有多个在研药物在临床研究阶段取得了早期成功:包括:Adagrasib(MRTX849)、JNJ-74699157 (ARS-3248)、JAB-3312、LY3499446以及泛KRAS抑制剂BI 1701963等。
热门靶点ROS1
ROS1是一种编码受体酪氨酸激酶的基因,与间变性淋巴瘤激酶(ALK)结构相似。ROS1与EGFR、ALK一样都是非小细胞肺癌(NSCLC)明确的驱动基因,融合(重排)是ROS1基因的主要变异类型。
在肺癌中占比较多的非小细胞肺癌中,ROS1融合发生概率约为1%~2%;且相较于其他非小细胞肺癌患者,ROS1 融合阳性患者往往是更年轻、且从不吸烟或仅有轻度吸烟史的肺腺癌患者。此外,ROS1融合具有排他性,通常不与其他驱动基因同时存在。
在2019年6月举行的美国临床肿瘤学会年会(ASCO)上,一款横扫ALK/ROS1/NTRK三靶点的靶向新药Repotrectinib(瑞波替尼,TPX-0005)的数据惊艳四座。
Repotrectinib是美国Turning Point Therapeutics公司开发了一种新一代口服多靶点靶向药,对ALK、ROS1和NTRK都有抑制作用,能够克服多种对其他TKI产生抗性的基因突变,杀死携带ROS1、NTRK和ALK阳性的实体瘤。
ROS1阳性肺癌患者福音!客观缓解率达79%,瑞波替尼再战告捷
在2022年4月12日,Turning Point Therapeutics公布了repotrectinib治疗ROS1阳性晚期非小细胞肺癌(NSCLC)的注册性临床试验TRIDENT-1的最新结果。该研究涵盖所有四种ROS1阳性晚期非小细胞肺癌队列。
在71例酪氨酸激酶抑制剂(TKI)初治的ROS1阳性非小细胞肺癌患者中,完全缓解4例,部分缓解52例,确认完全缓解率(cORR)为79%。
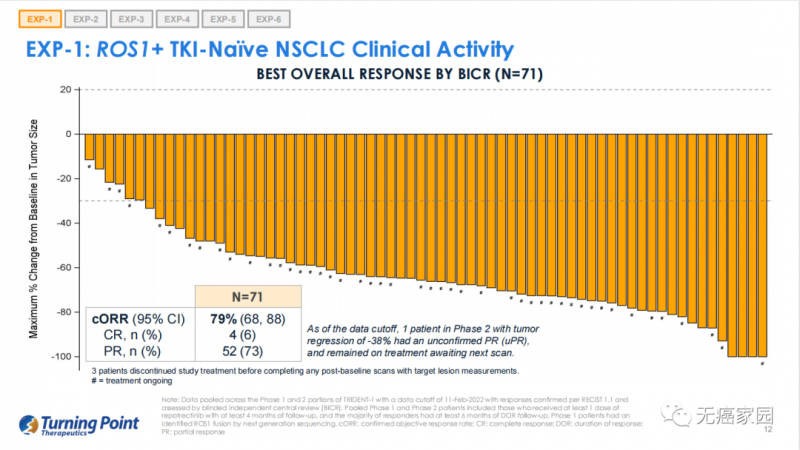
瑞波替尼在TKI初治ROS1阳性NSCLC患者中的疗效结果
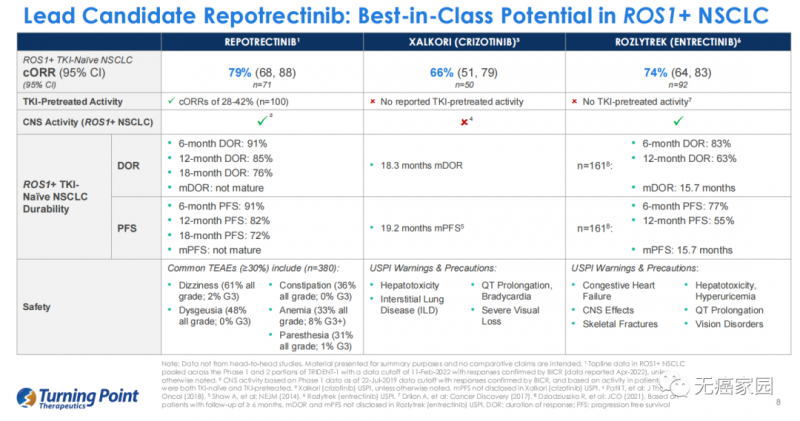
与其他ROS1抑制剂的靶向一线的确认客观缓解率(cORR)比较:克唑替尼66%、恩曲替尼74%,Repotrectinib以79%遥遥领先。
在中位随访时间10.2个月时,Repotrectinib估计12个月时的持续缓解率为85%。
在中位随访时间10.8个月时,Repotrectinib估计12个月时的无进展生存率为82%。
在接受过TKI治疗的ROS1阳性NSCLC患者群体中,17位患者携带ROS1 G2032R耐药性突变,其确认的客观缓解率为59%(10/17),包括1例完全缓解和9名例部分缓解患者。
安全性方面,从380例患者中积累的安全性和耐受性特征与此前研究一致。
此次公布的TRIDENT-1的1期和2期部分汇总结果感到非常鼓舞,业内专家认为repotrectinib是ROS1阳性晚期NSCLC患者的潜在同类最优候选药物。
目前,TPX-0005已经正式在国内开始开始招募患者了,国内的患者有机会免费接受最前沿抗癌药物的治疗,想参加的患者尽快联系无癌家园医学部,详细评估病情!
热门靶点EGFR
EGFR(ErbB-1或HER1)表皮生长因子受体主要在肺腺癌、亚裔、非吸烟及女性患者中,大约有 15% 的白种人和 30%~50% 的亚洲人中有 EGFR 基因突变。无吸烟史者,比例高达50%~60%,常见的突变位点是外显子19和21,占90%,称为经典型突变,其余10%为外显子18和20的突变。
目前,EGFR+最新的药物就是三代明星靶向药奥希替尼,虽然让很多肺癌患者成功续命,然而这款药物耐药也是很多患者面临的新的生存考验。因为截止目前为止,FDA 没有批准任何针对奥希替尼治疗后进展的靶向治疗。常规的治疗方案是化疗或化疗联合免疫治疗,疗效并不乐观,全球的目光都聚焦在第四代EGFR抑制剂上。
打破奥希替尼耐药困境,第四代EGFR靶向药BLU-945曙光初现
今年的AACR大会上,第四代 EGFR靶向药BLU-945最早开展的SYMPHONY研究结果公布,结果显示在奥希替尼耐药的人群中体现出振奋人心的疗效。
截至2022 年3月9日,33 名 EGFR 突变 NSCLC 患者接受了五种不同剂量的(范围:25~400 mg QD)BLU-945治疗。值得一提的是,大多数患者(79%)之前接受过至少三线系统治疗,高达97%的患者都接受了奥希替尼的治疗,可以说是临床上没有更好靶向治疗选择的晚期患者。
结果显示:
1.安全耐受性良好。
2.抗肿瘤活性强,肿瘤明显缩小。在经过大量预处理的患者中,较高剂量的 BLU-945 抗肿瘤活性更强。在接受 200-400 mg QD 治疗的患者中观察到肿瘤缩小。(1位接受 400 mg QD治疗的患者中出现未经证实的 PR 1 。这位患者携带外显子 19 缺失、T790M 和 C797S 突变,之前接受了铂类化疗、厄洛替尼和奥希替尼治疗后耐药,接受BLU-945后响应良好)。
3.肿瘤突变T790M和C797S含量明显降低。
所有患者在基线及每个治疗周期进行ctDNA检测。
让研究人员感到惊喜的是,BLU-945治疗后14天ctDNA检测结果显示, 83%(10/12)的患者外周血样中T790M突变丰度下降;81%(9/11)的患者C797S突变丰度下降。所有接受400mg QD的患者,T790M和C797S ctDNA均有下降,包括3例达到清除的标准(已检测不到)。
相比其他在研的第四代EGFR-TKI,BLU-945是目前进度最快的四代EGFR-TKI之一,其克服耐药的临床前数据显示出高效的抗肿瘤活性。让我们期待BLU-945能尽快公布更多的积极临床数据,尽快上市。
四代EGFR抑制剂QLH11811、H002公布临床前数据,潜力无穷
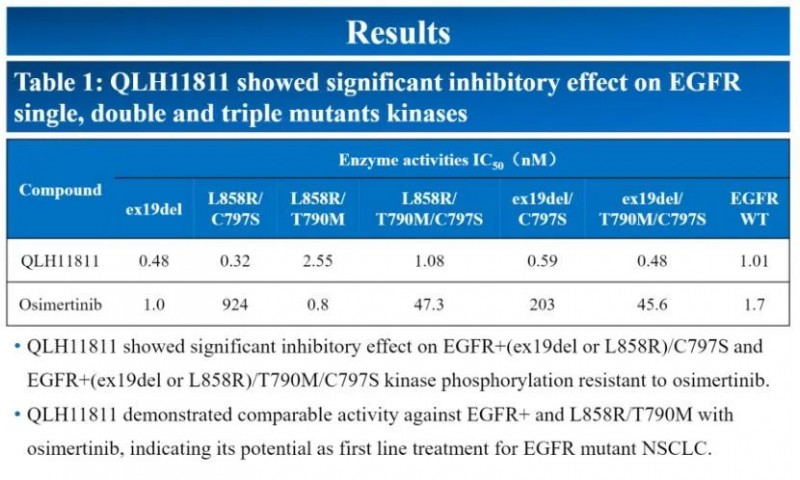
2022 AACR会议上,齐鲁制药公布了四代EGFR抑制剂QLH11811的临床前数据。从数据来看,QLH11811酶学活性极具竞争力。
QLH11811不仅逆转了奥希替尼耐药的C797S突变,对于常见的ex19del、L858R及T790M也能显示抑制活性。从临床前的肿瘤模型来看,QLH11811确实在多个肿瘤异种移植模型中到降低了肿瘤生长。
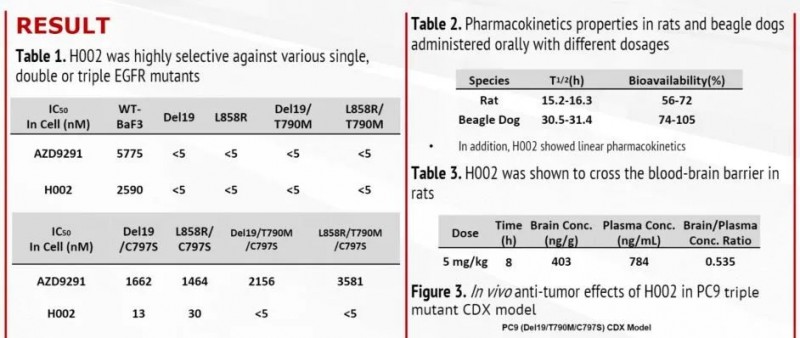
此外,红云生物也在AACR会议上,公布了获得临床许可的四代EGFR抑制剂H002临床前数据。H002的临床前数据同样优秀,也是涵盖了多种耐药突变的组合形式,并兼具一线和后线用药潜力。同时,H002也是全球少数具备透过血脑屏障能力的四代EGFR产品,临床优势和市场前景不容小觑。
热门靶点MET
近年来,MET抑制剂的研究层出不穷,其中沃利替尼、Tepotinib和Capmatinib是目前研究数据相对较多的3个药物。
客观缓解率60.9%!MET+肺癌患者将迎来疗效持久新疗法
MET 14外显子跳跃突变在非小细胞肺癌(NSCLC)的发生率为1%~3%,在肺肉瘤样癌(PSC)中的突变率却高达31.8%。MET 14外显子跳跃突变NSCLC对铂类为基础的化疗耐药率较高,因此患者预后也较差。
谷美替尼(SCC244)是一种国研高选择性MET抑制剂,在携带 MET 外显子 14 跳跃突变的非小细胞肺癌患者中表现出持久疗效。在2022年AACR大会上公布的1/2 期 代号为GLORY试验的最新数据再传捷报。
这项实验中共筛选了163例患者,其中73例MET外显子14跳跃突变的非小细胞肺癌参加了试验并接受了谷美替尼治疗。几乎所有患者都来自中国(90.4%),一小部分来自日本(9.6%)。值得一提的是,87.7%的患者都是局部晚期非小细胞肺癌,还有13.7%存在脑转移。
结果显示
接受谷美替尼治疗的患者的客观缓解率高达60.9%,总体来看疾病控制率达到82.6%!无论是初治还是经治人群均高度有效。
此次研究证明了SCC244的高效和持久性,还观察到了对脑转移的初步疗效,可谓是未来可期。
目前包括伯瑞替尼、TQ-B3139、ABBV-399在内的多款MET抑制剂新药的临床试验均在招募国内患者。
由于药物种类较多,且部分药物尚未公开名称及具体数据,因此大家可以线联系无癌家园医学部进行咨询,由专业医学顾问指导大家进行选择。
小编有话说
对于不同基因突变或不同类型的肺癌,都有不同的规范化的治疗方案。如果早期治疗,可以达到很好的疗效。对于晚期的患者,也同样应该接受规范化的正规治疗,这样不仅可以延长生命,而且还可以达到提高生活质量的目的。此外,
所以确诊为是恶性肿瘤后,一定要带上所有的检查结果,去肿瘤专科医院进行会诊,请肿瘤科专家给出适合自己的治疗方案,这样才不会耽误您的病情。最后祝愿每位患者都能够早日康复,重新拥抱健康!
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。