时间:2024-01-12 11:52 编辑:全球肿瘤医生网
CAR-T细胞免疫疗法治疗胰腺癌、肝癌、卵巢癌等多种实体瘤总生存时间超8年
据《新英格兰医学杂志》报道,佛罗里达州一位71岁的女性Kathy,在2018年诊断出患有胰腺癌后,经历了漫长且痛苦的抗癌过程,先后接受了至少八轮化疗、放疗,以及Whipple手术,并切除了部分胰腺。然而不幸的是,不到一年的时间,癌症就已扩散到肺部。
一次偶然的机会,她得知了晚期结肠癌患者在接受针对KRASG12D癌症突变的实验型基因疗法后,症状缓解的报道,抱着最后一丝希望,她联系了当地医院。天无绝人之路,尽管Kathy所患癌种不同,但她与之前接受治疗的结肠癌患者存在相同的基因突变一种名为KRAS的突变,这也让她能接受CAR-T细胞疗法的帮助,这是一种活体药物,医生先采集Kathy的T细胞,之后对这些细胞进行基因改造和重新编程,然后通过静脉输注的形式,回输到患者体内。
Kathy于2021年6月14日接受了第一次CAR-T细胞回输,据悉,治疗后1个月内,她肺部的肿瘤缩小了一半以上;6个月后,肿瘤比原来缩小了72%。主治医师表示,她的病情依然稳定,不过后续仍需密切关注,及时复查,以防癌症复发。
何谓CAR-T疗法
CAR-T疗法属于细胞免疫疗法的一种,是通过插入一段编码嵌合抗原受体(CAR)的DNA片段,对患者自身的T细胞进行基因重新编程,改造后相当于在T细胞上,安装了一个导航头,回输到患者体内后,可在免疫系统内继续生长和增殖,不断识别和攻击肿瘤细胞,最终达到治疗目的。
CAR-T疗法自获批以来,主攻领域一直是血液肿瘤,美国早在2017年,就批准了CAR-T细胞疗法上市,用于治疗复发或难治性弥漫大B细胞淋巴瘤;我国药监局也于2021年6月,批准了奕凯达(阿基伦塞注射液)上市,正是开启了与美国并驾齐驱的高速发展模式,截至目前共有10款CAR-T产品获批上市!近年来,随着CAR-T疗法研究的不断深入,更多靶点被发现,研究人员也在快马加鞭地拓展其在实体瘤领域的应用。
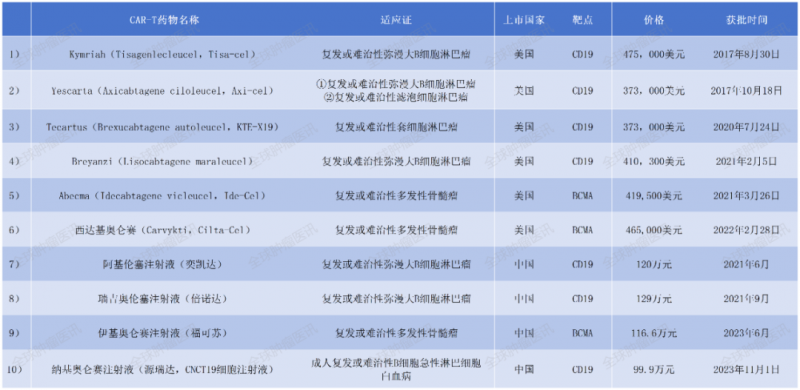
表1目前已获批上市的CAR-T细胞产品
CT041:胰腺癌克星,获FDA和我国药监局双认证

胰腺癌因其预后较差、治疗难度较高,又被称为万癌之王,近年临床研究表明,CT041在治疗胰腺癌方面展现出良好的疗效。CT041是一款自体CAR-T细胞候选产品,主要针对Claudin18.2(CLDN18.2)阳性实体瘤,如胰腺癌(PC)、胃癌/胃食管连接部癌(GC/GEJ)。
CT041于2022年1月,被美国FDA授予再生医学先进疗法(RMAT)资格,用于治疗Claudin18.2阳性肿瘤的晚期GC/GEJ。此外,科济生物医药公司研发的CT041研究新药(IND),也已被我国国家药品监督管理局(NMPA)批准,用于CLDN18.2阳性胰腺癌(PC)的术后辅助治疗。
《血液学与肿瘤学杂志》公布了CT041治疗胰腺癌因CA19-9升高且存在胰腺病变,于2019年5月6日接受手术,病理诊断为pT2N0胰腺癌。5个月后常规术后随访发现肺转移。自2019年12月6日起,一线化疗采用S-1单药治疗。在手术区姑息放疗期间,观察到肺部肿瘤进展。
由于CLDN18.2表达确定为3+/60%,故患者入组CT041临床试验。入组后,患者现接受了淋巴细胞清除治疗,之后回输CT041。治疗后4周初次评估,就达到部分缓解(PR),肺转移靶病灶随后消失并达到完全缓解。直到2023年7月最后一次随访时,肿瘤仍控制良好。
目前有多款CAR-T临床实验正在进行中,主要针对以下癌种:
Claudin18.2:用于胃癌,胰腺癌等;
间皮素(mesothelin):用于治疗间皮瘤、胰腺癌、卵巢癌、肺癌;
CEA:用于治疗肺癌、结肠癌、胃癌、乳腺癌和胰腺癌;
MUC-1:用于治疗肝癌、肺癌、胰腺癌、结肠癌、胃癌;
GPC3:用于治疗肝癌;
GUCY2C:用于结直肠癌;
PSMA:用于前列腺癌等;
EGFRvII:用于治疗神经胶质瘤、头颈部肿瘤;
B7-H3:用于治疗尤文肉瘤、横纹肌肉瘤、肾母细胞瘤、神经母细胞瘤和髓母细胞瘤以及特别难以治疗的脑干肿瘤(DIPG)。
上述癌种患者若想寻求CAR-T疗法帮助或检测相关靶点,可以致电医学部,进行初步评估。
图1患者治疗前后肺部病变的放射学评估
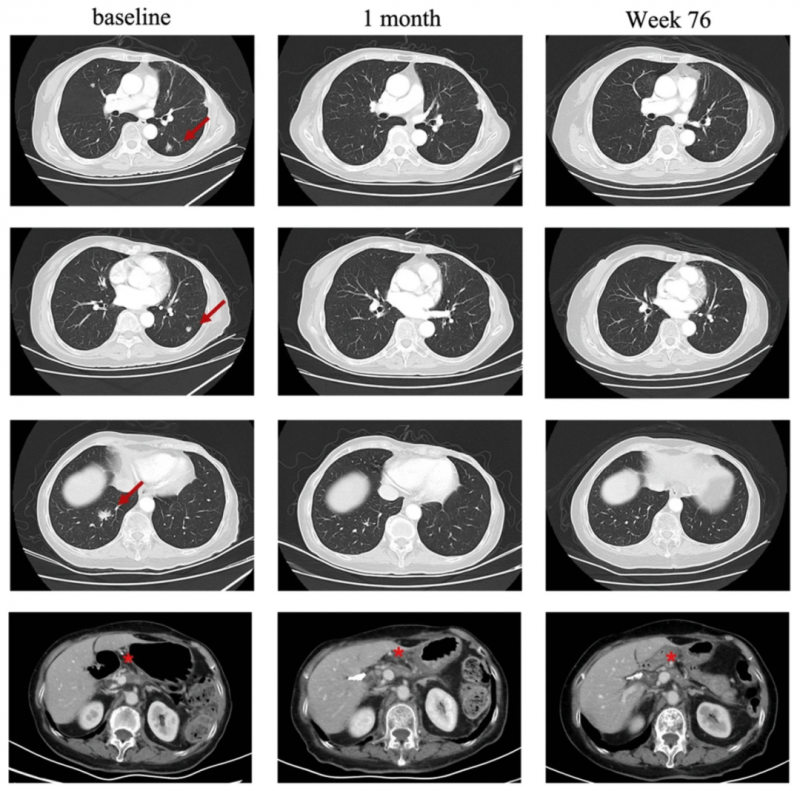
▲图片源自BMC,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:红色箭头表示目标病变。★表示原发病变
GPC3CAR-T:让晚期肝癌患者重燃长生存希望,总生存时间超8年

▲截图源自WILEYOnlineLibrary
肝细胞癌(HCC),尤其是伴下腔静脉癌栓(IVCTT)的治疗手段有限,很多患者在肝切除后的中位总生存时间仅为17.76个月,因此,迫切需要研发新的治疗方法,提高患者的生存率。近年研究发现,局部治疗+CAR-GPC3T(GPC3CAR-T)细胞治疗,对晚期肝细胞癌患者具有较好的效果。
国际知名免疫学期刊《CancerCommunications》报道了CAR-GPC3T细胞治疗肝细胞癌的令人惊艳的研究结果。
一例54岁男性Ib期肝细胞癌患者,既往患有乙型肝炎肝硬化,确诊后先后接受了肿瘤手术切除、经肝动脉介入化疗栓塞术(TACE)、微博消融术(MWA)、伽玛刀放射治疗(GKRS)等多种治疗后,肿瘤仍然复发,出现腹膜后淋巴结转移和下腔静脉癌栓,临床上已无更好的治疗方案。
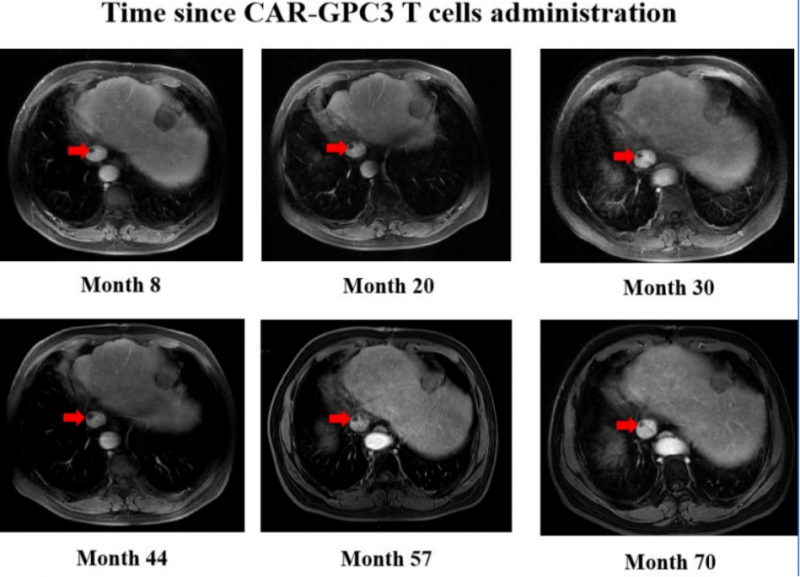
万般无奈下,患者入组了在中国进行的CAR-GPC3T细胞临床试验,并先后进行了两个周期的GPC3CAR-T细胞输注。结果显示:
病灶缩小:首次输注后2周,腹膜后LM的大小开始减小;病灶短轴和长轴直径分别减小了5.2%和4.5%,最后一次输注后的第7天,病变短轴减少7.4%。
AFP下降:AFP水平从1,301ng/mL降至565ng/mL,下降高达56.6%!
病情缓解:根据实体瘤疗效评估标准(RECIST;1.1版),患者疾病状态保持稳定达7个月。目前已保持无病状态超过5年,总生存时间超过8年。
这意味着,中国成功研发的针对实体瘤CAR-T疗法,让这例晚期肝癌患者达到了临床治愈!
PRGN-3005:治疗晚期铂耐药卵巢癌,疾病控制率高达85.7%
PRGN-3005属于一种UltraCAR-T细胞疗法,利用非病毒基因递送技术制造,消除了体外扩增并减少了制造时间,允许在非病毒基因转移后第二天快速给药,降低了生产时间和成本,而且还可获得更精确的肿瘤靶向,有助于颠覆当前CAR-T细胞治疗的格局,目前正被评估治疗晚期复发性卵巢癌、输卵管癌或原发性腹膜癌等。
《临床肿瘤学杂志》报道了一项PRGN-3005治疗复发或难治性(r/r)卵巢癌的1/1b期临床研究。共入组25例可评估的患者,中位年龄为64岁(38-76),并接受过中位8种既往治疗方案的大量预处理。入组后将其分为三组,分别经腹膜内(IP)输注(C1,n=12)、静脉(IV)输注(C2,n=6)、环磷酰胺LD治疗(IVLD,n=7)。
治疗后,所有受试者中20%的至少1个目标病变出现缓解(RECIST1.1评估)。其中,IVLD组患者首次再分期时的
疾病控制率(DCR)为85.7%,靶肿瘤负荷降低4/7(57%),CA125平均降低27.4%。12个月后接受第二次PRGN-3005输注后,一名患者的目标肿瘤负荷减少了28%。且未发生与PRGN-3005相关的剂量限制性毒性、神经毒性、3级细胞因子释放综合征(CRS)等不良反应。
上述结果表明,PRGN-3005UltraCAR-T疗法具有良好的耐受性,在治疗卵巢癌,观察到令人鼓舞的疾病控制率(DCR)率,且总体肿瘤负荷减少。
小编有话说
CAR-T疗法在治疗血液系统恶性肿瘤方面具有广阔的前景,并有多款产品获批上市,不过其在实体瘤治疗方面仍处于临床实验阶段,但小编相信随着CAR-T代数的更迭、更多明星靶点的出现,以及CAR-T在增殖、细胞因子释放等方面的改进,CAR-T攻克晚期实体瘤将指日可待!事实上,目前已有众多CAR-T治疗实体瘤的临床试验相继开展,而且也有幸运的患者得到完全缓解。目前CAR-T、TCR-T、TIL等多项T细胞疗法的临床实验正在招募各类实体瘤患者,对现有治疗手段不满意或想寻求新技术帮助的患者,将病历资料、近期病理报告等,提交至医学部,进行初步评估。
参考资料
[1]https://www.nbcnews.com/health/health-news/gene-therapy-pancreatic-cancer-experimental-approach-shrank-tumors-one-rcna31437
[2]https://ascopubs.org/doi/10.1200/JCO.2023.41.16_suppl.5590
[3]https://onlinelibrary.wiley.com/doi/10.1002/cac2.12472
[4]https://jhoonline.biomedcentral.com/articles/10.1186/s13045-023-01491-9#MOESM1
[5]https://www.carsgen.com/en/news/1105/
[6]https://www.carsgen.com/en/pipeline/new-pipeline/
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。