时间:2024-04-22 14:13 编辑:全球肿瘤医生网
2024年AACR年会更新TCR-T细胞疗法治疗肝癌进展,还可以精准打击肺癌、胰腺癌等实体瘤
备受瞩目的2024年美国癌症研究协会(AACR)年会(第115届),近日在美国圣地亚哥举行,作为历史悠久且权威的肿瘤研究学术盛会之一,AACR一直引领着全球肿瘤研究的前沿。本次大会也不负所望的公布了多项与细胞治疗相关的创新研究成果,其中就包括5例复发难治性肝母细胞瘤患者,经TCR-T治疗后,存活超9年的报道,相关摘要已在官方期刊《CANCER RESEARCH》更新。
TCR-T疗法亮相2024 AACR:治疗GPC3肝母细胞瘤效果惊艳
GPC3(Glypican-3)在多种实体瘤中高表达,如肝细胞癌、肝母细胞瘤、鳞状细胞肺癌、卵巢透明细胞癌等,但几乎不在正常组织中表达,因而被认为是肿瘤免疫治疗的理想靶点。
研究人员从1例接受GPC3衍生肽治疗的HLA-A*02:01阳性难治性肝母细胞瘤患者的外周血单核细胞中,建立了具有高亲合力的肽特异性CTL克隆,并通过创建病毒载体,制备针对GPC3的TCR-T细胞。
研究结果显示,5例复发及难治性肝母细胞瘤患者,治疗后均存活9年以上,且未见复发表现。
综上,这种TCR-T疗法可杀伤呈递GPC3衍生肽的癌细胞,在治疗HLA-A2阳性并表达GPC3癌症中,具有广阔的应用潜力。其实,除了肝母细胞瘤外,TCR-T疗法在多种实体瘤治疗领域,都表现出不俗的成绩!那么这款新兴疗法究竟有何魔力呢?哪些实体瘤患者可以从中获益呢?且听小编一一介绍。
TCR-T疗法:实体瘤新利器
人体内被誉为免疫战士的T细胞(即T淋巴细胞),可以抵御并消灭癌细胞,随着多款CAR-T疗法相继获批上市,也彰显了T细胞在治疗血液肿瘤领域的巨大威力!TCR-T与CAR-T疗法类似,都是利用经基因修饰改造的T淋巴细胞,获得肿瘤抗原特异性的一种细胞免疫疗法,但二者的抗原识别机制并不相同。CAR-T细胞仅能与肿瘤细胞表面蛋白结合;而TCR-T细胞既可识别膜蛋白,又可识别细胞内蛋白(详见下图)。
图1 TCR-T与CAR-T,与肿瘤细胞的识别及作用模式
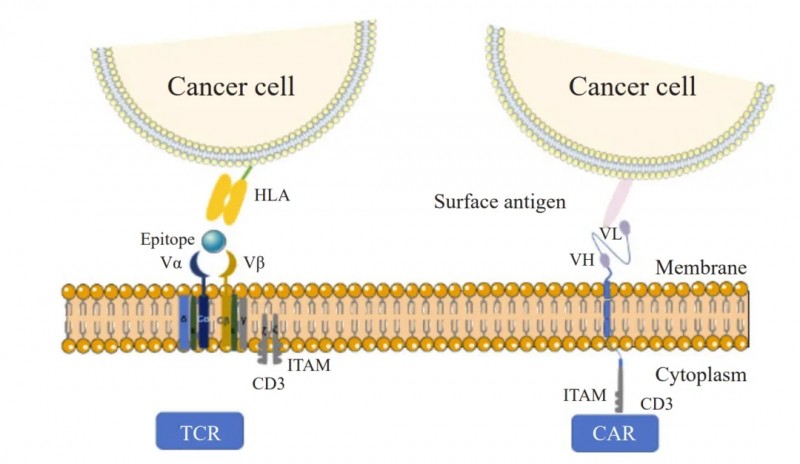
▲图源China Oncology,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
TCR-T即T细胞受体工程化T细胞疗法(T-cell receptor engineered T cell therapy,TCR-T),是将TCR基因序列,通过基因工程技术,转移到T细胞中,相当于给T细胞安装一个精密的感知器,使T细胞能特异性识别肿瘤抗原,把狡猾的肿瘤细胞揪出来,并精准杀死癌细胞。与CAR-T疗法相比,TCR-T具有更广泛的靶点,目前已在多项临床试验,尤其是在治疗实体瘤领域中,取得了亮眼的成绩(详见下表)!下面全球肿瘤医生网小编帮大家简单汇总一下TCR-T治疗部分实体瘤的惊艳疗效,以供参考。
表1 目前已经进入临床试验阶段的代表性靶点及TCR-T疗法
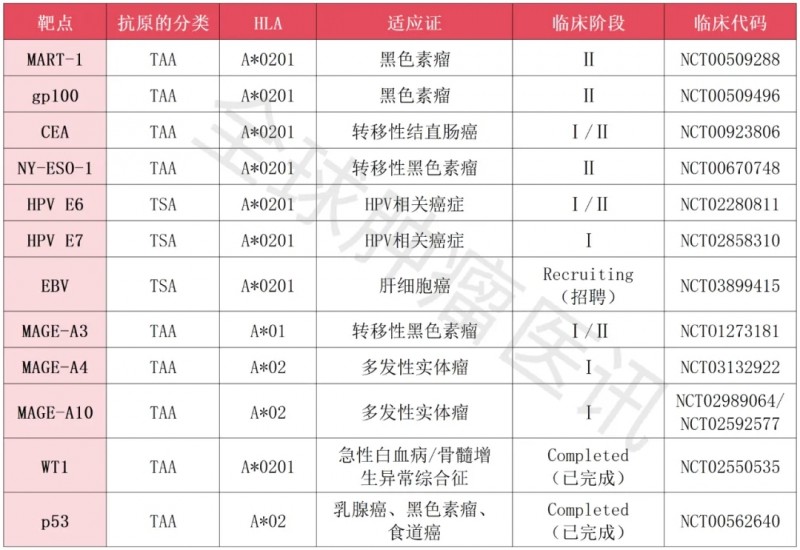
▲数据源自China Oncology,全球肿瘤医生网医学部整理
SCG101治疗乙肝病毒相关肝细胞癌,抗癌和抗病毒一箭双雕
SCG101是一款由星汉德生物公司研发的乙肝抗原特异性的TCR-T细胞疗法,该产品最为惊喜的是,具有抗肿瘤和抗病毒的双重功效,通过特异性靶向HBV抗原相关的T细胞表位,可清除HBV-HCC肿瘤细胞、HBV-DNA整合的癌前病变细胞、HBV感染细胞,目前已获美国食品药品监督管理局(FDA)、中国国家药品监督管理局(NMPA)、新加坡卫生科学管理局(HSA)、香港卫生署(DOH)的批准,用于乙肝感染相关肝癌的临床研究,将为乙肝病毒相关肝细胞癌患者带来新的希望与选择!
SCG101的突破性临床数据,已在2023年国际细胞与基因治疗大会(ISCT)上公布,本例乙型肝炎病毒(HBV)相关肝细胞癌(HCC)患者,在接受SCG101单药治疗后,肿瘤及HBV感染均得到缓解。
1、肿瘤改善:该患者在治疗第28天,获得部分缓解(PR),肿瘤靶病灶缩小66%(相比基线);并且在治疗第4个月时,进一步缩小74.5%;而另一处病灶则完全消失。截至数据统计时,该患者处于持续缓解状态,肿瘤未进展时间已超过6.9个月!
图2 HBV相关HCC患者回输SCG101前后的影像学变化
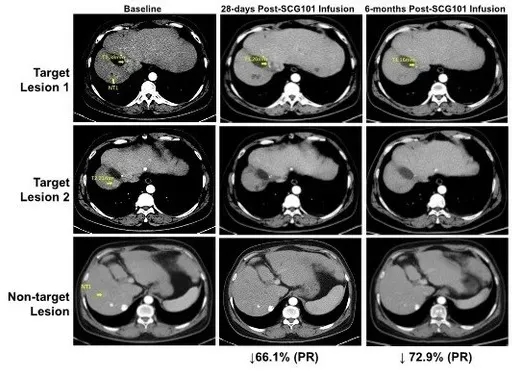
▲图源CISION,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
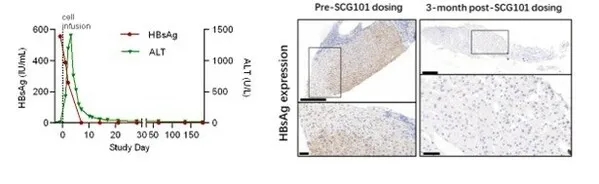
2、HBV感染缓解:肝脏免疫组化结果显示,患者回输SCG101前后,HBsAg(HBV血清学标志)从557.96 IU/mL(治疗前),降至1.3IU/mL(回输SCG101后第7天)、0.08 IU/mL(回输SCG101后第28天)。乙肝表面抗原阳性肝细胞更是实现100%清除!
图3 回输SCG101前后,HBsAg值变化
TCR-T疗法急招肝癌患者:
目前有一款TCR-T疗法的临床试验,正在招募肝癌患者,主要的纳入标准如下:
1、患有原发性肝细胞癌;
2、患有慢性乙肝感染史;
3、常规治疗无效获不适合进行常规治疗;
4、无肝硬化病史或仅有代偿性肝硬化;
5、未发生肝癌脑转移。
想参加的患者可将治疗经历、出院小结、近期病理报告等资料,提交至医学部,了解详细的入排标准,或进行初步评估。
NY-ESO-1治疗非小细胞肺癌,原发灶及转移灶
非小细胞肺癌(NSCLC)占所有肺癌病例的80%以上,包括三种常见的组织学亚型,即肺腺癌(LADC)、肺鳞状细胞癌(LSCC)、大细胞肺癌(LCLC)。晚期NSCLC(IIIb期和IV期)患者通常没有合适的手术方案可选,只能无奈选择化疗、放射治疗、靶向治疗等全身治疗手段。然而,放疗和化疗副作用较多,而且很多患者最终会因耐药性而导致化疗失败。加之,大多肺癌患者对免疫检查点抑制剂没有反应。因此,对于那些对免疫检查点治疗无效的患者,迫切需要新的免疫治疗策略。而近年来TCR-T疗法的出现,为晚期肺癌患者带来一丝曙光!
《肿瘤学快报》发表了一项NY-ESO-1(一款TCR-T细胞产品)治疗转移性非小细胞肺癌的临床研(NCT02457650)结果。入组的4例HLA-A2阳性的转移性非小细胞肺癌(NSCLC)患者,在入组后现接受淋巴细胞清除治疗,之后回输NY-ESO-1 TCR-T细胞,最后再结合IL-2全身给药治疗。在可评估疗效的2例患者中,结果显示,患者1达到疾病稳定(SD),且持续近3个月。患者2在治疗后,经历了持续4个月的部分缓解(PR)。
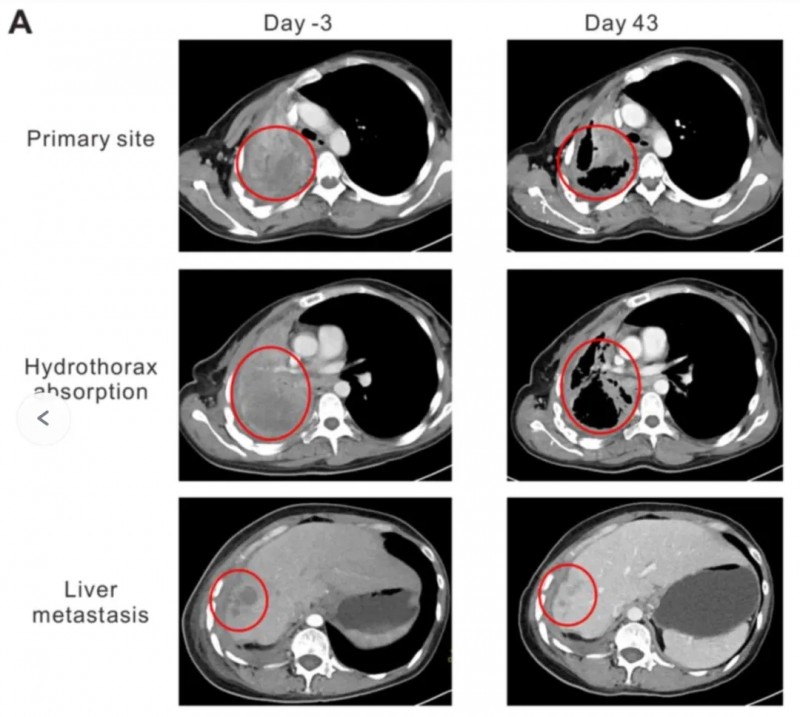
特别值得一提的是,患者2为1名44岁携带EGFR突变的转移性肺腺癌(LADC)女性患者,既往接受过(多西紫杉醇+卡铂)联合化疗、吉非替尼、厄洛替尼治疗等,但肿瘤依然进展,并出现右肺门、纵隔、胸膜和肝脏转移等表现。入组深圳市第二人民医院肿瘤科,接受NY-ESO-1回输后第43天,根据RECIST 1.1评定疗效为部分缓解(PR)。CT扫描示:
1、原发性肺肿瘤和肝转移的消退、胸水的吸收和肺部的重新扩张(图2A)。
2、肺部原发病灶尺寸由958654 mm,缩小至644454 mm。
3、肝转移病灶也从19.819.620 mm,缩小至101010 mm。
图4 患者2回输NY-ESO-1前后CT变化
▲图源oncology Letters,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:CT扫描示原发肿瘤位于右肺门。
①在输注TCR-T细胞前,病灶已转移至纵隔、右胸膜、右肝叶和肝包膜。
②2016年1月(第43天),在第1次T细胞输注2个月后,CT扫描示,原发性肺肿瘤和肝转移灶客观消退,胸水吸收和肺部重新扩张。
TCR-T治疗转移性胰腺癌,部分缓解率达72%
世界知名期刊《新英格兰杂志(The NEW ENGLAND JOURNAL of MEDICINE)》,发表了一位进行性转移性胰腺癌患者,在接受TCR-T治疗后,肿瘤快速消退的病例报告。
该患者为一位71岁的女性(CRI-4483),在67岁时确诊KRAS突变的胰腺癌,既往接受过手术、放化疗,但病情持续进展。抱着最后一线希望,该患者入组参与了KRASG12D靶向的TCR-T治疗。并在细胞输注前5天,接受预处理治疗(托珠单抗+环磷酰胺),之后回输TCR-T细胞;并在细胞输注后18小时,接受大剂量白细胞介素2(IL-2)治疗。
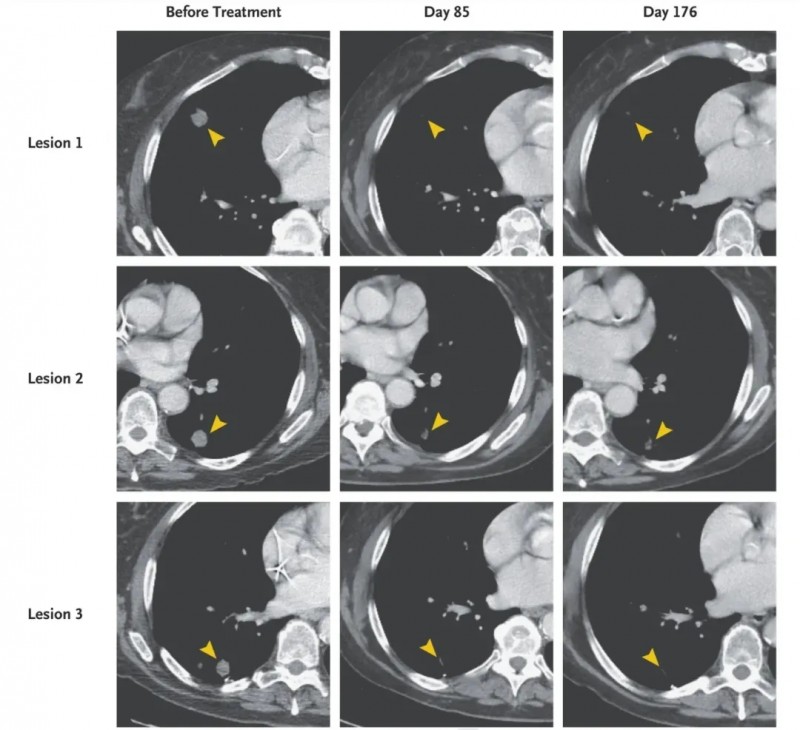
幸运的是,该患者在TCR-T治疗后第21天,血小板及绝对中性粒细胞计数得以恢复;治疗第1个月时计算机断层扫描显示,患者肺转移病灶消退(详见下图);治疗后6个月,部分缓解(PR)率达到72%!
本病例报告再次用数据表明,针对KRAS G12D热点突变的TCR-T疗法,有助于转移性胰腺癌的消退。同时也彰显了TCR-T疗法在治疗胰腺癌和其他表达KRAS G12D的癌症中,具有广阔的应用潜力。
图5 本例胰腺癌患者在TCR-T治疗前后,胸部计算机断层扫描对比
▲图源NEJM,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
TCR-T疗法作为一种新型抗肿瘤方案,虽与CAR-T同属于T细胞疗法,但其具有归巢能力强、靶点范围更广的优点,如果说CAR-T疗法是治疗血液肿瘤的利器,那么TCR-T疗法就是治疗实体瘤的新型武器,其在治疗肝癌、非小细胞肺癌、胰腺癌、黑色素瘤、宫颈癌、滑膜肉瘤等多种实体瘤方面具有独特的优势。我们也期望未来会有越来越多的靶点和TCR-T细胞产品问世,让更多的实体瘤患者获益!
目前正有几款在研的TCR-T疗法,正在招募乙型肝炎病毒相关肝细胞癌、晚期宫颈癌、肛门癌、头颈部肿瘤(喉癌、口腔癌)等癌种!想寻求TCR-T细胞疗法或国内外其他治疗新技术帮助的病友,可咨询医学部,详细评估病情!
参考资料
[1]Tsuyoshi Terada,et al.T cell receptor-engineered T cell therapy using TCR gene derived from an HLA-A2 hepatoblastoma patient who was completely cured by administration of glypican-3 peptide vaccine.2024.AACR.
https://aacrjournals.org/cancerres/article/84/6_Supplement/3614/737210/Abstract-3614-T-cell-receptor-engineered-T-cell
[2]Weitao Z,et al.TCR-T immunotherapy for the treatment of solid tumor: current status, challenges and future prospects[J]. China Oncology, 2023, 33(7): 707-716.
http://www.china oncology.com/EN/abstract/abstract1917.shtml
[3]Xia Y,et al.Treatment of linkstatic nonsmall cell lung cancer with NYESO1 specific TCR engineeredT cells in a phase I clinical trial: A case report[J]. oncology letters, 2018, 16(6): 6998-7007.
https://www.spandidos publications.com/10.3892/ol.2018.9534?text=abstract
[4]Simnica D,et al.Neoantigen T-Cell Receptor Gene Therapy in Pancreatic Cancer[J]. The New England Journal of Medicine, 2022, 387(6): 573-573.
https://www.nejm.org/doi/full/10.1056/NEJMoa2119662
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。