时间:2024-08-22 13:38 编辑:全球肿瘤医生网
CAR-T疗法Breyanzi在欧盟获批,中国CLDN18.2 CAR-T细胞疗法Satri-cel疾病控制率高达96.1%
近期,CAR-T研发领域有两项重要进展震撼全球,首先是血液肿瘤领域大名鼎鼎的Breyanzi再添新战绩,欧洲药品管理局正式批准其新适应症申请,为晚期血癌患者点亮了新的希望;另一项就是我国自研的治疗胰腺癌和胃癌的CAR-T细胞疗法Satri-cel,2期关键试验顺利完成了患者入组。
作为我国首创的CLDN18.2 CAR-T疗法,Satri-cel的1期战绩惊人,不仅获得了高达96.1%的疾病控制率!更是在北肿专家团队的带领下,成功亮相2024 ASCO大会,并引起广泛关注,是我国实体瘤CAR-T研发领域的重要里程碑!为实体瘤患者点亮了长生存的希望!
Breyanzi再添新战绩,欧洲药品管理局批准新适应症申请
2024年8月19日,百时美施贵宝公司研发的一款新型CAR-T细胞产品Breyanzi,获欧洲药品管理局(EMA)的新适应症申请验证,用于既往接受过2种全身治疗的成年复发或难治性滤泡性淋巴瘤(FL)的治疗。
滤泡性淋巴瘤是第二大最常见的非霍奇金淋巴瘤(NHL)类型,占所有NHL的20%~30%,且FL的治疗效果往往不尽如人意,很多患者会在接受一线治疗后复发,更遗憾的是,每次复发后,预后都可能恶化。据统计,FL一线免疫化疗后24个月内疾病进展患者的总生存期(OS)较差,5年OS率为64%,而Breyanzi的出现为这些患者带来了新的曙光!

▲截图源自businesswire
Breyanzi:被欧美日盖章认可的CAR-T细胞疗法
Breyanzi(利基迈仑赛,lisocabtagene maraleucel,liso-cel)是一种针对CD19的CAR-T细胞疗法,具有4-1BB共刺激域,可增强CAR-T细胞的扩增和持久性。Breyanzi由患者自身的T细胞制成,医生将采集到的T细胞,经过基因改造技术,制备成CAR-T细胞,再回输到患者体内,以精准识别并杀伤特定的癌细胞。Breyanzi此前已获美国食品药品监督管理局(FDA)批准,用于治疗以下癌种:
1、2024年3月15日,获批用于复发或难治性慢性淋巴细胞白血病(CLL)、小淋巴细胞淋巴瘤(SLL)的治疗。
2、2024年5月31日,获批用于治疗复发或难治性套细胞淋巴瘤(MCL)。
3、2024年5月15日,获FDA加速批准,用于治疗既往接受过2种治疗的复发或难治性滤泡性淋巴瘤(FL)。
除了在美国和欧盟获批外,Breyanzi还在日本获得批准,用于治疗既往接受过一线全身治疗、二线全身治疗的复发或难治性滤泡性淋巴瘤(FL)患者,它是全球首个在二线治疗中获批的CAR-T药物!
Breyanzi重锤淋巴瘤,2期临床总体缓解率高达97%
Breyanzi本次获得欧洲药品管理局批准,主要基于2期TRANSCEND(NCT04245839)临床研究的惊艳数据!本次研究共有139名患者被纳入滤泡性淋巴瘤(FL)队列,并接受了白细胞分离术[3L+(n =114),2L(n =25);2L或2L+(n=139)]。在数据截止时,130例FL患者接受了Breyanzi回输治疗,中位年龄为60岁。结果显示如下:
1、在3L+滤泡性淋巴瘤(FL)患者中:总体缓解率(ORR)高达97%!完全缓解(CR)率高达94%(92/95),12个月的无进展生存期(PFS)率为81%(95%CI:71.4-87.2);12个月的总生存期(OS)率为92%(95%CI:84.8-96.0)。
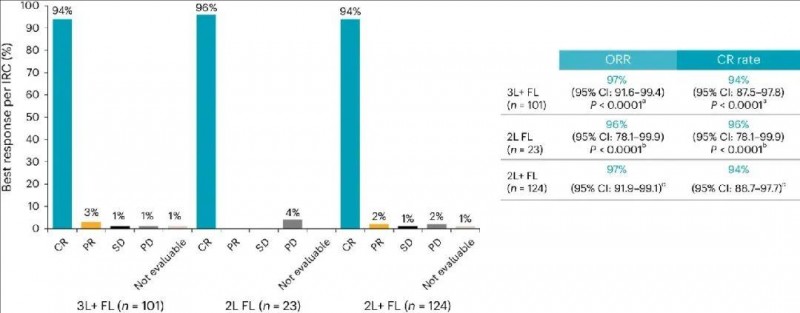
▲图源nature,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2、在2L 滤泡性淋巴瘤(FL)患者中:总体缓解率(ORR)高达96%,所有应答者均达到完全缓解(CR);12个月的无进展生存期(PFS)率高达91%(95%CI:69.5-97.8);12个月总生存期(OS)率更是高达96%(95%CI:72.9-99.4)。
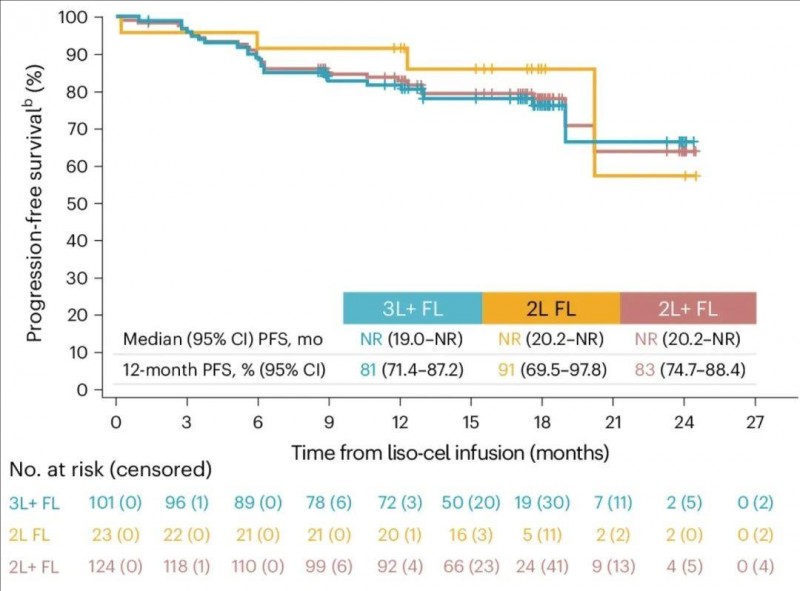
▲图源nature,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
中国首创CAR-T II期试验顺利入组,1期疾病控制率高达96.1%
2024年8月19日,科济生物官网宣布,中国首创Claudin18.2 CAR-T细胞疗法satri-cel的关键II期临床试验,已完成患者入组。这一重要里程碑标志着我国在CAR-T细胞疗法治疗实体瘤领域,又迈出了坚实的一步!
▲截图源自CARSGEN
中国自研Satri-cel,点亮胃癌和胰腺癌治疗新希望
Satri-cel(satricabtagene autoleucel,研发代码:CT041)是一种针对Claudin18.2的自体CAR-T细胞候选产品,主要针对胃或胃食管连接部癌(GC/GEJ)、胰腺癌(PC)。
2022年1月,美国FDA授予Satri-cel再生医学先进疗法(RMAT)资格,用于Claudin18.2(CLDN18.2)阳性晚期胃或胃食管连接部癌(GC/GEJ)的治疗;2021年欧洲药品管理局(EMA)授予其孤儿药资格,用于晚期胃癌的治疗,有望成为全球首创产品。
北肿团队携Satri-cel亮相2024 ASCO大会,1期疾病控制率高达96.1%
此前Satri-cel就曾在世界舞台大放异彩,我国北京大学肿瘤医院研究团队,就曾携satri-cel的1期临床惊艳数据(NCT03874897),亮相2024年ASCO(美国临床肿瘤学会)大会,这是首个应用CLDN18.2-CAR-T细胞治疗实体瘤的临床研究数据,相关结果同步发表在全球顶级医学期刊《Nature Medicine》上。
本次入组的51例基线时有靶病变的CLDN18.2阳性晚期胃或胃食管连接部癌(GC/GEJ)患者,在入组接受satri-cel(即CAR-T细胞)单药治疗后,疾病控制率(DCR)高达96.1%(49/51)!客观缓解率(ORR)为54.9%(28/51),中位无进展生存期(mPFS)为5.8个月(95%CI,4.1,8.0),中位总生存期(mOS)为9.0个月(95%CI,7.0,11.9),中位缓解时间(mDOR)为6.4个月(95%CI,4.6,8.3)。
▼satri-cel疗效的泳道图
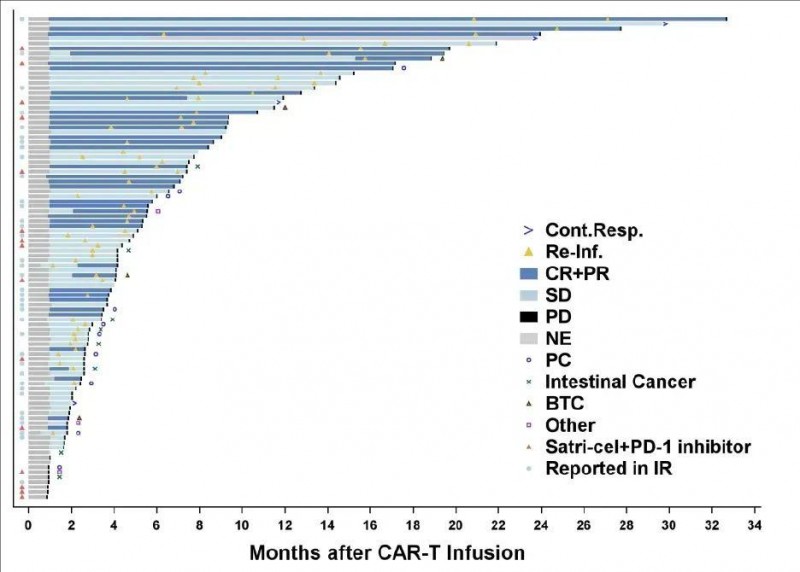
▲图源nature medicine,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
CAR-T细胞招募进行时
好消息是,天价CAR-T细胞终于启动临床招募啦,这也意味着中国患者也有机会免费获得这款抗癌黑科技的帮助啦!
【非霍奇金淋巴瘤CAR-T细胞】
①项目名称:全人源抗CD19和CD22 CAR-T细胞,治疗复发/难治性B细胞非霍奇金淋巴瘤的Ⅰ/Ⅱ期临床研究。
②项目编号:CTR20212328。
③分期:Ⅰ期和Ⅱ期。
④治疗线数:二线失败。
⑤突变基因:CD19。
⑥适合人群:复发/难治性B细胞非霍奇金淋巴瘤患者。
【胃癌CAR-T细胞】
①项目名称:CT041自体CAR-T细胞注射液,在晚期胃/食管胃结合部腺癌和胰腺癌受试者中的Ⅰb/II期临床试验。
②项目编号:CTR20201940。
③药品名称:CT041。
④分期:Ⅱ期。
⑤治疗线数:二线失败。
⑥突变基因:Claudin 18.2。
⑦适合人群:经病理确诊的晚期胃/食管胃结合部腺癌患者,且接受至少二线治疗失败;或经病理确诊的晚期胰腺癌患者,且至少一线治疗失败的患者。
【胰腺癌CAR-T细胞】
①项目名称:CT041自体CAR-T细胞注射液,在晚期胃/食管胃结合部腺癌和胰腺癌受试者中的Ⅰb/Ⅱ期临床试验。
②项目编号:CTR20201940。
③药品名称:CT041自体CAR-T细胞注射液。
④分期:Ⅰ期和Ⅱ期。
⑤治疗线数:二线失败。
⑥突变基因:Claudin 18.2。
⑦适合人群:至少二线治疗失败的晚期胃/食管胃结合部腺癌和至少一线治疗失败的晚期胰腺癌。
想要参加上述临床试验的患者,可将基因检测报告、近期病理报告、出院小结等资料,提交至医学部,了解详细的入排标准,或初步评估是否有机会参加临床试验。
小编寄语
随着CAR-T、TCR-T、TIL、NK细胞疗法、癌症疫苗等新型疗法的出现,恶性肿瘤的治疗已获得长足的进展。在传统三大疗法(手术、放化疗)的基础上,辅以其他新型疗法,助癌症患者降低癌症复发/转移风险,尽可能延长生存时间、提高生存质量。
CAR-T细胞作为其中的佼佼者,近年来各国研发热情不断高涨,除了中美外,斯洛伐克、印度、欧盟等多国也不断加入研发大军中。我国现阶段共有20多家企业正在布局CAR-T疗法的研发,其中涵盖驯鹿医疗、复星凯特、传奇生物、科济生物、等多家制药巨头。全球肿瘤医学部小编也期望随着越来越多靶点和CAR-T产品的不断出现,能让更多的晚期癌症患者获益,最终实现巩固疗效、降低复发、提高生存质量、延长生存期的美好愿景!
若您对当前治疗方案不满意,或想寻求CAR-T、CAR-NK、TCR-T、TIL等国内外新型抗癌新技术的帮助,可将完整的病理报告、影像学报告、治疗经历、出院小结等资料,提交至医学部,进行初步评估或申请国内外抗癌专家会诊。
参考资料
[1]Morschhauser F,et al.Lisocabtagene maraleucel in follicular lymphoma: the phase 2 TRANSCEND FL study[J]. Nature Medicine, 2024: 1-9.
https://www.nature.com/articles/s41591-024-02986-9
[2]Qi C,et al.Claudin18. 2-specific CAR T cells in gastrointestinal cancers: phase 1 trial final results[J].Nature Medicine, 2024:1-11.
https://www.nature.com/articles/s41591-024-03037-z
[3]https://www.businesswire.com/news/home/20240816750573/en/European-Medicines-Agency-Validates-Bristol-Myers-Squibb%E2%80%99s-Application-for-CAR-T-Cell-Therapy-Breyanzi-for-Relapsed-or-Refractory-Follicular-Lymphoma
[4]https://www.carsgen.com/en/news/20240819/
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。