时间:2024-08-22 16:31 编辑:全球肿瘤医生网
2024年6月17日中国药监局批准枸橼酸依奉阿克胶囊(Envonalkib、安洛晴、TQ-B3139)用于治疗ALK阳性的局部晚期或转移性非小细胞肺癌
2024年6月17日,中国国家药品监督管理局(NMPA)批准正大天晴药业集团研发的枸橼酸依奉阿克胶囊(Envonalkib、安洛晴、TQ-B3139)用于治疗未经过间变性淋巴瘤激酶(ALK)抑制剂治疗的ALK阳性的局部晚期或转移性非小细胞肺癌(NSCLC)患者。

依奉阿克在中国获批上市
获批依据
依奉阿克胶囊的此次的获批上市,其详细获批依据主要基于一项多中心、随机、开放标签、活性对照的III期临床试验(NCT04009317),即TQ-B3139-III-01研究。以下是详细的获批依据:
研究设计
研究共招募了264名受试者,以1:1的比例随机分配接受依奉阿克或克唑替尼治疗。受试者的基线特征包括中位年龄53岁,65岁以下受试者占比85.2%;肺腺癌占比93.9%;从未吸烟受试者占比65.9%。这些特征与ALK阳性NSCLC患者的流行病学特点高度一致。
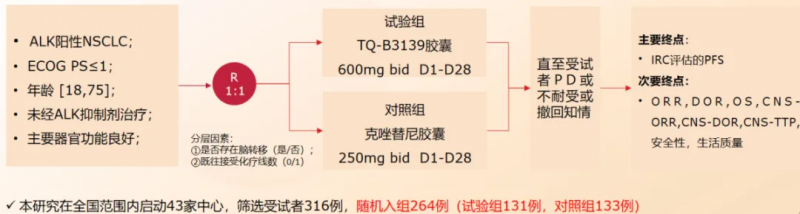
TQ-B3139-III-01研究设计
治疗方案
依奉阿克组接受依奉阿克胶囊口服治疗,克唑替尼组接受克唑替尼胶囊口服治疗,直至疾病进展或出现不可耐受的毒性反应。
研究终点
主要终点:根据RECIST 1.1标准,由独立审查委员会(IRC)评估的无进展生存期(PFS);
次要终点:包括研究者评估的PFS、IRC评估的客观缓解率(ORR)、疾病控制率(DCR)、中枢神经系统客观缓解率(CNS-ORR)等。
研究结果
无进展生存期(PFS):
●IRC评估的中位PFS:依奉阿克组为24.87个月(95% CI: 15.6430.36),克唑替尼组为11.60个月(95% CI: 8.2813.73);依奉阿克组相比克唑替尼组,PFS显著延长(HR=0.47,P0.0001);
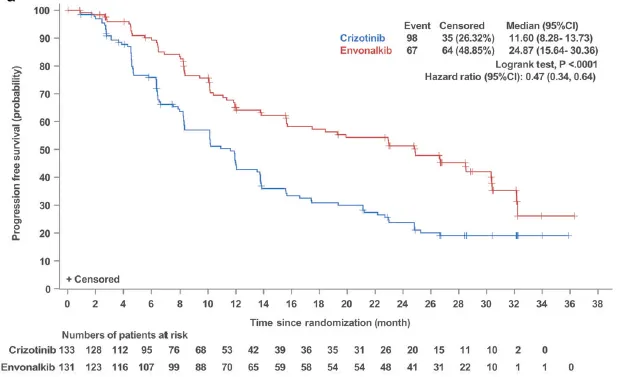
IRC评估的中位PFS
●研究者评估的中位PFS:依奉阿克组为28.7个月,克唑替尼组为12.0个月(HR=0.42,P0.0001),结果与IRC评估一致。
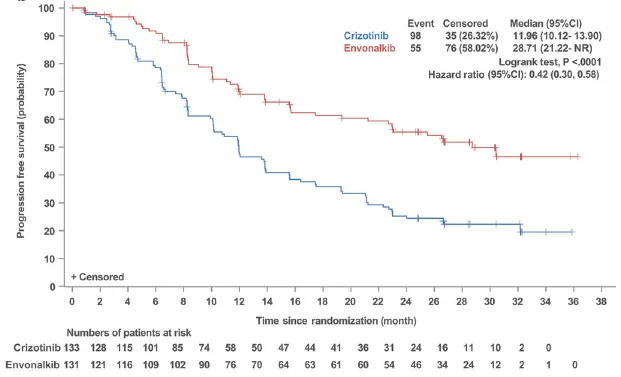
IRC评估的中位PFS
客观缓解率(ORR):
●IRC评估的ORR:依奉阿克组为81.68%,克唑替尼组为70.68%(p=0.056);
●研究者评估的ORR:依奉阿克组为81.0%,克唑替尼组为73.7%。
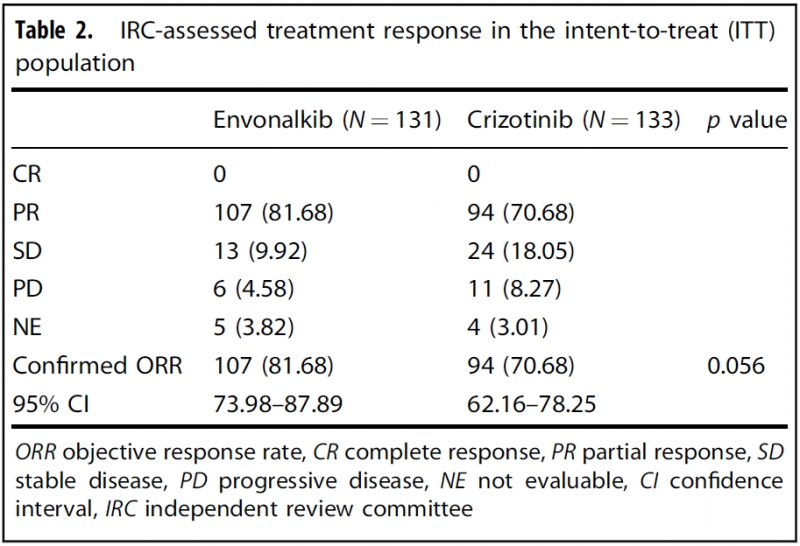
客观缓解率
缓解持续时间(DOR):
●依奉阿克组的中位DOR为25.79个月(95% CI: 16.5329.47),克唑替尼组为11.14个月(95% CI: 9.2316.59)(p=0.0003)。
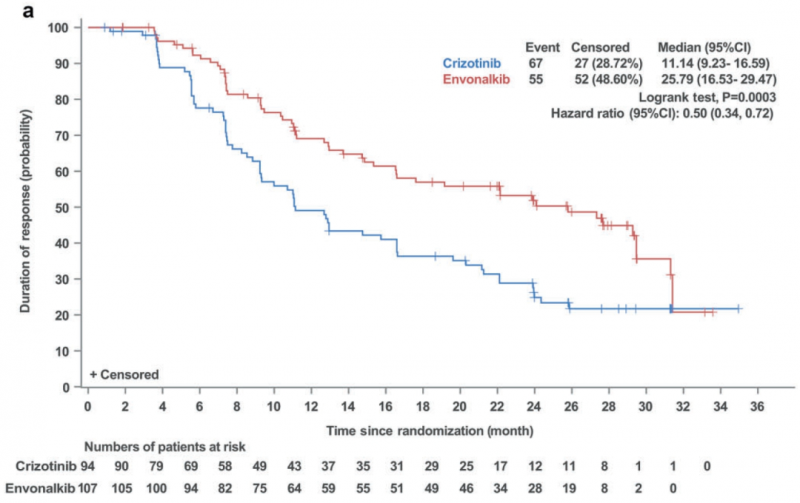
缓解持续时间
中枢神经系统客观缓解率(CNS-ORR):
●在基线脑靶病灶受试者中,依奉阿克组的CNS-ORR为78.95%,克唑替尼组为23.81%;依奉阿克组在脑转移患者中的疗效显著优于克唑替尼组(p=0.0030)。
总生存期(OS):
●OS数据尚不成熟,两组中位OS均未达到;依奉阿克组和克唑替尼组的24个月OS率分别为78.4%和75.0%。
安全性评估
●依奉阿克组和克唑替尼组分别有55.73%和42.86%的参与者出现3级治疗相关不良事件(TRAEs);
●依奉阿克组因TRAE导致的停药率较低(4.6% vs 3.0%),且大多为1-2级AEs,血液相关毒性较低。
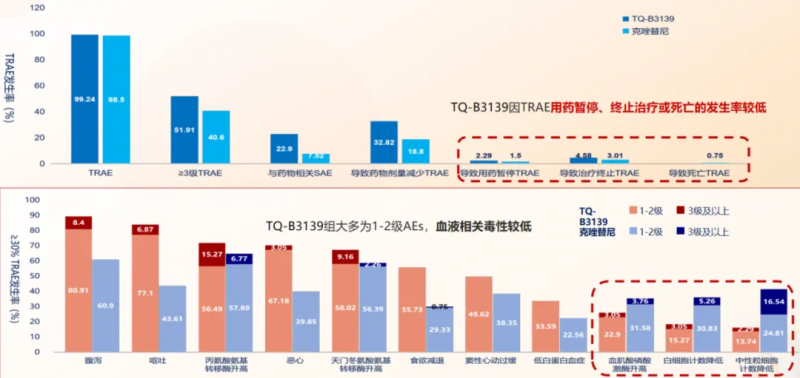
依奉阿克III期研究不良反应
研究意义
依奉阿克作为国产新一代ALK抑制剂,其III期临床试验结果显示,在疗效和安全性方面均表现出显著优势,特别是针对脑转移患者的疗效尤为突出;这一研究结果为依奉阿克胶囊的获批上市提供了强有力的临床依据,也为ALK阳性晚期NSCLC患者提供了新的治疗选择。
结语
依奉阿克胶囊的获批上市,为ALK阳性非小细胞肺癌患者带来了新的治疗选择,其显著优于克唑替尼的疗效和良好的安全性,使其有望成为ALK阳性NSCLC患者的一线治疗新选择,正大天晴药业集团在创新药物研发领域的持续投入和卓越成果,不仅为患者提供了更多的治疗选择,也为推动国内医药行业的发展做出了重要贡献。
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。