时间:2024-08-23 15:01 编辑:全球肿瘤医生网
中国首款KRAS G12C突变靶向药氟泽雷塞片(Fulzerasib、达伯特/Dupert、GFH925)获批上市,已上市和在研的KRASG12C靶向药还有哪些
2024年8月21日,癌症患者又迎来了一个好消息!氟泽雷塞片(Fulzerasib,达伯特、Dupert,GFH925)的上市申请,获得了国家药品监督管理局(NMPA)的批准,用于成人至少接受过一种系统性治疗的KRAS-G12C突变型晚期非小细胞肺癌(NSCLC)的治疗。
一直以来,KRAS G12C突变的晚期非小细胞肺癌患者的治疗选择有限,传统化疗的获益甚微。而氟泽雷塞片是一种新型口服强效KRAS G12C抑制剂,旨在通过共价且不可逆地修饰KRAS G12C蛋白的半胱氨酸残基,靶向GTP/GDP交换(通路激活的重要步骤),有效抑制下游信号通路,从而诱导肿瘤细胞凋亡、细胞周期停滞,最终达到抗癌的目的。氟泽雷塞片也成为了中国首个获批上市的KRAS G12C抑制剂,标志着中国正式开启KRAS突变靶向治疗的新时代!具有里程碑式的意义!
▲截图源自NMPA
氟泽雷塞单药或联合西妥昔单抗,暴击KRAS G12C突变非小细胞肺癌
01、氟泽雷塞片单药治疗非小细胞肺癌,疾病控制率高达90.5%
氟泽雷塞片本次新药申请获批,主要是基于Ⅱ期临床研究(NCT05005234)的惊艳数据。本次入组的116例可评估疗效的非小细胞肺癌(NSCLC)患者,在接受氟泽雷塞单药治疗后,客观缓解率(ORR)为49.1%(95%CI:39.7-58.6),疾病控制率(DCR)高达90.5%(95%CI:83.7,95.2),中位无进展生存期(PFS)为9.7个月(95%CI:5.6-11.0)。
02、氟泽雷塞联合西妥昔单抗,疾病控制率可达100%
此外,在2024年ASCO大会上,还公布了氟泽雷塞片联合西妥昔单抗的II期KROCUS临床研究(NCT05756153)数据。本次共入组的27例中位年龄为68岁的NSCLC患者,其中40.7%(11例)的患者存在脑转移。在接受氟泽雷塞片联合西妥昔单抗治疗后,结果显示:
1、疾病控制率(DCR):疾病控制率(DCR)竟然达到了惊人的100%。
2、客观缓解率(ORR):ORR高达80.0%,其中71.4%的脑转移患者获得了部分缓解(PR);8例患者的靶病变肿瘤缩小50%,还有1例患者幸运地获得了完全缓解(CR),详见下图。
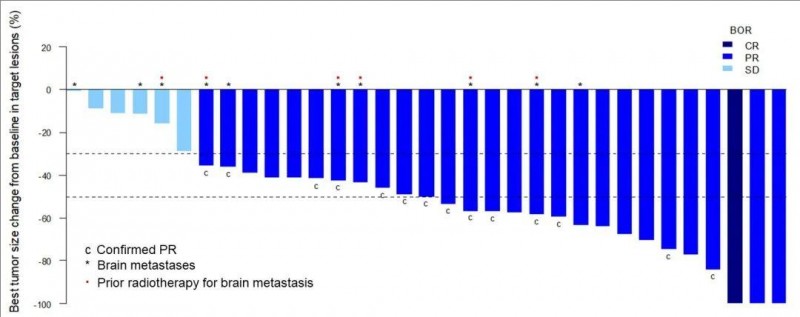
▲图源JCO,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,氟泽雷塞片作为单一疗法或联合西妥昔单抗,在KRASG12C突变的非小细胞肺癌的一线治疗中,展现出显著的疗效和良好的安全性。
KRAS突变难成药的魔咒,终于被打破了
KRAS靶点是一种常见的致癌驱动突变,在多种癌症类型中均有发现,比如近90%的胰腺癌、15%~20%的肺癌、30%~40%结肠癌患者均存在KRAS突变。其中,KRAS G12D被视为KRAS中的钻石亚型,存在于4%的肺腺癌、12%的结直肠癌(CRC)、34%的胰腺导管腺癌(PDAC)、其他实体瘤中。
图1 KRAS突变的类型和比例
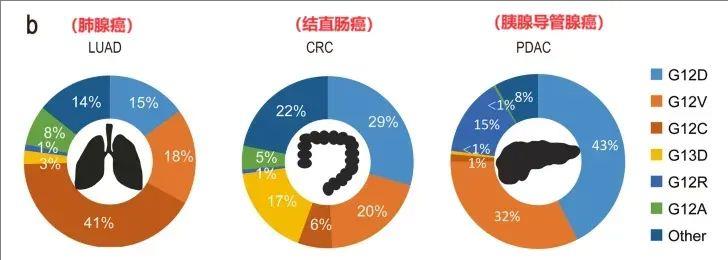
▲图源BMC,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:所选肿瘤类型中,总体发病率最高的前6个KRAS等位基因
KRAS一直被医学界视为不可成药的靶点,也是史上最臭名昭著的靶点,KRAS很少与EGFR、ALK等其他驱动基因突变共存。因此,患者一旦化疗或免疫疗法失败,几乎完全没有可用的靶向治疗方案,疗效低下且预后不良,很多病友会在绝望地等待中遗憾离去。
本次氟泽雷塞的问世,为我国KRAS G12C突变患者带来了一线生机。要知道在此之前,只有2款小分子药物,被美国FDA批准可以针对KRAS G12c突变。KRAS靶点不可成药的魔咒终于被打破了,既往接受化疗或免疫治疗失败的实体瘤患者,也终于迎来了新的曙光!
做了基因检测的癌友,可自行查看检测报告,一旦发现存在KRAS突变,可致电医学部,了解详细的入排标准或进行初步评估。看不懂检测报告的患者,也可联系全球肿瘤医生网医学部,详细解读报告。
此前已获批的两款KRAS靶向药
01、索托拉西布
2021年5月28日,美国食品药品监督管理局(FDA)批准索托拉西布(Sotorasib,Lumakras,AMG510)的上市申请,用于成年KRAS G12C突变的局部晚期/转移性非小细胞肺癌的治疗,这是首款获批治疗KRAS突变的靶向药,成功打破了KRAS不可成药的魔咒!
2023年ASCO大会上公布的Ⅱ期临床研究,共入组30例KRAS G12C突变晚期非小细胞肺癌患者,在接受索托拉西布+卡铂-培美曲塞联合治疗后,客观缓解率(ORR)高达88.9%。在治疗6个月时,总生存(OS)率高达87.0%,中位无进展生存(PFS)率达到61.2%(详见下图)。
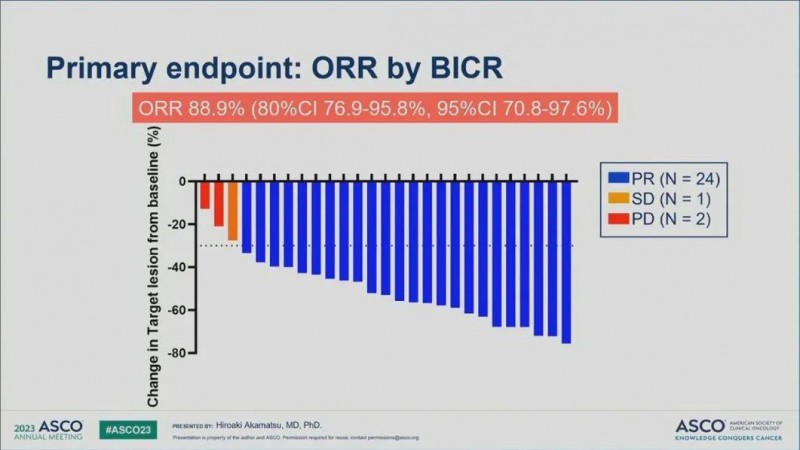
▲图源JCO,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
02、Krazati
2022年12月12日,美国FDA加速批准Krazati(Adagrasib,阿达格拉西布,MRTX849)的上市,用于KRAS G12C突变的局部晚期或转移性非小细胞肺癌(NSCLC)的治疗,这些患者既往接受过1种全身治疗。Krazati是第二款获批上市的KRAS G12C抑制剂!
五款在研KRAS靶向药,剑指肺癌、胰腺癌、结直肠癌等
01、国研IBI351,暴击非小细胞肺癌,疾病控制率高达96.7%
IBI351(GFH925)是我国自主研发的一款新型、强效的KRAS G12C抑制剂,已获得中国国家药品监督管理局的优先审批资格,用于治疗KRAS G12C突变的晚期非小细胞肺癌(NSCLC),且患者既往接受过1线全身治疗。
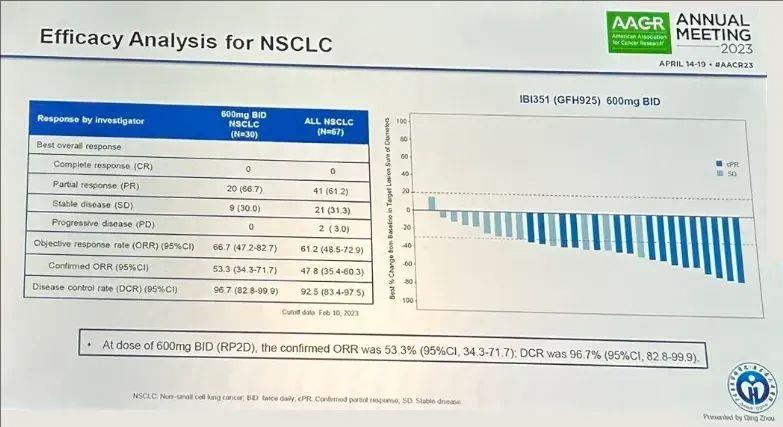
IBI351的1期临床研究结果,已在2023年AACR(美国癌症研究协会)大会上公布。在入组的67例可评估疗效的NSCLC患者中,客观缓解率(ORR)达到61.2%,疾病控制率(DCR)高达92.5%。此外,在30例接受推荐2期剂量(RP2D,即600mg,2次/天)的患者中,ORR达到66.7%,DCR更是高达96.7%(详见下图)!
02、国研D-1553重创结直肠癌,半数患者疾病稳定
D-1553(Garsorasib)是我国自主研发的一款口服高效的KRAS G12C抑制剂,既可有效抑制肿瘤生长,且具有较高的中枢神经系统渗透性。
D-1553的2期临床研究(NCT04585035)结果,已在2023年的欧洲肿瘤内科学会(ESMO)大会上公布。入组的40例结直肠癌患者在接受D-1553+西妥昔单抗双药联合治疗后,疾病控制率(DCR)高达95.0%!总体缓解率(ORR)达45.0%,其中,50%的患者达到疾病稳定(SD)。这也意味着,近一半患者在接受联合治疗后,肿瘤显著缩小30%以上;此外,几乎所有患者在治疗后,病灶出现不同程度的缩小或控制稳定。
03、Divarasib:泛癌种KRAS抑制剂
Divarasib(代号GDC-6036)是一款口服高效的选择性KRAS G12C抑制剂,可用于治疗结直肠癌、非小细胞肺癌、其他实体瘤(如胰腺腺癌、十二指肠腺癌、胆管癌、胃腺癌、阑尾腺癌、肛门腺癌、乳腺癌、子宫内膜鳞状细胞癌)等。
Divarasib的Ⅰ期临床研究,共入组137例患者(包括非小细胞肺癌60例、结直肠癌55例、其他实体瘤22例)。结果显示:
1、在非小细胞肺癌患者(n=58)中:超半数患者在接受GDC-6036治疗后,病灶显著缩小超过30%,甚至有幸运患者病灶完全消失。具体表现为59%的患者达部分缓解(PR),2%的患者获得完全缓解(CR),29%的患者达到病情稳定(SD)。
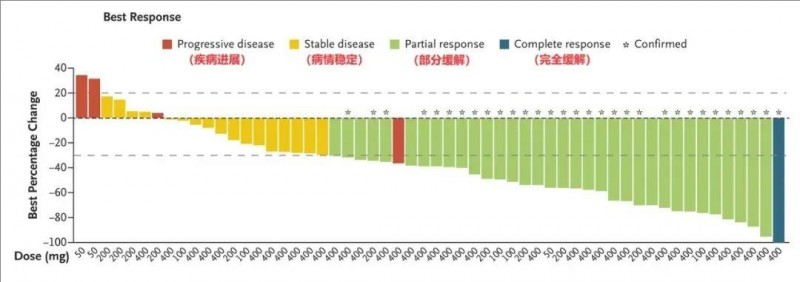
▲图源N Engl J Med,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2、结直肠癌患者(n=55)中:49%的患者达到病情稳定(SD),35%达到部分缓解(PR),2%的患者幸运地获得完全缓解(CR)。
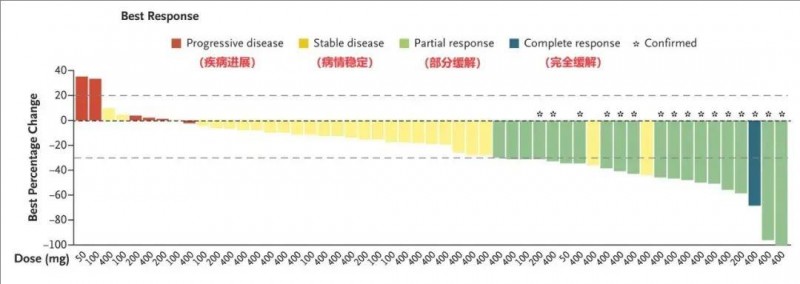
▲图源N Engl J Med,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
3、在其他实体瘤患者(n=22)中:50%的患者达到病情稳定(SD),36%的患者获得部分缓解(PR)。
04、ASP3082注射液:首个针对KRAS G12D突变的降解剂
ASP3082是一种新型小分子蛋白水解KRAS突变体蛋白降解药物,2024年6月11日,中国国家药品监督管理局药品评审中心(NMPA)批准其新药IND申请,用于既往经治局部晚期(不可切除)或转移性恶性KRAS G12D突变实体瘤的治疗。它是全球首个同时也是目前唯一一个进入临床阶段的KRAS G12D蛋白降解药物。
▲截图源自NMPA
05、MRTX1133:或将实现持久肿瘤消除
MRTX1133是一款可逆性、选择性的KRAS G12D抑制剂,可逆转早期肿瘤的生长,重新编程早期及晚期肿瘤的肿瘤微环境,对KRAS G12D的选择性是野生型KRAS的1000倍以上,在结直肠癌、胰腺癌等多款实体瘤的治疗中具有巨大的潜力。据悉,MD安德森癌症研究中心已启动了Ⅰ期临床试验,让我们拭目以待!
小编寄语
我国的新药研发水平,正以前所未有的中国速度,跻身世界前列!本次氟泽雷塞的获批上市,不仅成为了第三款获批上市的KRAS抑制剂,更是成功打破了欧美对KRAS靶向药领域的垄断。而且值得欣慰的是,目前还有多款新药的临床研发正在如火如荼地进行中,剑指肺癌、胰腺癌、结直肠癌等多款令人闻风丧胆的KRAS突变实体瘤,为曾经无药可用的晚期癌症患者带来了一线生机!小编也期望未来能有更多的癌症新药获批上市,并逐步纳入医保范畴,让更多的癌症患者有病可医、有药可用!
好消息是,目前由国内几家知名的癌症医院牵头,我国近期开展了多项KRAS新药的临床试验,并且已经开始正式招募患者。想参加的患者可致电医学部,进行评估申请或了解详细的入排标准。
参考资料
[1]Gregorc V,et al.KROCUS: A phase II study investigating the efficacy and safety of fulzerasib (GFH925) in combination with cetuximab in patients with previously untreated advanced KRAS G12C mutated NSCLC[J]. 2024.
https://ascopubs.org/doi/10.1200/JCO.2024.42.17_suppl.LBA8511
[2]Sakata S,et al.The primary endpoint analysis of SCARLET study: A single-arm, phase II study of sotorasib plus carboplatin-pemetrexed in patients with advanced non-squamous, non-small cell lung cancer with KRAS G12C mutation (WJOG14821L)[J]. 2023.
https://ascopubs.org/doi/10.1200/JCO.2023.41.16_suppl.9006
[3]Sacher A,et al.GO42144 Investigator and Study Group. Single-Agent Divarasib (GDC-6036) in Solid Tumors with a KRAS G12C Mutation. N Engl J Med. 2023 Aug 24;389(8):710-721.
https://www.nejm.org/doi/10.1056/NEJMoa2303810?url_ver=Z39.88-2003rfr_id=ori:rid:crossref.orgrfr_dat=cr_pub%20%200pubmed
[4]https://www.nmpa.gov.cn/zhuanti/cxylqx/cxypxx/20240821175034132.html
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。