时间:2024-11-07 15:14 编辑:全球肿瘤医生网
美国癌症中心重磅:抗癌黑马T细胞治疗33种癌症,生存率提升近2倍
近期美国莫菲特癌症中心进行了一项关于-T细胞在33种癌症类型中重要作用的临床研究。该研究调查了TCGA数据库中的10,131名患者,并用最新版本的TRUST4算法,对来自33种不同癌症类型的11,000个肿瘤样本中的T细胞受体(TCR),进行了全面分析。
该研究结果揭示了T细胞的多样性和预后意义,突出了它们不同癌症组织中的作用和潜在效用,并再次强调了T细胞作为各种癌症预后生物标志物的潜力,为改善免疫疗法和推进癌症研究提供了见解。虽然T细胞仅占T淋巴细胞的0.5%~5%,但它们可以直接消灭肿瘤细胞,而且具有抗癌和抗感染的双重作用,在治疗多款实体瘤(如肝癌、肾癌、肺癌、胰腺癌等)、血液肿瘤(如淋巴瘤、多发性骨髓瘤等)方面具有独特的优势,是当之无愧的抗癌新星!

▲截图源自Cell Rep Med
-T细胞:连接天然免疫与获得性免疫的桥梁,兼具抗肿瘤和抗病毒的双重功效
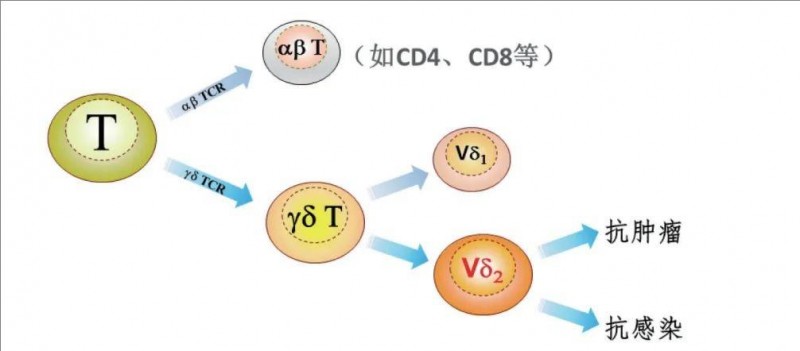
-T细胞是一类罕见的T细胞亚群,又可分为两个主要的亚群,即V1、V2。由于、链结构的不同,各亚群的功能也有差异,如V2细胞亚群就具有抗肿瘤、抑制病菌感染的特性。
-T细胞虽然仅占T淋巴细胞的0.5%~5%,但其功能全面、强大,被视为T细胞中的特种部队。而且无需抗原提呈细胞参与,即可选择性地识别并杀伤肿瘤细胞、被病菌感染的细胞。相比其他免疫细胞,-T细胞最独特的优势在于它既有抗肿瘤的功能,同时又具有抗感染的双重作用,是天然免疫与获得性免疫的桥梁,在免疫功能的响应中发挥着不可或缺的作用。
▲图源cnki,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
-T细胞:全力碾压实体瘤与血液肿瘤等三十多款癌种
-T细胞自发现30余年来,己成为肿瘤细胞疗法中的重要组成部分,也是目前免疫细胞治疗研究领域的一个重要热点。其有效性和安全性已在大量的临床试验中得到验证,已被应用于多种类型的癌症,包括实体瘤(如非小细胞肺癌、肾细胞癌、胃肠道肿瘤、结直肠癌、乳腺癌、卵巢癌、宫颈癌、前列腺癌、黑色素瘤、骨癌)、血液肿瘤(如白血病/淋巴瘤、多发性骨髓瘤)等。
肾癌T细胞比例1%,无复发生存率提高近2倍
肾细胞癌 (RCC) 是一种相对罕见的癌症,近几十年来发病率不断上升。而手术是目前治疗局限性肾细胞癌 (RCC) 的最有效策略之一,在癌症早期阶段预后良好。但部分患者即便接受早期 RCC 根治性切除,也会观察到复发。其中,约 10% 的患者可能会在 5 年内复发,约 2% 的患者则可能在 5 年后复发。为了改善预后,过去几十年来开展了多项辅助全身治疗的研究。而最近研究发现,在肿瘤监视、防御感染中,发挥重要作用的T细胞,与肾细胞癌的预后密切相关。
《泌尿肿瘤学》杂志近期报道的一项临床研究,共入组137例局限性非转移性肾细胞癌(RCC)患者,根据外周血T细胞比例,将其分为两组,即正常组(97例,外周血T细胞比例1%)、低T细胞组(40例,外周血T细胞比例1%)。
经过10年以上的长期随访(随访时间中位数为123个月,范围3个月~12.5年),结果显示:在T细胞低水平组(n=40例)中,有13例(32.5%)患者复发;而在T细胞正常水平组(n=97例)中,仅16例(16.5%)患者复发。显然,外周血中T细胞1%的患者,其无复发生存率(RFS)和总生存期(OS)明显更好(详见下图),预后趋势良好。
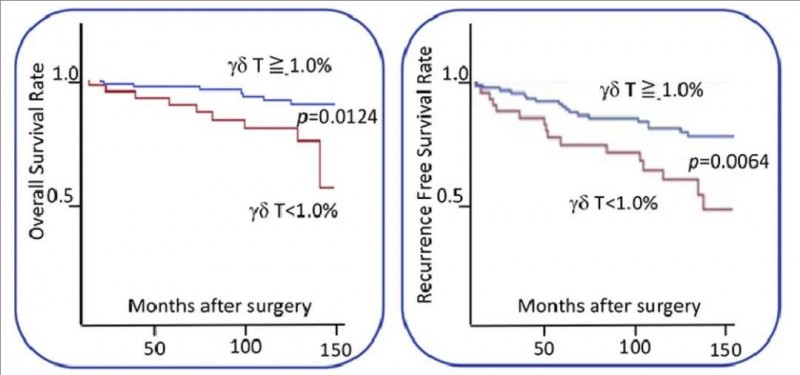
▲图源ScienceDirect,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
T细胞显著延长肝癌/肺癌生存时间,总生存期19个月
V9V2细胞是外周血 T细胞中,占主导地位的亚群。《细胞与分子免疫学》报道了一项应用V9V2 T细胞,治疗晚期癌症的临床研究惊艳数据。本次共入组132例癌症患者中,包括肺癌、肝癌、胰腺癌、乳腺癌、其他类型肿瘤患者。其中,仅18例(8例肝癌、10例肺癌)患者接受了5 次细胞回输,大多患者仅接受了 1-4 次细胞输注。结果显示如下:
1、肺癌组患者:中位总生存期(OS)分别为9.1个月(未接受 T细胞治疗) vs 19.1个月(接受 T细胞治疗)。显然,接受 T细胞治疗的患者总生存时间延长近1年(详见下图)!
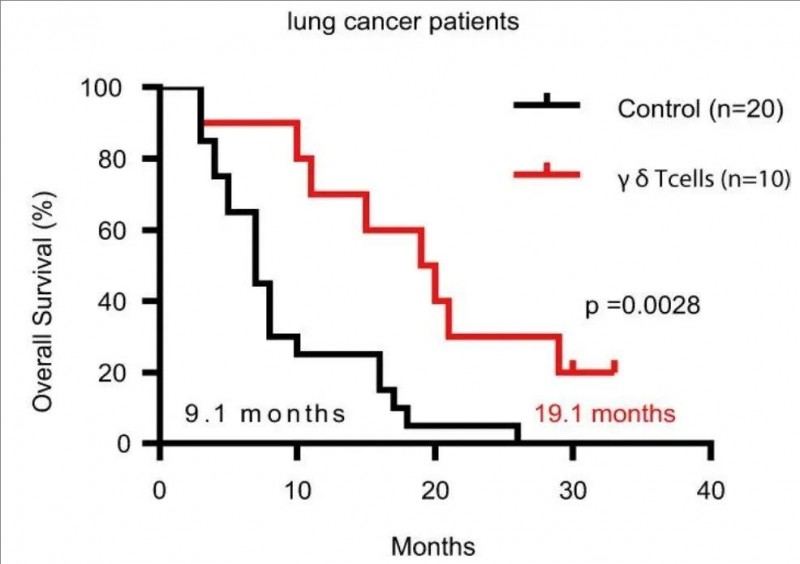
▲图源PMC,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2、肝癌组患者:中位总生存期(OS)分别为8.1个月(未接受 T细胞治疗) vs 23.1个月(接受 T细胞治疗)。显然,接受 T细胞治疗的患者总生存时间提高近3倍(详见下图)!
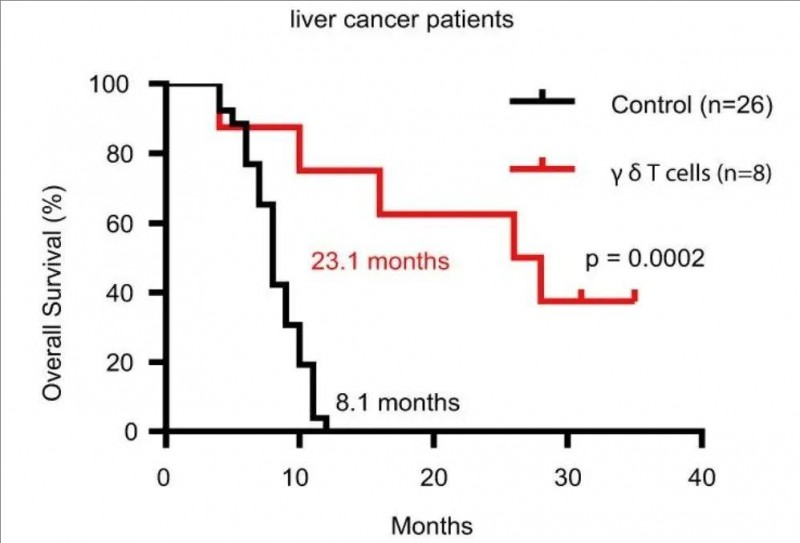
▲图源PMC,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得一提的是,有7名肝癌患者和9名肺癌患者,存活10个月,代表性CT图像也说明了NF细胞的治疗效果(详见下图)。更为惊喜的是,在2020年6月的最新随访中,3名肝癌患者和2名肺癌患者,在接受T细胞治疗后30~35个月仍然存活!
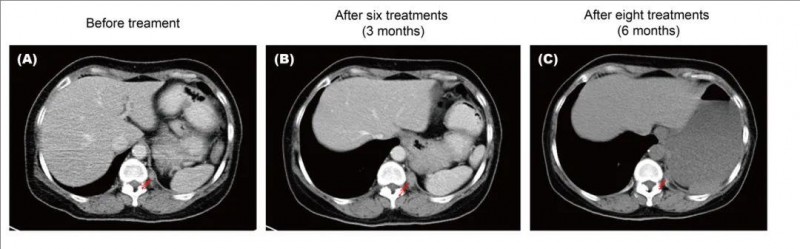
▲图源PMC,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
血液系统恶性肿瘤:T 细胞治疗后达到部分缓解
《血液学(Blood)》杂志,曾报道过一个应用帕米膦酸盐+T 细胞,治疗淋巴系统恶性肿瘤达到部分缓解的案例。
该患者确诊为滤泡中心淋巴瘤,曾接受过高剂量化疗,但效果不理想,病情仍然复发。入组接受帕米膦酸盐和低剂量IL-2,在体内刺激T细胞治疗后,CT检查显示,大多数淋巴结没有明显变化,且皮肤转移及纵隔淋巴结消退(详见下图)。仅有1个淋巴结增大,病理活检显示该淋巴结主要为纤维化,仅剩下少量淋巴瘤细胞。在此之后,肿瘤质量稳步下降,最终经过19个月的治疗,该患者达到部分缓解(PR)(详见下图)。
▼患者治疗前后,CT图像对比
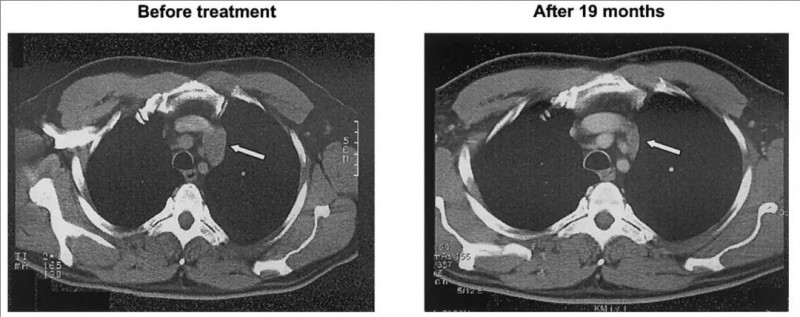
▲图源Blood,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:CT扫描提示,患者皮肤转移及纵隔淋巴结消退(箭头)。
其他癌种
除了上面提到的几款癌症外,T细胞还可用于治疗以下癌种(详见下表),鉴于篇幅限制,无法一一展开叙述,想了解T细胞疗法更多讯息的患者,可将治疗经历、近期病理检查结果等,提交至医学部,详细评估病情。
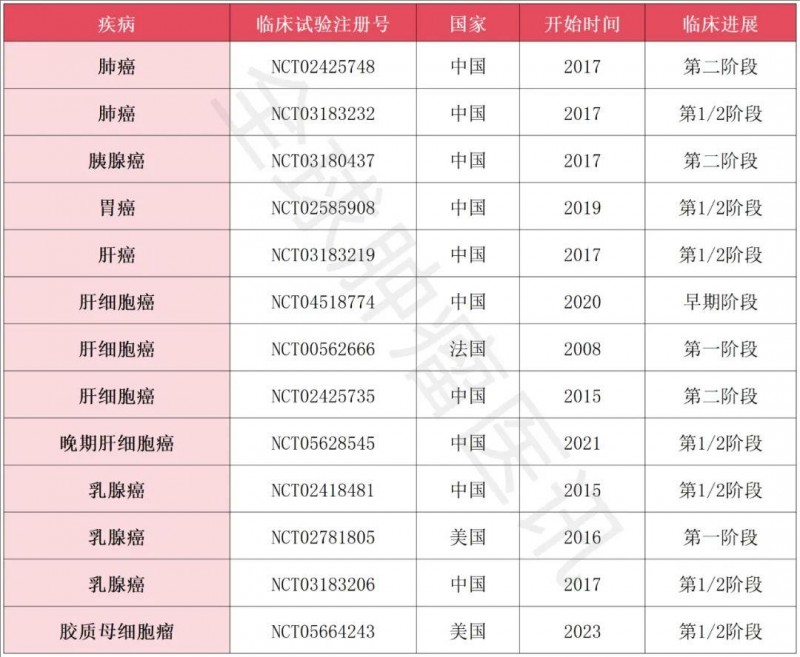
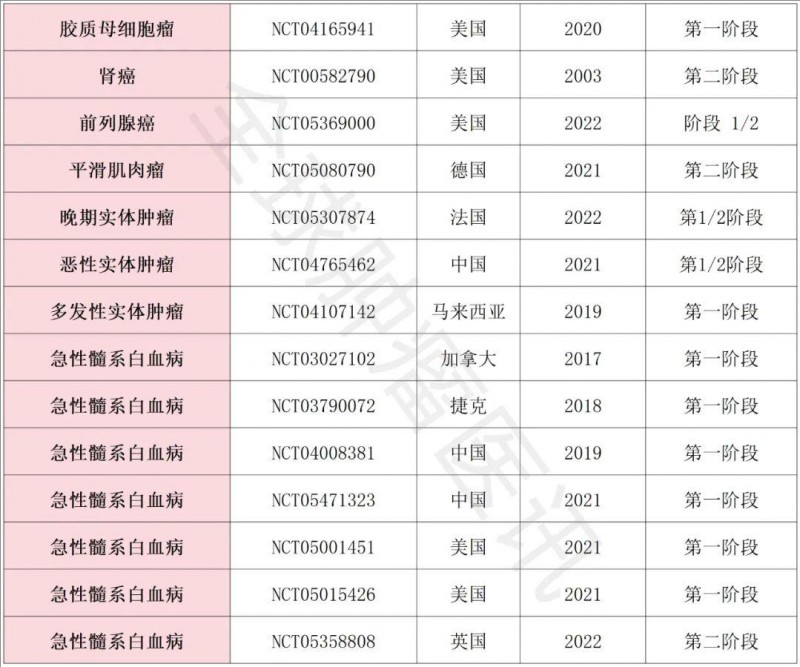

▲数据源自Chinese Medical Journal,全球肿瘤医生网医学部整理汇总
小编寄语
近年研究发现,T细胞具有独特的肿瘤抗原识别能力、强大的肿瘤杀伤活性,而且可与手术、化疗、靶向药等传统抗癌手段联合,改善患者的预后、延长生存时间,从而成为免疫细胞治疗中的黑马,具有广阔的应用潜力!
值得一提的是,目前我国有多个针对T细胞治疗不同癌种的临床研究正在进行中,对现有治疗方案不满意,或想寻求T细胞等国内外新型抗癌疗法帮助的患者,可将出院小结、治疗经历、近期病理及影像学检查报告等,提交至医学部,进行初步评估或申请国内外抗癌专家会诊。
参考资料
[1]Yu X,et al.Pan-cancer TCR analysis uncovers clonotype diversity and prognostic potential. Cell Rep Med. 2024 Oct 15;5(10):101764.
https://www.cell.com/cell-reports-medicine/fulltext/S2666-3791(24)00494-4?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS2666379124004944%3Fshowall%3Dtrue
[2]Si-Yi T,et al.Recent progress on human T cells based tumor immunotherapy[J].Chinese Bulletin of Life Sciences, 2017.
http://en.cnki.com.cn/Article_en/CJFDTotal-SMKX201709006.htm
[3]Kobayashi H,et al.A retrospective cohort study of the impact of peripheral blood gamma- delta T cells to prognosis of nonlinkstatic renal cell cancer after curative resection. Urol Oncol. 2023 Dec;41(12):488.e1-488.e9.
https://www.sciencedirect.com/science/article/abs/pii/S1078143923003356?via%3Dihub
[4]Xu Y,et al.Allogeneic V9V2 T-cell immunotherapy exhibits promising clinical safety and prolongs the survival of patients with late-stage lung or liver cancer. Cell Mol Immunol. 2021 Feb;18(2):427-439.
https://pmc.ncbi.nlm.nih.gov/articles/PMC8027668/
[5]Wilhelm M,et al. T cells for immune therapy of patients with lymphoid malignancies[J]. Blood, 2003, 102(1): 200-206.
https://ashpublications.org/blood/article/102/1/200/16804/T-cells-for-immune-therapy-of-patients-with
[6]Zhao Y,et al. T cells: Major advances in basic and clinical research in tumor immunotherapy[J]. Chinese Medical Journal, 2024, 137(01): 21-33.
https://journals.lww.com/cmj/fulltext/2024/01050/___t_cells__major_advances_in_basic_and_clinical.4.aspx
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。