时间:2024-11-12 16:46 编辑:全球肿瘤医生网
全面盘点中美两国11款已上市的CART产品
Aucatzyl是FDA批准的第5款CD19 CAR-T细胞产品,同时也是全球第12款获批的CAR-T产品!在此之前已有11款CAR-T疗法相继获批(包括美国6款,中国5款)。
美国已获批上市的六大CAR-T产品
1、Kymriah
药物名称:Kymriah(Tisa-cel)
研发公司:诺华制药
上市时间:2017年8月30日
药物介绍:
Kymriah是全球首个获FDA批准上市的CAR-T细胞产品,用于复发或难治性(R/R)弥漫大B细胞淋巴瘤(B-ALL)的治疗,完全缓解(CR)率超过60%!同时也是美国首个获批的基因疗法,自此开启了CAR-T疗法治疗癌症的新时代!
2、Yescarta
药物名称::Yescarta(Axi-cel)
上市时间:2017年10月18日
药物介绍:
Yescarta是一款针对CD19的转基因自体CAR-T细胞疗法,用于复发或难治性(R/R)弥漫大B细胞淋巴瘤/滤泡细胞淋巴瘤的治疗,中位总生存期(OS)长达25.8个月。
3、Tecartus
药物名称:Tecartus(KTE-X19)
上市时间:2020年7月24日
药物介绍:
TECARTUS是一款靶向CD19的CAR-T细胞疗法,主要用于治疗复发或难治性套细胞淋巴瘤的治疗。TECARTUS的2期ZUMA-3临床数据显示,完全缓解(CR)率高达56%。
4、Breyanzi
药物名称:Breyanzi(利基迈仑赛,liso-cel)
研发公司:百时美施贵宝公司
上市时间:2024年3月15日
药物介绍:
Breyanzi是一款靶向CD19的自体CAR-T细胞疗法,先后多次获美国FDA批准,分别用于治疗成人复发或难治性(R/R)慢性淋巴细胞白血病(CLL)、小淋巴细胞淋巴瘤(SLL)(2024年3月15日)、复发或难治性套细胞淋巴瘤(MCL)(2024年5月30日)。
5、Abecma
药物名称:Abecma(ide-cel)
研发公司:百时美施贵宝/蓝鸟生物公司
上市时间:2024年4月4日
药物介绍:
Abecma是全球首个抗BCMA CAR-T细胞疗法,用于复发/难治性多发性骨髓瘤、既往接受过2种治疗的复发或难治性多发性骨髓瘤的治疗。3期临床试验(KarMMa-3)结果显示,Abecma将多发性骨髓瘤的疾病进展或死亡风险足足降低了51%!
6、西达基奥仑赛
药物名称:西达基奥仑赛(Carvykti,cilta-cel)
研发公司:传奇生物。
上市时间:2024年4月5日。
药物介绍:
西达基奥仑赛是一种靶向BCMA的CAR-T细胞疗法,它也是首个获得FDA批准的国产CAR-T疗法,用于成人复发或难治性多发性骨髓瘤(R/R MM)的治疗!3期CARTITUDE-4临床研究数据显示,完全缓解率(CR)高达73.1%!
中国已获批上市的五大CAR-T产品
1、阿基仑赛注射液药
物名称:阿基仑赛注射液(奕凯达)
研发公司:复星凯特
上市时间:2021年6月1日。
药物介绍:
阿基仑赛注射液是中国首个以药品途径,获批上市的CAR-T细胞治疗产品,针对CD19靶点,用于成人复发或难治性大B细胞淋巴瘤(r/r LBCL)的治疗。
2、瑞基奥仑赛注射液
药物名称:瑞基奥仑赛注射液(relma-cel,倍诺达)
研发公司:药明巨诺
上市时间:2021年9月1日
药物介绍:
瑞基奥仑赛注射液是一款CD19 CAR-T细胞治疗产品,2021年9月1日获批上市,用于既往经二线系统性治疗失败的复发或难治的大B细胞淋巴瘤的治疗,它是我国获批的第2款CAR-T产品!
2020年美国血液学会(ASH)年会上,公布了瑞基奥仑赛的惊艳数据,结果显示:中位总生存(OS)率高达90.8%,治疗3个月客观缓解率(ORR)达到58.6%,治疗6个月无进展生存(PFS)率高达54.2%。
▼55例可评估疗效的患者,根据SPD的肿瘤体积相对于基线的变化
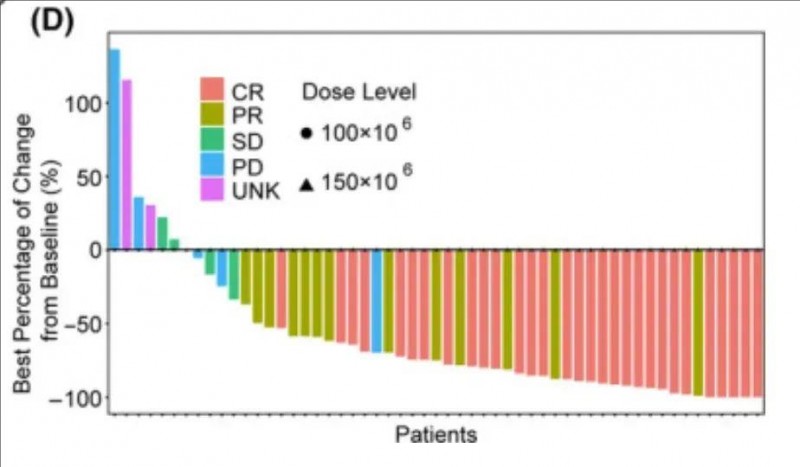
▲图源Cancer Med,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
3、纳基奥仑赛注射液
药物名称:纳基奥仑赛注射液(CNCT19细胞注射液,源瑞达)
研发公司:合源生物
上市时间:2023年11月8日
药物介绍:
纳基奥仑赛注射液是中国首个治疗白血病的CAR-T细胞产品,针对CD19靶点,于2023年11月8日获批,用于成人复发或难治性B细胞急性淋巴细胞白血病(r/r B-ALL)的治疗。
第64届美国血液学年会(ASH)上,公布的关键性临床数据显示:治疗3个月内,总体缓解率(ORR)高达82.1%;完全缓解(CR)率高达66.7%,CR/CRi患者的MRD(微小残留病灶)阴性率高达100%!治疗3个月时,CR率达51.3%,ORR达64.1%(详见下表)。

4、伊基奥仑赛
药物名称:伊基奥仑赛注射液(Equecabtagene Autoleucel Injection,福可苏)
研发公司:驯鹿生物、信达生物
上市时间:2023年6月30日
药物介绍:
伊基奥仑赛注射液是全球首款全人源BCMA靶向CAR-T疗法!同时也是中国首个获批的BCMA CAR-T疗法!国家药品监督管理局(NMPA)于2023年6月30日批准其上市,用于复发/难治性多发性骨髓瘤(R/R MM)的治疗。伊基奥仑赛1/2期临床研究数据显示,总缓解率(ORR)竟高达96.0%!
5、泽沃基奥仑赛
药物名称:泽沃基奥仑赛(赛恺泽,zevor-cel)
研发公司:科济药业
上市时间:2024年3月1日
药物介绍:
泽沃基奥仑赛是一款自体BCMA CAR-T细胞产品,它是我国第二款靶向BCMA的CAR-T细胞产品,同时也是我国第五款获批上市的CAR-T产品!用于治疗复发或难治性多发性骨髓瘤。
Ⅰ/Ⅱ期(LUMMICAR STUDY 1)临床研究结果显示,总缓解率(ORR)达100%(14/14),其中78.6%的患者获得了完全缓解(CR)或严格完全缓解(sCR)!中位无进展生存期(PFS)长达25.0个月。所有患者(n=14)的中位缓解持续时间长达24.1个月(2年),sCR/CR患者的中位缓解持续时间为26.0个月(详见下图)。

▲图源Cancer Med,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
CAR-T疗法研发领域快速崛起,群雄逐鹿
除了上文提到的已获得中美批准上市的12款CAR-T产品(包括刚刚获批上市的用于治疗复发或难治性B细胞前体急性淋巴细胞白血病的Aucatzyl)外,越来越多的临床试验,均已验证CAR-T细胞疗法在治疗恶性肿瘤,尤其是血液系统恶性肿瘤中的疗效!全球在研的3000多种细胞疗法药物中,CAR-T疗法就占据了半壁江山。
CAR-T疗法开启复发或难治性套细胞淋巴瘤治疗新纪元,总缓解率高达89%
套细胞淋巴瘤(MCL)是一种独特、罕见的B细胞非霍奇金淋巴瘤亚型,其临床病程具有异质性,既包括可能多年不需要治疗的惰性类型,还包括尽管采用强化治疗方案但预后不良的高度侵袭性类型。特别是对于具有高风险疾病特征的MCL患者,预后通常较差。而近年来,复发或难治性套细胞淋巴瘤(R/R MCL)的治疗领域发生了重大变化,逐渐从传统化疗和免疫疗法,转向靶向治疗和以CAR-T为代表的细胞疗法。
一项针对984例接受CAR-T治疗的复发或难治性套细胞淋巴瘤(R/R MCL)患者的荟萃分析显示,总缓解率(ORR)高达89%(95%CI:87%91%),完全缓解(CR)率高达74%。总生存率(OS)分别为80%(6个月) vs 69%(12个月)。无进展生存(PFS)率为68%(6个月) vs 51%(12个月)。
转移性结直肠癌GCC19CAR-T治疗后,中位总生存期超22个月
结直肠癌(CRC)是全球第二大癌症死亡原因,大约一半的患者最终会发展为晚期、无法治愈的CRC,且治疗效果的进步有限。近期研究发现,自体CAR-T细胞产品在接受过大量治疗的转移性结直肠癌(mCRC)患者中,表现出抗肿瘤活性。
《美国医学会肿瘤学杂志》报道了一项应用GCC19 CAR-T治疗转移性结直肠癌的1期临床研究,共入组15例转移性结直肠癌(mCRC)患者,中位年龄(范围)为44岁(33-61岁),入组接受GCC19(鸟苷酸环化酶-C)CAR-T治疗。
结果显示:客观缓解率(ORR)达到40%。其中40%(6例)的患者达到部分缓解(PR),另外5例患者的最佳反应为病情稳定(SD),因此总体临床受益率为73%。
截至数据数据统计时止,中位总生存期(OS)长达22.8个月(95%CI,13.4-26.1);接受较高剂量治疗的患者的中位无进展生存期(PFS)显著高于接受较低剂量治疗的患者,中位PFS分别为6.0个月(高剂量组) vs 1.9个月(低剂量组)(详见下图)。
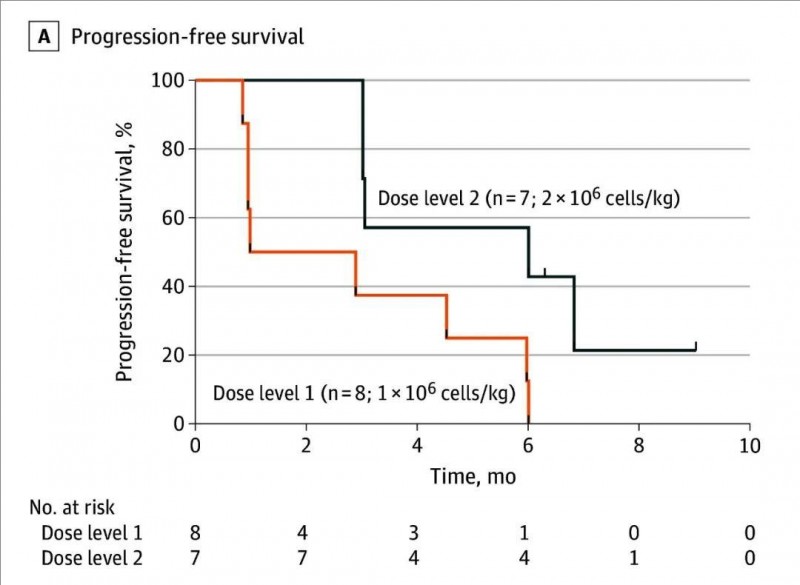
▲图源JAMA Oncol,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得一提的是,一位接受GCC19 CAR-T治疗后,达到部分缓解(PR)的患者(患者1),在治疗前、治疗1个月、3个月和6个月时的影像学变化,影像学显示治疗后该患者转移性病灶明显改善(详见下图)。
▼患者1接受CAR-T细胞输注前后的影像学变化
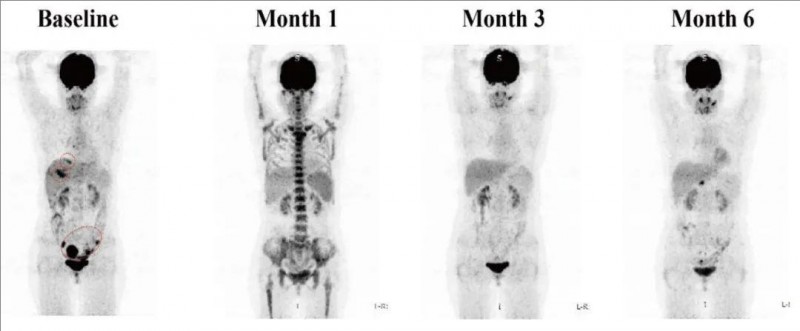
▲图源JAMA Oncol,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
十二年前,急性淋巴细胞白血病患儿Emily Whitehead在接受CAR-T细胞疗法治疗后,获得临床治愈,并存活至今的案例让CAR-T这款新型免疫细胞疗法一战成名!如今,我们很欣慰的看到,全球已有12款CAR-T产品获批上市,为无数饱受疾病折磨的血液肿瘤患者带来了新的希望与曙光!
更加欣慰的是,各国都纷纷加入CAR-T研发大军中,截至2023年,全球免疫细胞的临床研究项目已超2000项(ClinicalTrials.gov),其中仅CAR-T疗法一项就占据了近半数以上,这也彰显了CAR-T疗法在抗癌领域的广阔应用前景。而且近年来,研究人员不断更新CAR-T的新技术、发现新的靶点,尝试将其用于实体瘤治疗领域,并取得了不俗的疗效。全球肿瘤医学部小编希望CAR-T疗法可以早日突破价格和实体瘤治疗瓶颈,让越来越多的癌症患者获益,助其降低复发风险、实现长期带瘤生存的美好愿景!
如果您也想寻求CAR-T、TCR-T、TIL、CAR-NK等国内外新型抗癌疗法的帮助,可将近期影像学检查结果、近期病理报告、治疗经历等资料,提交至医学部,详细评估病情,或申请国内外抗癌专家会诊。
参考资料
[1]Roddie C,et al.Obecabtagene autoleucel (obe-cel, AUTO1) for relapsed/refractory adult B-cell acute lymphoblastic leukemia (R/R B-ALL): pooled analysis of the ongoing FELIX phase Ib/II study[J]. Blood, 2023, 142: 222.
https://ash.confex.com/ash/2023/webprogram/Paper179454.html
[2]Ying Z,et al.Relmacabtagene autoleucel (relma-cel) CD19 CAR-T therapy for adults with heavily pretreated relapsed/refractory large B-cell lymphoma in China. Cancer Med. 2021 Feb;10(3):999-1011.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7897944/
[3]Fu C,et al. Three-Year Follow-up on Efficacy and Safety Results from Phase 1 Lummicar Study 1 of Zevorcabtagene Autoleucel in Chinese Patients with Relapsed or Refractory Multiple Myeloma[J]. Blood,2023, 142(Supplement 1): 4845-4845.
https://www.sciencedirect.com/science/article/abs/pii/S0006497123114467
[4]Fu C,et al. Three-Year Follow-up on Efficacy and Safety Results from Phase 1 Lummicar Study 1 of Zevorcabtagene Autoleucel in Chinese Patients with Relapsed or Refractory Multiple Myeloma[J]. Blood,2023, 142(Supplement 1): 4845-4845.
https://www.sciencedirect.com/science/article/abs/pii/S0006497123114467
[5]Chen N,et al.Chimeric Antigen Receptor T Cells Targeting CD19 and GCC in linkstatic Colorectal Cancer: A Nonrandomized Clinical Trial. JAMA Oncol. 2024 Sep 19:e243891.
https://pmc.ncbi.nlm.nih.gov/articles/PMC11413756/
[6]https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-obecabtagene-autoleucel-adults-relapsed-or-refractory-b-cell-precursor-acute
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。