时间:2024-11-27 15:07 编辑:全球肿瘤医生网
CAR-T细胞疗法治疗致命脑瘤,帮助患者生存期延长3倍,肿瘤缩小最高可达100%
一直以来,血液系统恶性肿瘤都是CAR-T细胞疗法的主战场,国内外有多款产品相继获批,而且临床疗效有目共睹。但实体瘤因其异质性、复杂的微环境等顽固壁垒,让诸多前沿免疫疗法折戟沉沙。但值得欣慰的是,近年来随着研究的不断深入,CAR-T细胞疗法在治疗实体瘤领域也取得了突破性进展。
近期,全球知名期刊《Nature》发表了一项振奋人心的临床研究结果,改造后的CAR-T细胞疗法在治疗一种致死率近乎100%的致命脑癌方面,取得了显著疗效,其中一例患者更是奇迹般获得完全缓解,且近3年未复发!这一惊艳的研究成果,再次验证了CAR-T疗法在治疗恶性实体瘤方面的巨大应用潜力,为现有治疗方案无效的肿瘤患者带来了新的曙光与选择!
致命脑瘤GD2-CAR T治疗后,生存期从11个月,飙升3倍,肿瘤缩小率可达100%
H3K27M突变的弥漫性中线神经胶质瘤(DMG)起源于神经系统的中线结构,主要发生在儿童和年轻人中。脑桥弥漫性中线神经胶质瘤(也称为弥漫性内在性脑桥神经胶质瘤,DIPG)是儿童脑癌最常见的死亡原因,姑息放疗是标准治疗方法,即便配合化疗、靶向疗法等,预后仍然不理想,患者中位总生存期仅为11个月,5年总生存率低于1%。而脑干外(包括脊髓)DMG患者的中位总生存期为13个月。因此,迫切需要新的治疗方法,改善患者的预后。近期研究发现,GD2-CAR-T细胞疗法在治疗神经母细胞瘤的试验中,取得了令人惊叹的疗效。
全球知名期刊《Nature》报道了自体GD2-CART细胞,治疗DIPG和脊髓弥漫性中线胶质瘤(sDMG)的首次人体/首次儿童I期临床试验(NCT04196413)的惊艳数据。
本次共入组13例中位年龄为15岁(范围4-30岁)的患者,其中10例为脑桥弥漫性中线神经胶质瘤(即弥漫性内在性脑桥神经胶质瘤,DIPG)、3例脊髓弥漫性中线神经胶质瘤(sDMG)。这些患者均存在H3K27M突变,入组前至少4周完成标准一线放射治疗,未接受皮质类固醇治疗。最终11例患者接受了一次GD2-CART细胞静脉回输治疗,结果显示如下:
1、中位总生存期(OS):所有患者的中位总生存期(OS)为确诊后20.6个月,其中,DIPG(脑桥弥漫性中线神经胶质瘤)患者的中位总生存期为17.6个月,sDMG(脊髓弥漫性中线神经胶质瘤)患者的中位总生存期为31.96个月。
▼患者的生存期
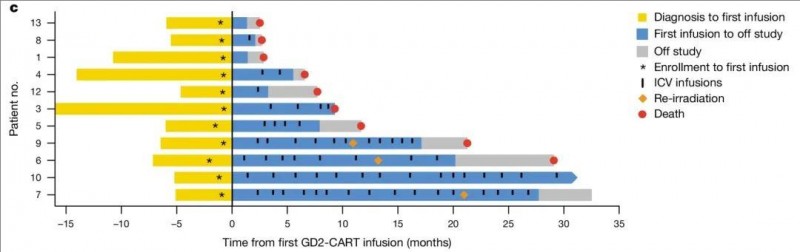
▲图源nature,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:每条柱状图代表从诊断到第一次治疗的时间(黄色)、试验时间(蓝色)
2、肿瘤体积缩小:4例患者的肿瘤体积大幅缩小,缩小幅度分别为52%、54%、91%、100%,另有3例患者肿瘤小范围缩小。
▼第一次GD2-CART治疗前后的肿瘤体积变化
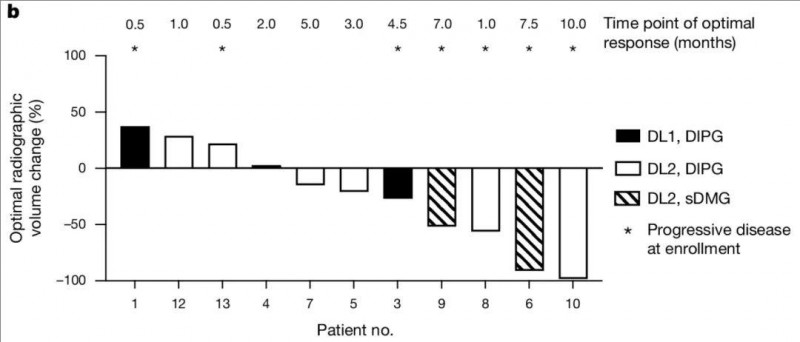
▲图源nature,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:星号(*)表示在第一次GD2-CART细胞输注时,有记录的病情进展的患者
值得一提的是,其中2位脑桥弥漫性中线神经胶质瘤(DIPG)患者(患者007、患者010),在数据截止后,仍然存活,生存时间分别达到33个月、30个月,远超传统治疗11个月的中位总生存期!
010号患者CAR-T治疗后,症状缓解、肿瘤持续缩小,生存时间已达30个月
1、肿瘤持续缩小,完全缓解达30个月:该患者确诊为脑桥弥漫性中线神经胶质瘤(DIPG),在完成前期放疗后,通过影像学检查显示有进展或假进展的可能。在第一次GD2-CART细胞输注后的数月内,肿瘤体积持续缩小至完全反应。这种完全缓解在入组后30个月(数据截止时间)持续,并且仍在继续(详见下图)。
2、症状缓解:该患者在入组时,存在感觉和运动障碍,需要步行辅助(长距离使用轮椅)。在GD2-CART治疗后,不仅经历了影像学上的完全反应,同时伴有显著的临床改善,包括左侧听力改善,半脸、半身和味觉改善、运动协调性改善、步态改善至独立行走的程度。
▼010号患者在基线时(治疗前),首次GD2-CART输注后3、5、16和29个月时,中脑、脑桥和延髓水平的肿瘤T2加权轴向MRI对比
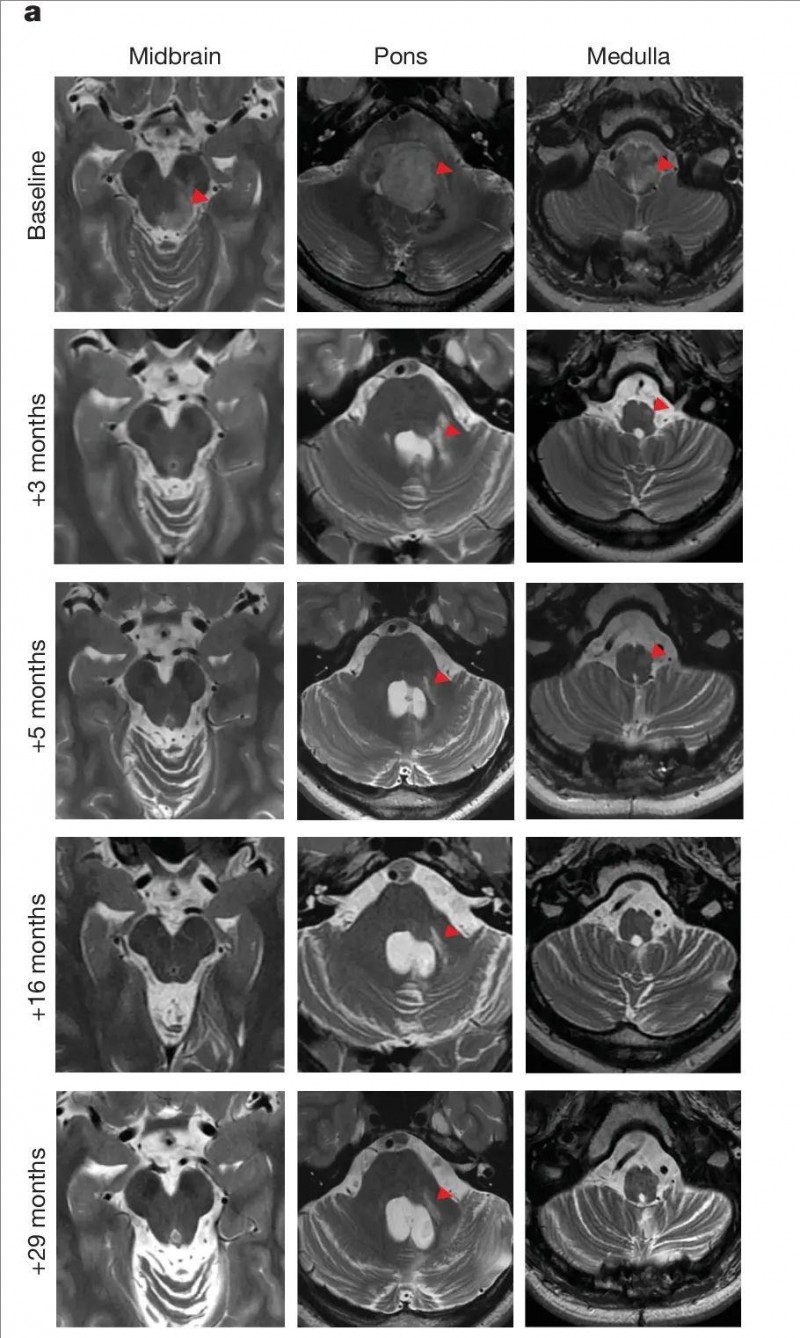
▲图源nature,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:红色箭头表示T2信号异常
①在基线时(治疗前),可见肿瘤累及中脑(左侧右侧)、脑桥和延髓,且肿块遮挡第四脑室;CAR-T治疗3个月后消退。
②治疗3个月时,随着脑干大小恢复正常,脑干周围脑脊液回流明显,大部分脑干的T2信号恢复正常。但T2信号仍异常,可能提示肿瘤仍存在于脑桥活检道区域周围(红色箭头),但5个月后消退。
006号患者CAR-T治疗7个月,肿瘤缩小91%、症状明显改善
1、肿瘤体积明显缩小:该患者确诊为脊髓弥漫性中线神经胶质瘤(sDMG),在第一次治疗时处于明显的临床和放射学肿瘤进展中,而在第一次GD2-CART细胞输注后7个月内,肿瘤体积显著缩小91%(详见下图)。
▼006号患者在基线时(治疗前)、首次输注GD2-CART后2、6和9个月时的脊髓弥漫性中线神经胶质瘤的MRI图像对比
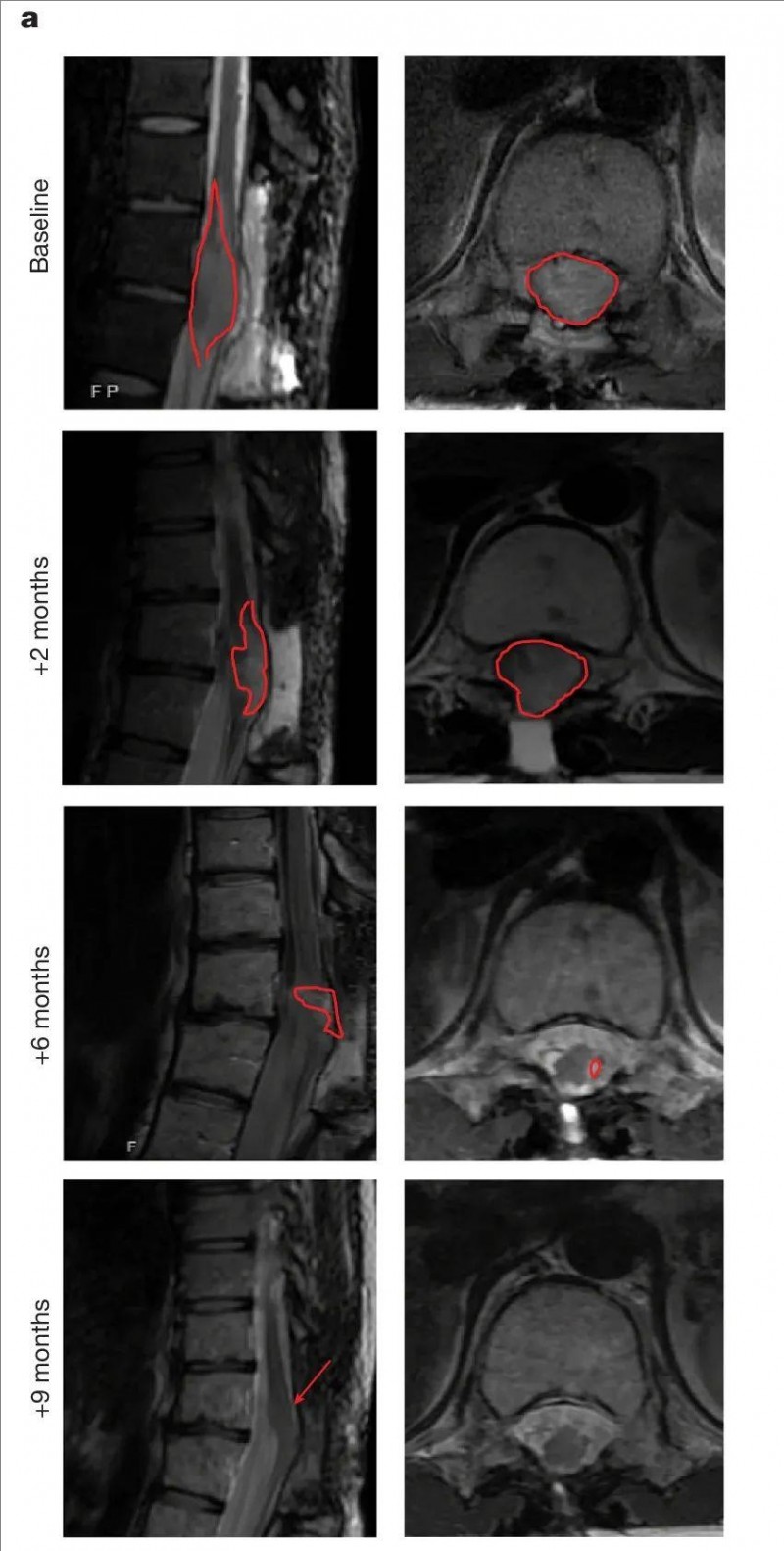
▲图源nature,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:红色轮廓表示T2信号异常(提示肿瘤)
①在基线时(治疗前),以T11/12脊髓水平为中心的肿瘤弥漫性地影响脊髓,并扩张脊髓以填满整个椎管,脊髓周围未观察到脑脊液(CSF)。
②GD2-CART治疗后,脊髓肿瘤浸润逐渐改善,直至恢复正常大小且T2信号异常最小(红色箭头)。
2、症状显著改善:在第一次输注GD2-CART之前,该患者患有严重的截瘫、神经性疼痛、肠道和膀胱功能障碍。在输注GD2-CART后,且总体反应最好的时候(肿瘤缩小90%以上),患者疼痛明显改善,下肢功能改善,能够用拐杖行走。
中国患者如何寻求CAR-T疗法帮助
目前有多款CAR-T临床研究正在进行中,主要针对下列靶点及癌种:
①GPC3:用于治疗肝癌;
②EGFRvII:用于治疗头颈部肿瘤、神经胶质瘤等;
③PSMA:用于治疗前列腺癌等;
④Claudin18.2:用于治疗胃癌、胰腺癌等;
⑤GUCY2C:用于治疗结直肠癌;
⑥CEA:用于治疗肺癌、结肠癌、胃癌、乳腺癌、胰腺癌等;
⑦MUC-1:用于治疗肝癌、肺癌、胃癌、胰腺癌等;
⑧间皮素(mesothelin):用于治疗间皮瘤、结肠癌、肺癌、卵巢癌、胰腺癌等;
⑨B7-H3:用于治疗神经母细胞瘤、髓母细胞瘤、横纹肌肉瘤、肾母细胞瘤、尤文肉瘤、特别难以治疗的脑干肿瘤(DIPG)。
做过基因检测的患者,可立即查看检测报告,一旦发现存在上述癌种及相应靶点,可将治疗经历、近期病理及基因检测结果,提交至医学部,进行初步评估或了解详细的入排标准。
参考资料
[1]Monje M,et al.Intravenous and intracranial GD2-CAR T cells for H3K27M+ diffuse midline gliomas[J]. Nature, 2024: 1-8.
https://www.nature.com/articles/s41586-024-08171-9
[2]Zhao Z,et al.An armored GPC3-directed CAR-T for refractory or relapsed hepatocellular carcinoma in China: A phase I trial[J]. 2021.
https://meetings.asco.org/abstracts-presentations/199036/poster
[3]https://ir.allogene.com/news-releases/news-release-details/allogene-therapeutics-presents-interim-phase-1-data-allo-316
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。