时间:2024-12-18 14:43 编辑:全球肿瘤医生网
Claudin18.2,胃癌患者必须知道的明星靶点,Claudin18.2(CLDN18.2)靶向药胃癌抗癌路上的精准武器
胃癌(GC)在全球范围内属于第五大常见癌症类型。伴随分子靶向治疗的兴起,针对HER2靶点的曲妥珠单抗,已然成为HER2阳性胃癌的一线治疗用药。另外,针对血管内皮生长因子受体2的单克隆抗体雷莫芦单抗与紫杉醇联合运用,在二线治疗过程中也展现出了对患者生存状况的改善作用。而用于PD-1的纳武单抗(Nivolumab)则获批应用于三线或后续治疗阶段。不过,对于那些不可切除或者已处于转移性晚期的胃癌患者而言,其预后状况依旧难以令人满意。所以,积极开发新型治疗策略已然成为当下极为紧迫的任务。
除了上面提到的靶点和药物外,一个暴露于胃和胃食管结合部腺癌(GEJ)表面,极具治疗潜力的靶点CLDN18.2,也是胃癌患者务必知晓的。特别是随着全球首款 CLDN18.2 靶向药佐贝妥昔单抗(Zolbetuximab)震撼上市之后,更是使得CLDN18.2这一明星靶点再度引起广泛关注。
胃癌患者必须知道的明星靶点CLDN18.2
CLDN是体内上皮细胞粘附所必需的,对屏障功能至关重要,它是一个至少包含27种跨膜蛋白的家族,在信号转导和肿瘤发生中发挥作用,如肿瘤细胞的生长和存活、肿瘤增殖、转移和肿瘤组织中的癌症干细胞等。其中,1998年发现的CLDN18.2蛋白是在正常和恶性胃粘膜上皮细胞中,表达的紧密连接蛋白中的一种分子。
在正常胃黏膜上皮中,CLDN18.2(Claudin18.2)表达严格局限于除胃干细胞区以外的胃黏膜分化上皮细胞。但在胃癌、胃食管结合部腺癌(GEJ)、食管癌、结肠癌、胰腺癌、乳腺癌、肝癌、卵巢癌、非小细胞肺癌等某些恶性肿瘤中,它也普遍表达。
值得注意的是,在正常组织中,组织粘附复合物内的CLDN18.2表位完全无法接近;然而,在恶性转化时,细胞粘附被破坏,CLDN18.2表位暴露在胃和GEJ(G/GEJ)腺癌细胞表面,使其成为一个有希望的靶点,尤其在消化系统肿瘤中(如胃癌、胃食管结合部癌、食管癌和胰腺癌)异常过表达,比如,在胃癌或胃食管结合部癌中,在高达70%-80%的胃癌或胃食管结合部癌患者,以及60%的胰腺癌患者可检测到Claudin 18.2的高度表达。因此确诊胃癌、食管癌、胰腺癌等消化道肿瘤后,除了检测HER2、PD-L、MET等靶点外,还要再检测下是否存在Claudin 18.2。
▼晚期胃癌CLDN18.2靶向治疗的发展
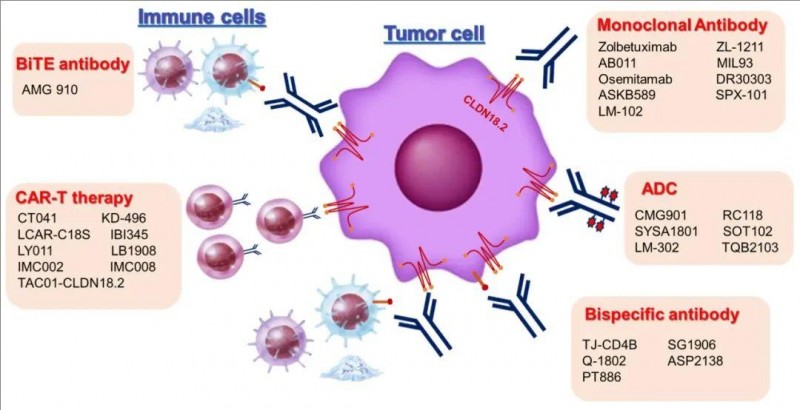
▲图源MDPI,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
CLDN18.2抗癌新药及新技术
截至 2023 年 8 月,Clinical Trials.gov (NCT) 网站上,共有 43 项正在进行的针对CLDN18.2的临床试验,包括CAR-T疗法、ADC(抗体-药物偶联物)药物、双特异性抗体 (BsAbs)等。
全球首款CLDN18.2靶向疗法-佐贝妥昔单抗震撼上市,显著延长生存期!
2024年3月26日,佐贝妥昔单抗(Zolbetuximab,VYLOY,代号IMAB362)获日本厚生劳动省(MHLW)批准上市,用于CLDN18.2阳性、不可切除、晚期或复发性胃癌的治疗,它是首个同时也是目前唯一获得世界监管机构批准的CLDN18.2靶向疗法。
全球知名期刊《自然医学》报道了佐贝妥昔单抗的Ⅲ期GLOW临床研究(NCT03653507)的惊艳数据,本次共入组507例既往未接受过治疗的CLDN18.2阳性、HER2阴性的局部晚期或转移性胃癌或胃食管交界癌患者,将其分为两组,即佐贝妥昔单抗组(接受佐贝妥昔单抗+CAPOX治疗)、安慰剂组(接受安慰剂+CAPOX治疗)。结果显示如下:
1、中位无进展生存期(PFS):接受佐贝妥昔单抗治疗的患者,PFS显著延长,中位PFS分别为8.21个月(佐贝妥昔单抗组) vs 6.80个月(安慰剂组)(详见下图)。12个月PFS率分别为35%(佐贝妥昔单抗组) vs 19%(安慰剂组);24个月PFS率分别为14%(佐贝妥昔单抗组) vs 7%(安慰剂组)。
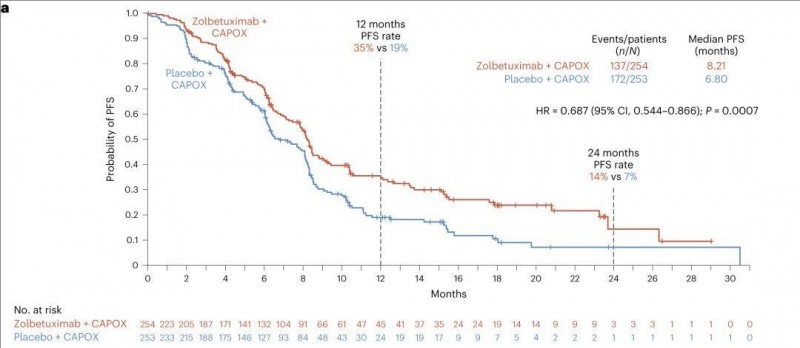
▲图源nature,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2、中位总生存期(OS):佐贝妥昔单抗组患者的OS在统计学上显著延长,中位OS分别为14.39个月(佐贝妥昔单抗组) vs 12.16个月(安慰剂组)(详见下图)。12个月的OS率分别为58%(佐贝妥昔单抗组) vs 51%(安慰剂组);24个月的OS率分别为29%(佐贝妥昔单抗组) vs 17%(安慰剂组)。
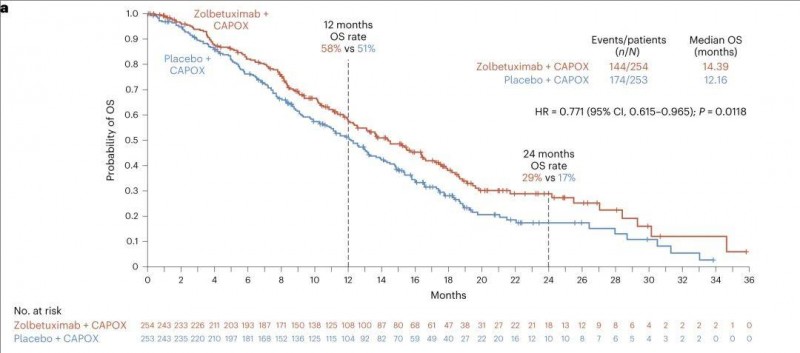
▲图源nature,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:做了基因检测的病友可拿出检测报告看看,一旦存在Claudin18.2突变,可马上联系医学部,初步评估是否有机会接受国内新药治疗,看不懂报告的病友也可致电全球肿瘤医生网医学部,详细解读报告。
北肿公布CT041第1阶段试验最终结果:疾病控制率高达96.1%
CT041(satri-cel)是一款靶向Claudin18.2(CLDN18.2)的自体CAR-T细胞(嵌合抗原受体T细胞)。近日,北肿研发团队公布了关于CT041-CG4006的1期临床试验(NCT03874897)的最终结果。
本次共入组98例CLDN18.2阳性晚期胃肠道肿瘤患者,入组接受不同剂量的CT041(即CAR-T细胞)回输治疗,治疗剂量分别为2.5108(89例患者)、3.75108(6例患者)、5.0108(3例患者),中位随访时间为32.4个月。
结果显示:在全部98例患者中,91.8%(90例)基线有靶病灶,治疗后70例患者出现不同程度的肿瘤缩小,总缓解率为38.8%,疾病控制率(DCR)高达91.8%,中位总生存期(OS)长达8.8个月(95% CI:7.1,10.2),中位无进展生存期(PFS)为4.4个月(95% CI:3.7,6.6)。
▼CT041治疗后疗效的泳道图
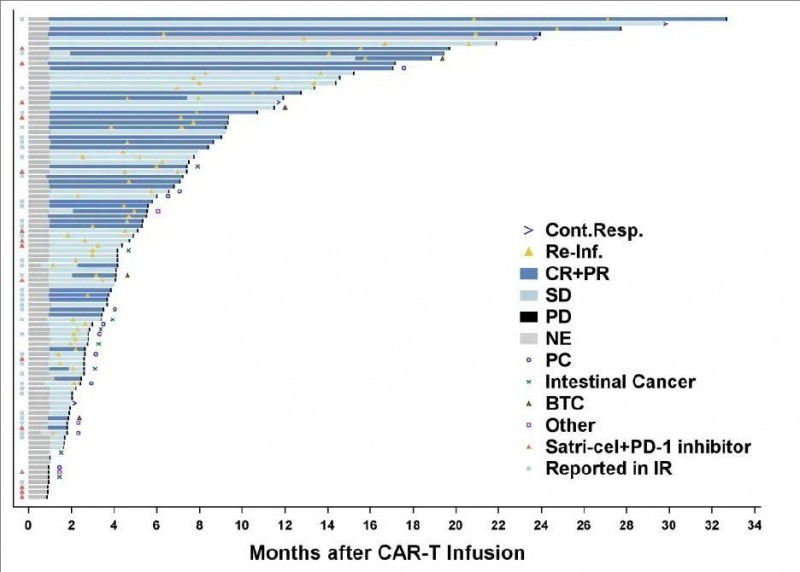
▲图源nature medicine,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
更多Claudin18.2的新药/新疗法正在招募中
相信看了上面的数据,Claudin18.2阳性癌症患者,一定重燃了希望!好消息是,除了上面提到的佐贝妥昔单抗、CT041(CAR-T)外,目前国内外还有多款针对Claudin18.2的新药获新疗法正在招募胃癌、胰腺癌等多款实体肿瘤患者,包括但不限于:
1、TQB2103
TQB2103是中国生物制药自主研发的针对CLDN18.2的ADC药物。TQB2103与表面表达CLDN18.2的肿瘤细胞结合后,被内化并运输到溶酶体,在溶酶体中释放细胞毒性有效载荷,从而通过脱氧核糖核酸(DNA)损伤选择性杀死肿瘤细胞。通过旁观者效应,它可以杀死相邻的阴性肿瘤细胞。目前正在进行一项I期临床试验,评估TQB2103注射液对晚期癌症患者的耐受性、安全性和有效性(NCT05867563)。
2、ASKB589
ASKB589是一种人源化抗CLDN18.2IgG1mAb,具有高亲和力和增强的ADCC。已公布ASKB589对晚期实体瘤患者的I/II期剂量递增和扩展研究的初步结果(NCT04632108)。本研究评估了ASKB589单药治疗(A部分)和与化疗联合治疗(B部分)的最大耐受剂量(MTD)、安全性和耐受性、PK、PD和疗效。在A部分9名可评估患者(10mg/kgASKB589)中,5名患者(45%)的肿瘤缩小,而2名患者获得部分缓解(PR)。此外,6名患者病情稳定(SD),疾病控制率(DCR)高达89%。在B部分12名可评估患者(6mg/kgASKB589)中,所有患者的肿瘤均缩小,9名患者获得PR,客观缓解率(ORR)高达75%,DCR疾病控制率(DCR)更是达到100%。综上,ASKB589显示出高达20mg/kg剂量的可控安全性和良好的抗肿瘤活性。
3、IMC002
IMC002是一种基于抗CLDN18.2VHH抗体的自体CAR-T细胞疗法,具有高特异性,与CLDN18.2无交叉反应。一项1期、开放标签、多中心、剂量递增研究旨在评估IMC002对CLDN18.2阳性胃肠道肿瘤患者的安全性、可行性和初步疗效,包括但不限于晚期胃癌、食管胃交界处腺癌和晚期胰腺癌(NCT05946226)。约9-18名CLDN18.2阳性晚期胃肠道肿瘤患者将依次纳入三个剂量递增队列,以评估自体IMC002治疗的安全性和可行性。患者入组后将接受白细胞分离术和IMC002产品制备。如果病情迅速进展,患者可按照研究者的决定接受桥接疗法。在接受环磷酰胺、氟达拉滨和白蛋白紫杉醇淋巴细胞清除治疗后,患者将被分配到三个剂量递增组接受CAR-T细胞治疗。
4、SYSA1801
SYSA1801是一种靶向CLDN18.2的ADC,可递送微管抑制剂MMAE。临床前研究表明,SYSA1801在表达CLDN18.2的胃癌、胰腺癌和肺癌的多种细胞系和PDX中表现出显著的体内和体外抗肿瘤活性。I期试验纳入的33名耐药复发性实体瘤患者中,26名(78.8%)患有胃癌。在第I部分中,患者接受了高达3mg/kg的SYSA1801。在17名可评估的胃癌患者中,ORR为47.1%(8名患者为PR),DCR为64.7%(3名患者为SD)。SYSA1801的最佳剂量正在探索中(NCT05009966)。
5、LM-302
LM-302(TPX-4589)是一种针对CLDN18.2而开发的新型ADC,由重组人源化抗CLDN18.2IgG1mAb(LM-102)与细胞毒性有效载荷MMAE偶联而成。根据临床前数据,在高表达和低表达的胃和胰腺CLDN18.2肿瘤模型中,LM-302体外有效抑制肿瘤细胞增殖,体内减少肿瘤生长。此外,在GC肿瘤模型中,与佐贝妥昔单抗相比,LM-302表现出更好的内化和疗效。目前,针对CLDN18.2阳性晚期实体瘤患者的LM-302的I期研究正在评估中(NCT05001516)。此外,目前正在进行一项I/II期、开放标签、多中心研究,旨在评估LM-302联合特瑞普利单抗(抗PD-1抗体)对晚期实体瘤患者的安全性和耐受性(NCT05188664)。
小编寄语
CLDN18.2作为胃癌治疗领域的新兴靶点,为胃癌患者带来了新的希望。随着研究的不断深入和临床实践的逐步积累,基于CLDN18.2的治疗药物和方案将不断优化和完善。未来,我们有望看到更多高效、低毒的CLDN18.2靶向治疗药物问世,并且在联合治疗模式的探索上取得更大突破,从而显著提高胃癌患者的治疗效果,改善患者的生存质量和预后,为胃癌的攻克迈出坚实的一步。
胃癌患者及其家属应该与医生积极沟通,了解CLDN18.2靶点相关知识以及其在治疗方案中的应用可能性,共同参与到胃癌的精准治疗决策过程中,以争取更好的治疗效果和生存机会。已经做了基因检测的病友,可将病历提交至医学部,初步评估获得用药方案及临床试验推荐。
参考资料
[1]Inamoto R,et al.Claudin18. 2 in advanced gastric cancer[J]. Cancers, 2023, 15(24): 5742.
https://www.mdpi.com/2072-6694/15/24/5742
[2]Shah M A,et al.Zolbetuximab plus CAPOX in CLDN18. 2-positive gastric or gastroesophageal junction adenocarcinoma: the randomized, phase 3 GLOW trial[J]. Nature medicine, 2023, 29(8): 2133-2141.
https://www.nature.com/articles/s41591-023-02465-7
[3]Qi C,et al.Claudin18. 2-specific CAR T cells in gastrointestinal cancers: phase 1 trial final results[J].Nature Medicine, 2024:1-11.
https://www.nature.com/articles/s41591-024-03037-z
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。