全球肿瘤医生网提醒患者:国内细胞免疫治疗技术,包括cart细胞,树突细胞疫苗,NK细胞,TILs细胞,TCR t细胞治疗,癌症疫苗等技术均处于临床试验阶段,未获准在医院正式使用。国内患者可以参加正规临床试验,在医生的监管下使用,全球肿瘤医生网不推荐患者贸然尝试任何医疗机构和研发机构的收费治疗。
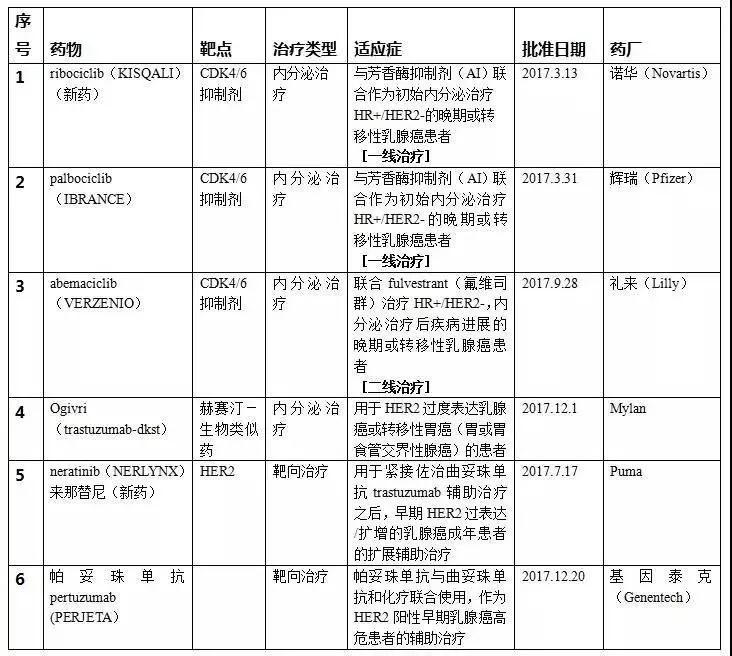
2017年在乳腺癌领域获批了4个新适应症和2个新药。其中靶向药物2个,包括帕妥珠单抗和一个新药来那替尼;内分泌治疗药物4个,包括3个CDK4/6抑制剂:Kisqali、IBRANCE、VERZENIO和1个赫赛汀生物类似药-Ogivri。
2017年美国FDA审批的
乳腺癌新适应症和新药:
对于激素受体阳性的乳腺癌患者,主要治疗手段是内分泌治疗。但CDK4/6的异常激活会使内分泌治疗发生耐药,如能阻断CDK4/6的激活,可有效控制肿瘤生长。2017年,美国FDA在乳腺癌领域批准了4个CDK4/6抑制剂用内分泌药物,分别如下:
1Ribociclib(瑞博西尼)
17年3月,美国FDA批准了诺华公司新药ribociclib(Kisqali,以前称为LEE011)与芳香酶抑制剂联合作为初始内分泌类治疗方案,用于绝经后激素受体阳性、人类表皮生长因子受体-2阴性(HR+/HER2-)的晚期或转移性乳腺癌女性患者。
这是继辉瑞Ibrance之后第二个CDK4/6抑制剂,作为乳腺癌领域的新药,它的获批是基于一项III期临床研究的数据MONALEESA-2,该研究共纳入了668例绝经后HR+/HER2-晚期乳腺癌初治患者,结果显示,相对于单用芳香酶抑制剂来曲唑治疗,ribociclib与来曲唑联用可将疾病进展或死亡(PFS)风险降低了44%。联合用药组的中位PFS为25.3个月,而来曲唑单药组的中位PFS为16个月。可见ribociclib与来曲唑联合显示了卓越的疗效,目前总生存数据尚未成熟。
2Palbociclib(帕博西尼)
与ribociclib一同获批的一线药物是palbociclib(IBRANCE, Pfizer),作为全球首个CDK4/6激酶抑制剂在2015年就已通过一项II期研究的无进展生存期(PFS)数据获得了FDA的加速批准,2017年又加入一个新的乳腺癌适应症,与芳香酶抑制剂(来曲唑)联用,作为内分泌基础的一线治疗,用于绝经后HR+/HER2-的晚期乳腺癌患者。
该批准基于一项国际、随机、双盲、安慰剂对照试验PALOMA-2,比较帕博替尼联合来曲唑与来曲唑加安慰剂治疗晚期乳腺癌患者,主要终点是无进展生存期。
试验招募666名绝经后晚期乳腺癌患者,ER+、HER2-、未经激素治疗。随机分组(治疗组2:对照组1),每天125mg帕博替尼或者安慰剂,治疗21天,停止7天;每天曲唑2.5mg,患者在疾病恶化或无法忍受的毒性时停止治疗。病人在治疗初期检查血细胞,每两周查一次。实验组与对照组相比较:无进展生存期(PFS)24.8 vs 14.5个月,生存期延长达将近两倍。
3Abemaciclib
第三个内分泌药是abemaciclib(VERZENIO),2017年9月,获得美国FDA批准上市,abemaciclib获批用于用于激素受体阳性HR+、HER2阴性的晚期或复发乳腺癌治疗。
abemaciclib作为CDK4/6抑制剂,在细胞中,CDK4/6能促进肿瘤的生长,而CDK4/6抑制剂可选择性地抑制细胞周期蛋白依赖性激酶4和6(CDK4/6),恢复细胞周期控制,阻断肿瘤细胞增殖,因此,abemaciclib有望能控制乳腺癌的进展,改善病情。
此项获批是依据一项III期临床试验的结果,入组经内分泌治疗后疾病进展的HR+/HER2-晚期乳腺癌患者669例,随机分到abemaciclib+氟维司群联合组和氟维司群单药组。结果显示,联合组的中位PFS为16.4个月;而单药组患者中位PFS为9.3个月。abemaciclib使患者的PFS有显著改善,因此获批作为经内分泌治疗后进展HR+/HER2-乳腺癌二线治疗。
4Trastuzumab-dkst(曲妥珠单抗生物类似物)
第四个是trastuzumab-dkst(Ogivri),这是第一个由FDA批准的赫赛汀生物类似药,也是美国第二次批准的用于治疗癌症的仿制药。2017年12月,trastuzumab-dkst获得了FDA的优先审批资格,被批准用于治疗赫赛汀标签中的所有适应症,用于HER2过表达的乳腺癌患者,凭借的是一项III期临床研究非常卓越的疗效数据。生物类似药是一种生物制品,除了满足法律规定的其他标准之外,还要有可靠的临床试验数据证明其与已被FDA批准的生物药具有高度相似性,且在安全性,纯度和效力方面没有临床意义上的差异。
对于trastuzumab-dkstogivri预期的副作用研究人员也做出了介绍,其中包括头痛、腹泻、恶心、寒战、发热、感染、充血性心力衰竭、失眠、咳嗽和皮疹。除此之外,trastuzumab-dkst的标签还包括一个黑框警告,那就是增加患心脏病的危险,严重过敏样反应、肺损伤,以及损害发育中的胎儿。
分割线
另外两个在获批的是乳腺癌治疗的两个靶向药,分别如下:
1Neratinib(来那替尼)
第一个是新药来那替尼neratinib(NERLYNX), 2017年7月,美国FDA批准了neratinib用于早期HER2阳性乳腺癌的延长辅助治疗,这些成年患者群体先前已接受过含trastuzumab单抗的治疗方案。
这是基于一项多中心、随机、双盲、安慰剂对照试验ExteNET(NCT00878709),在2840例早期HER2阳性、在近两年内完成了trastuzumab治疗的乳腺癌患者随机试验中,研究人员评估了neratinib的安全性和有效性。该研究还测量了试验开始之后癌症复发或死亡发生的时间。经过两年疗程后,经neratinib治疗的患者中94.2%没有发生癌症复发或死亡,而接受安慰剂的患者为91.9%。
neratinib是一种口服的、有效的不可逆的酪氨酸激酶抑制剂,像拉帕替尼和阿伐他汀一样,用于延长辅助治疗早期HER2过表达/扩增乳腺癌的成年患者,通过阻止通过表皮生长因子受体(EGFR),HER1,HER2和HER4信号通路转导,达到抗癌的目的。FDA批准该药后,为早期、HER2阳性、标准曲妥珠辅助治疗后、存在高危风险的乳腺癌患者的强化治疗提供了新的选择。
2Pertuzumab(帕妥珠单抗)
第二个获批的靶向药物是pertuzumab(PERJETA),获批的适应症为与曲妥珠单抗和化疗联合使用,作为HER2阳性的早期高危乳腺癌患者的辅助治疗。
基于一个多中心、随机、双盲、安慰剂对照III期试验APHINITY,评估了作为辅助治疗,与赫赛汀联合化疗相比,pertuzumab联合赫赛汀和化疗的疗效和安全性,共参考了4804例HER2阳性早期乳腺癌患者的治疗情况。
对于HER2阳性可手术乳腺癌患者,在化疗联合赫赛汀基础上加用pertuzumab可显著提高无浸润性疾病生存率。pertuzumab组患者的腹泻发生率高于安慰剂组。
在意向治疗人群(ITT)中,接受Perjeta / 赫赛汀 / 化疗的患者其3年无侵入性疾病生存率(iDFS)为94.1%,优于使用安慰剂 / 赫赛汀 / 化疗的对照组(93.2%),达到了该研究的主要临床目的。
日前,Pertuzumab(帕妥珠单抗)在中国的上市申请获得CDE承办受理,国内患者有望不用出国就能买到。其他药物在美国虽然已经上市,国内上市估计还早得很。
更多药品信息请登录
声明:
本公众号内容仅作交流参考,不作为诊断及医疗依据,仅依照本文而做出的行为造成的一切后果,由行为人自行承担责任。专业医学问题请咨询专业人士或专业医疗机构。
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。
帮助广大患者在抗癌之路上少走/不走弯路
最终成功战胜病魔!
靶向治疗|最新资讯|临床试验|靶向药物|
基因检测|免疫治疗资讯|定期专家科普讲座