时间:2018-10-26 15:23 编辑:全球肿瘤医生网
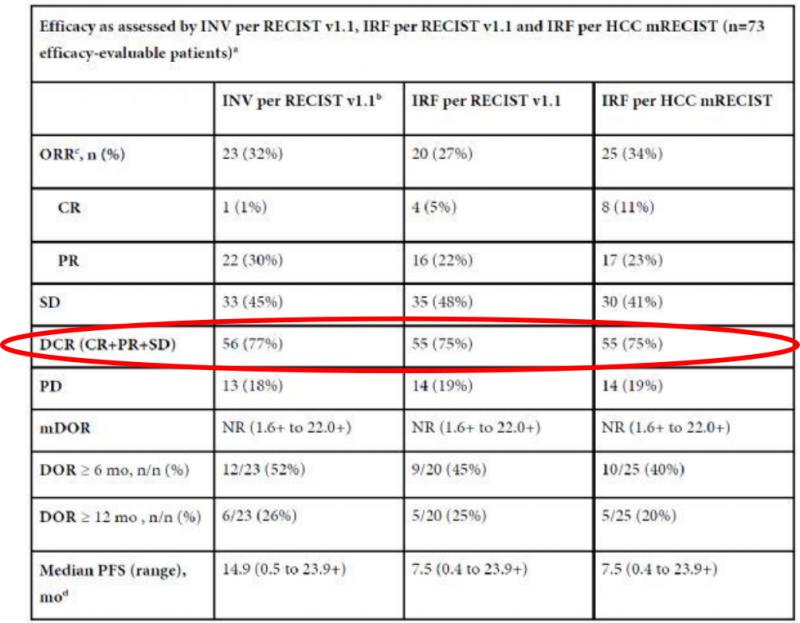
疗效评估群体包括所有接受联合治疗并被随访至少16周的患者,中位生存随访时间为7个月。完全缓解率(CR)方面,INV根据RECIST v1.1评估的CR为1例(1%),IRF根据RECIST v1.1评估的CR为4例(5%),IRF根据HCC mRECIST评估的CR为8例(11%)。疾病控制率(DCR,即经历缓解或稳定病情)在所有形式的评估中都保持一致,INV根据RECIST v1.1评估的DCR为77%(n=56/73),IRF根据RECIST v1.1评估以及根据HCC mRECIST评估的DCR均为75%(55/73)。中位缓解持续时间(DOR)和总生存期(OS)还没有达到。
在安全性可评估群体(n=103)中,27%的患者(n=28/103)经历3-4级治疗相关不良事件,2%(n=2/103)经历治疗相关的5级不良事件。除了现有单个药物的安全概况之外,没有发现与联合治疗相关的新的安全信号。
今年7月,美国FDA根据正在进行的Ib期研究的总体数据,已授予Tecentriq+Avastin组合疗法一线治疗晚期或转移性肝细胞癌的突破性药物资格(BTD)。这也是罗氏产品组合中迄今为止被授予的第23个BTD,也是Tecentriq迄今被授予的第3个BTD。
http://news.bioon.com/article/6728996.html
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。