2020年,结直肠癌患者又有哪些新的治疗方案可用?有哪些新的药物即将上市,全球肿瘤医生网医学部整理了的信息,供大家参考。
晚期结直肠癌的整体药物治疗策略
一线治疗方案
晚期结直肠癌的治疗方案包括化疗,靶向和免疫治疗。在进行治疗前,一定要进行基因检测,因为医生会基于原发病灶的位置,基因突变及生物标记物检测情况制定治疗方案。
结直肠癌的化学通常选择多药联合,医生根据患者实际情况进行组合搭配,常用的初始标准组合方案如下:
1、FOLFOX(LV / 5-氟尿嘧啶+ 奥沙利铂)
2、CAPEOX(希罗达(卡培他滨)+ 奥沙利铂)
3、FOLFIRI(LV / 5-氟尿嘧啶+伊立替康)
4、FOLFOXIRI(LV / 5-氟尿嘧啶+伊利替康+ 奥沙利铂)
这些治疗方案通常与Avastin®(贝伐单抗)联合使用,可改善生存率,尤其是对于左侧结肠癌的治疗。
说到这里,也需要提醒大家,结直肠癌肿瘤病灶发生在左侧(降结肠、乙状结肠、直肠)与右侧(升结肠、横结肠、盲肠)的治疗方案和预后是完全不同的,切忌混为一谈。在确诊后,大家一定要找的专家制定治疗方案。
左半RAS/RAF野生型患者具体方案如下,I级推荐方案(首选):FOLFOX/FOLFIRI±西妥昔单抗II级推荐方案:FOLFOX/CapeOx/FOLFIRI±贝伐单抗;FOLFOXIRI±贝伐单抗
右半RAS/RAF野生型患者具体方案如下,I级推荐方案(首选):FOLFOX/CapeOx/FOLFIRI±贝伐单抗;FOLFOXIRI±贝伐单抗。与FOLFIRI + Avastin相比,FOLFOXIRI + Avastin的5年总生存率估计提高了一倍。II级推荐方案:FOLFOX/FOLFIRI±西妥昔单抗。
二线治疗治疗方案
在一线时,我们就会选用贝伐单抗联合化疗,如果治疗无效的话,可以换一个化疗方案,继续选用贝伐单抗。当然,也可以在换一个化疗方案的同时换另一个靶向药,换成阿柏西普,或者是雷莫芦单抗。
三线及后线治疗方案
结直肠癌一线和二线的药物方案选择,通常是一些比较标准的化疗药和靶向药。从三线治疗开始是属于后线治疗。后线治疗方案可以使用一些刚刚问世的口服化疗药,包括TAS-102,还有S-1(替吉奥)、瑞格菲尼或者一些免疫疗法,如派姆单抗(MSI-H)。
结直肠癌精准靶向治疗方案及进展
2017版的结直肠癌治疗指南中,关于基因检测的推荐只涉及到KRAS,NRAS,dMMR和MSI-H,而在2020年的治疗指南中,新纳入了BRAF,HER2,NTRK等新的靶点,通过基因检测,了解结直肠癌的更多分子信息,能够帮助我们找到更多的用药方案。患者平均存活率在3年以上,这是精准医学带来的巨大的进步。
确诊后,医生必须尽早对每位患有转移性结直肠癌(mCRC)的患者进行基因检测,以确定疾病中的亚组,因为这些信息可能会预测治疗预后,比如HER2扩增提示抗EGFR治疗耐药。以下基因是必须进行检测的!
MSI,BRAF,KRAS,NRAS,RAS,HER2,NTRK。
FDA批准的靶向治疗药物
VEGF:贝伐珠单抗、阿帕西普
VEGFR:雷莫芦单抗、瑞戈菲尼、呋喹替尼
EGFR:西妥昔单抗,帕尼单抗
PD-1/PDL-1:帕姆单抗、纳武单抗
CTLA-4:易普利单抗
BRAF:维莫非尼,康奈非尼
NTRK:拉罗替尼,恩曲替尼
| 研发公司 | 药物靶点 | 药物名称 | 上市时间 | 中国是否上市 | 医保报销 |
| 百时美施贵宝 | HER1(EGFR/ERBB1) | Cetuximab(西妥昔单抗)Erbitux | 2006 | 是 | 是 |
| 武田/安进 | HER1(EGFR/ERBB1) | Panitumumab(帕尼单抗) | 2005 | 否 | 否 |
| 拜耳 | KIT/PDGFRβ/RAF/RET | Regorafenib(瑞戈非尼) | 2012 | 是 | 是 |
| 和记黄埔 | VEGFR1/2/3 | Fruquinitinib(呋喹替尼) | 2018 | 否 | 否 |
| 赛诺菲 | VEGFA/B | Ziv-aflibercept(阿柏西普) | 2012 | 否 | 否 |
| 礼来 | VEGFR2 | Ramucizumab(雷莫芦单抗) | 2014 | 否 | 否 |
| 基因泰克 | VEGFR | Bevacizumab(贝伐珠单抗) | 2004 | 是 | 是 |
| 百时美施贵宝 | BRAF V600E | Encorafenib(康奈非尼) | 2020 | 否 | 否 |
| 百时美施贵宝 | PD-1 | Nivolumab(纳武单抗) | 2015 | 是 | 否 |
| 百时美施贵宝 | CTLA-4 | Ipilimumab(伊匹单抗) | 2011 | 否 | 否 |
EGFR靶向药
表皮生长因子受体 (EGFR)发生在约10%的结肠癌中,最常见于左侧。
西妥昔单抗和帕尼单抗分别于2004年和2006年被FDA正式批准用于治疗晚期结直肠癌。
西妥昔单抗(爱必妥 Cetuximab Erbitux )
2004年,FDA日前批准西妥昔单抗(cetuximab,Erbitux)治疗有远处转移的晚期结直肠癌。成为第一种获得FDA批准治疗结直肠癌的单克隆抗体,其治疗适应证为:①依立替康(irinotecan) 单独用药或依立替康与其他化疗药物联用效果不佳的晚期结直肠癌患者,可联合应用西妥昔单抗和依立替康;②不能耐受依立替康的患者可单独应用西妥昔单抗。
2019年10月,国家药品监督管理局正式批准西妥昔单抗用于RAS基因野生型转移性结直肠癌一线治疗,并且纳入医保(2290元/支)
帕尼单抗(panitumumab Vectibix)
2006年9月美国FDA批准帕尼单抗用于治疗表皮生长因子受体(EGFR)表达阳性且在含氟尿嘧啶,奥沙利铂和伊立替康的化疗方案后病情仍然进展或转移的结直肠癌.
2014年5 月 26 日,美国 FDA 批准帕尼单抗(Panitumumab)可与 FOLFOX 方案(氟尿嘧啶,亚叶酸钙,奥沙利铂)联用于 Kras野生型mCRC 患者的一线治疗。
BRAF V600E靶向药
7-10% 的结肠癌患者携带 BRAF V600E 突变。BRAF V600E 突变属于 BRAF 激活突变,是 BRAF 比例最高的变异形式。具有独特的临床特征:
主要出现在右半结肠;
dMMR比例高,达到20%;
BRAF V600E突变预后差;
不典型的转移模式;
具有BRAF突变基因的患者通常预后较差,一些新的精确抗癌药物已被证明可以使生存时间加倍。
研究发现 FOLFOXIRI+贝伐珠单抗可能成为 BRAF 突变患者的 治疗。
2019 V2版NCCN指南推荐BRAF V600E 转移性结直肠癌二线治疗方案:
维罗非尼+伊利替康+西妥昔单抗/帕尼单抗
Dabarafenib+曲美替尼+西妥昔单抗/帕尼单抗
Encorafenib+Cetux/Pan
好消息是,面对如此凶险的BRAF V600E突变转移性结直肠癌,2020年4月8日,辉瑞(Pfizer)公司宣布美国FDA已经批准Braftovi®(encorafenib,康奈非尼)和Erbitux®(cetuximab,西妥昔单抗)联合用药方案(Braftovi二药方案),用于治疗携带BRAF V600E突变的转移性结直肠癌(mCRC)患者。这些患者已经接受过一种或两种前期疗法。此次批准,也使Braftovi二药方案成为FDA批准的针对携带BRAF基因突变mCRC患者的首个靶向疗法。
Kras靶向药
KRAS突变是最致命的癌症生长和发展的初始驱动遗传因子之一。表现出这种突变的患者通常预后较差,并且对护理标准治疗的抵抗力很差。据统计,KRAS基因突变出现在近,30-40%的结肠癌中,至今没有获批的靶向治疗方案。
KRAS 突变或 NRAS 突变的患者不应使用西妥昔单抗或者帕尼单抗,可能对整体疗效产生负面影响。近两年,针对Kras的靶向治疗进展取得了重大突破,多款靶向药物显示出巨大的潜力。
AMG510
经过三十年的研究,AMG 510是第一个达到临床阶段的KRAS G12C抑制剂!
首次人体结果显示KRAS突变实体瘤的初步安全性,耐受性数据和抗肿瘤活性!
FDA批准AMG 510孤儿药物指定用于KRASG12C阳性非小细胞肺癌和结肠直肠癌,打开了历史性的缺口,让我们看到了希望。
好消息是,这款有望攻克KRAS的抗癌新星已经来到中国,即将正式开展临床试验。3月9日,CDE(国家药监局药品审评中心)官网公布,安进公司研发的KRAS G12C抑制剂AMG 510临床申请获药审中心承办,意味着将在不久后开始招募国内晚期肿瘤患者,全球肿瘤医生网将会密切关注,及时为大家提供招募信息。

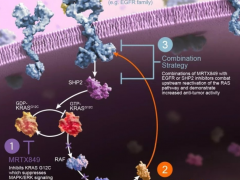
MRTX849横空出世,对肺癌,结直肠癌初显成效
另一家公司Mirati在AACR期刊《癌症发现》上的一篇论文中也报告了令人鼓舞的人类成果。其KRAS(G12C)抑制剂MRTX849使六名肺癌患者中的三名以及四名结肠癌患者中的一名肿瘤缩小。
MRTX849是一款针对KRAS G12C突变体的特异性优化口服抑制剂。在名为MRTX849-001的1/2期临床试验中,MRTX849在治疗携带KRAS G12C基因突变的非小细胞肺癌(NSCLC)和结直肠癌(CRC)患者时表现出可喜的安全性和抗癌活性。
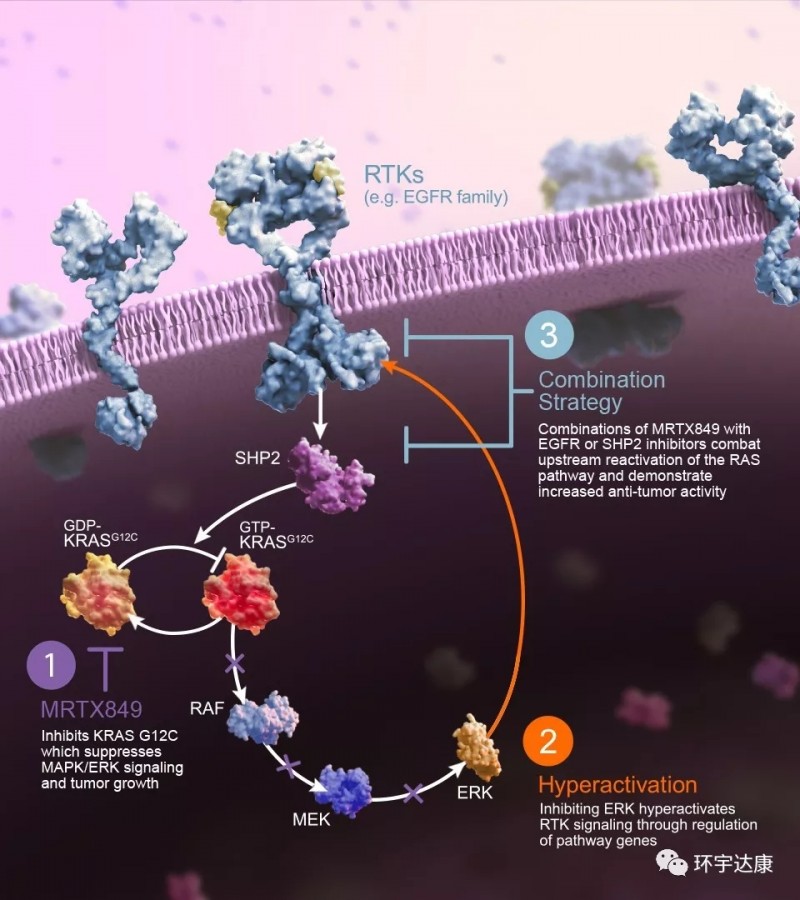
KRAS突变新药Onvansertib闪亮登场,已获FDA快速通道认定
PLK1是丝氨酸/苏氨酸激酶,是细胞有丝分裂的主要调节剂。PLK1在结直肠癌中过表达,与预后不良有关,但是研究人员发现在抑制PLK1后可以诱导癌细胞分裂周期停滞和凋亡,因此将PLK1鉴定为KRAS突变结直肠癌细胞中的理想靶标。在此提醒病友们在进行基因检测的时候可以关注下有没有这个突变,也可以联系全球肿瘤医生网医学部进行解读,推荐治疗方案。
Onvansertib是一种新型的,具有高度选择性的PLK1抑制剂,当与伊立替康联合使用时,效果更好。
onvansertib + FOLFIRI +贝伐单抗的组合可能成为结直肠癌的二线治疗选择。
2020ASCO公布的研究数据显示,入组9名患者,疾病控制率高达(DCR)89%(8/9),客观缓解率(ORR):44.4%(4/9);4例患者达到PR(部分缓解),4例患者达到SD(疾病稳定)。
HER2扩增靶向药
在2%~6%的晚期或转移性结直肠癌患者中发现HER2扩增或过表达。
帕妥珠单抗+曲妥珠单抗
帕妥珠单抗和曲妥珠单抗分别与不同HER2结构域结合而对肿瘤细胞产生协同抑制作用。
MyPathway是第一个探讨帕妥珠单抗+曲妥珠单抗治疗用于HER2扩增转移性结直肠癌患者疗效的临床研究(无论KRAS突变状态)。这项研究表明HER2双靶向治疗——帕妥珠单抗+曲妥珠单抗的耐受性良好,或可作为HER2扩增转移性结直肠癌患者的治疗方案。较早进行基因检测明确HER2突变并考虑早期使用HER2靶向治疗可能会给患者带来获益。
曲妥珠单抗+拉帕替尼
HERACLES研究了曲妥珠单抗(T)联合拉帕替尼(L)治疗HER-2阳性且KRAS野生型 mCRC患者。
结果显示,可评估的23例患者主要研究终点达到:客观缓解率35%(8/23 )。18例患者出现肿瘤缩小:18/23(CR+PR+缩小SD)生存结果显示,HER-2 copy数更高的患者接受抗HER-2治疗后的生存更好。
HER2靶点"广谱药"DS-8201或成结直肠癌后线治疗新选择
DESTINY-CRC01研究是一项开放、多中心、单臂的II期临床试验,旨在评估Trastuzumab deruxtecan(T-DXd;DS-8201)后线(≥3线)治疗HER2阳性/RAS野生型的转移性结直肠癌(mCRC)的疗效和安全性。共纳入78名HER2阳性、RAS野生型且至少经过2线及以上治疗后病情进展的mCRC患者。
研究结果显示DS-8201 6.4mg/kg q3w在标准治疗无效的HER2阳性mCRC的患者中显示出较好的疗效,其安全性与先前的结果一致,但ILD是一种严重的不良事件,需要及时准确的识别和干预。
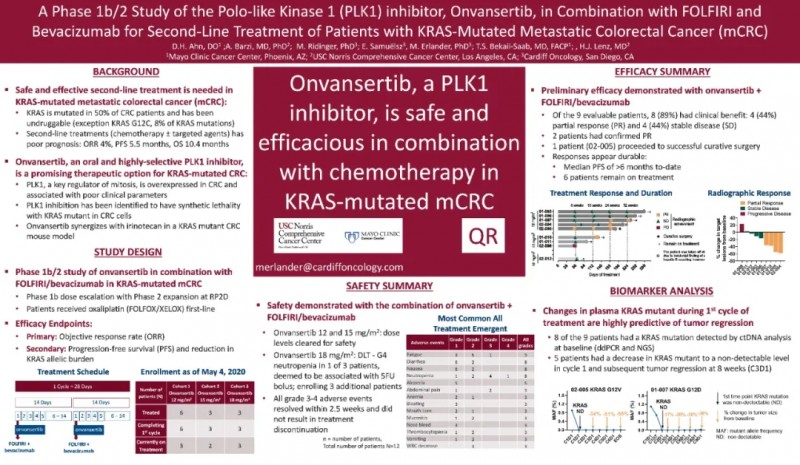
NTRK靶向药
约1~5%的结肠癌患者出现NTRK融合,建议进行NGS检测。
拉罗替尼(Larotrectinib Vitrakvi)
2020年1月23日~1月25日,美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO-GI)上专门分析了携带NTRK融合蛋白的消化道肿瘤患者的临床用药效果。试验结果显示:消化道肿瘤亚组的总缓解率为43%,其中结肠癌患者的总体缓解率为50%。反应的持续时间差异较大,从3.5个月到超过14.7个月不等。
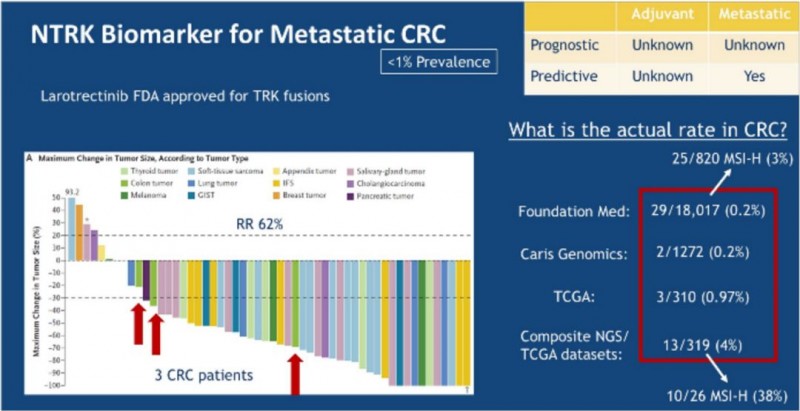
在中位随访期19个月之后,中位总体生存时间长达33.4个月,将近三年。一年的总生存率(OS)为69%。在数据截断时,四名结肠癌患者和一名胰腺癌患者仍然活着,而且病情没有恶化。并且拉罗替尼的安全性和耐受性是良好的。大多数不良反应为1级或2级。
恩曲替尼(Entrectinib Rozlytrek)
2019年8月,恩曲替尼获批上市,是一种具有中枢神经系统活性的酪氨酸激酶抑制剂(TKI),能够穿过血脑屏障,是临床上唯一一种被证明针对原发性和转移性脑疾病具有疗效的TRK抑制剂,并且没有不良的脱靶活性(off-target activity,未达到预先设定的目标);可以阻断ROS1和NTRK激酶活性,并可能导致ROS1或NTRK基因融合的癌细胞死亡。
VEGF靶向药
贝伐单抗(Avastin®)
贝伐单抗是重组的人源化单克隆抗体。2004年2月26日获得FDA的批准,是美国第一个获得批准上市的抑制肿瘤血管生成的药。贝伐珠单抗单药的无进展生存率较低,通常推荐与化疗联合使用。
联合化疗方案:IFL、FOLFIRI、FOLFOX及CapeOX;
使用剂量:5mg/kg(2周方案)及7.5mg/kg(3周方案)。
IFL方案联合贝伐珠单抗治疗晚期结直肠癌,将OS由15.6个月提高至20.3个月(AVF2107研究)。
贝伐珠单抗联合FOLFIRI方案作为一线治疗,其无进展生存率为58.7%,PFS为10.3个月(FIRE3研究)。
贝伐珠单抗分别联合FOLFOX或FOLFIRI作为一线治疗,PFS达到11.3个月,OS达到31.2个月(CALGB80405研究)。
瑞戈非尼(regorafenib)
瑞格菲尼是一种口服的激酶抑制剂,靶向RTK激酶。它通过抑制 VEGFR2-TIE2的活性来抑制肿瘤周边血管生成,也就抑制了肿瘤的营养供给,进而实现缩小肿瘤,并且控制肿瘤进展。2012年9月,瑞格菲尼被FDA批准治疗晚期结肠癌。2017年5月,我国CFDA也已经批准瑞戈非尼用于分别用于治疗既往接受过以氟尿嘧啶、奥沙利铂和伊立替康为基础的化疗,以及既往接受过或不适合接受抗VEGF治疗、抗EGFR治疗(RAS野生型)的转移性结直肠癌(mCRC)患者。
阿柏西普(Zaltrap ziv-aflibercept)
阿柏西普于2012年被美国FDA批准治疗晚期结直肠癌,它是一种嵌合蛋白药物,通过抑制人血管内皮生长因子VEGF来限制肿瘤营养供给,进而抑制肿瘤增殖。
雷莫芦单抗(ramucirumab Cyramza)
Cyramza是一种单克隆抗体药物,它主要通过和血管内皮生长因子受体(VEGFR2)结合,抑制肿瘤周边的新血管生成,抑制肿瘤的营养供给,进而达到抑制肿瘤增殖的效果。
2015年4月24日,FDA批准雷莫芦单抗与FOLFIRI方案联合使用,用于治疗在使用贝伐单抗、奥沙利铂和氟嘧啶治疗期间或治疗之后有疾病进展的转移性结直肠癌患者。
呋喹替尼(爱优特)
呋喹替尼是一种国产的高选择性VEGFR长效抑制剂,其作用机理和瑞戈菲尼类似。
2018年9月在中国获批用于治疗既往接受过氟尿嘧啶类、奥沙利铂和伊立替康为基础的化疗,以及既往接受过或不适合接受抗血管内皮生长因子(VEGF)治疗、抗表皮生长因子受体(EGFR)治疗(RAS野生型)的转移性CRC患者。
呋喹替尼在结直肠癌的三线治疗中的效果良好。因此既往治疗失败的结肠癌患者可以选择使用。
结直肠癌免疫治疗方案及进展盘点
预后优劣顺序:MSI-H 且 BRAF 野生型>MSI-H 且 BRAF 突变型>MSS 且 BRAF 野生型>MSS 且 BRAF 突变型。
MSI-H/dMMR转移性结直肠癌
微卫星不稳定性高(MSI-H)是预后良好的因素,而 MSI-H 的结直肠癌中 BRAF 突变率约 50%。
免疫检查点抑制剂是 MSI-H 的有效治疗方式。目前可以应用于 MSI-H 型 mCRC 患者的免疫检查点抑制剂有派姆单抗、纳武单抗及易普利单抗。
Opdivo(nivolumab 纳武单抗)
2017年8月,FDA加速批准静脉输注Nivolumab用于氟尿嘧啶、奥沙利铂、伊立替康治疗后疾病进展的高微卫星不稳定性(MSI-H)或错配修复缺陷(dMMR)成人或儿童(≥12岁)转移性结直肠癌(mCRC)患者。
Keytruda(帕姆单抗)
2020年6月29日,美国食品药品监督管理局(FDA)批准使用派姆单抗(KEYTRUDA,Merck&Co.)一线治疗无法切除或转移性微卫星不稳定性高(MSI-H)或错配修复缺陷(dMMR)结直肠癌的患者癌症。
Nivolumab +Ipilimumab
2018年7月10日,FDA加速批准ipilimumab(伊匹单抗)与nivolumab(纳武单抗)联合用于治疗12岁及以上、微卫星不稳定性高(MSI-H)或错配修复缺陷(dMMR)、使用氟嘧啶、奥沙利铂和伊立替康治疗后进展的转移性结直肠癌(mCRC)患者。
MSS结直肠癌
95%的结直肠癌患者都是MSS型,这类患者往往对免疫治疗的效果不佳,临床迫切需要更加有效的治疗方案。
Regorafenib(Stivarga)+Nivolumab
一项针对于微卫星稳定(MSS)疾病的患者,大约53名患者接受了[组合治疗]并且达到了40%的高反应率,这在这部分难治性患者中是闻所未闻的。
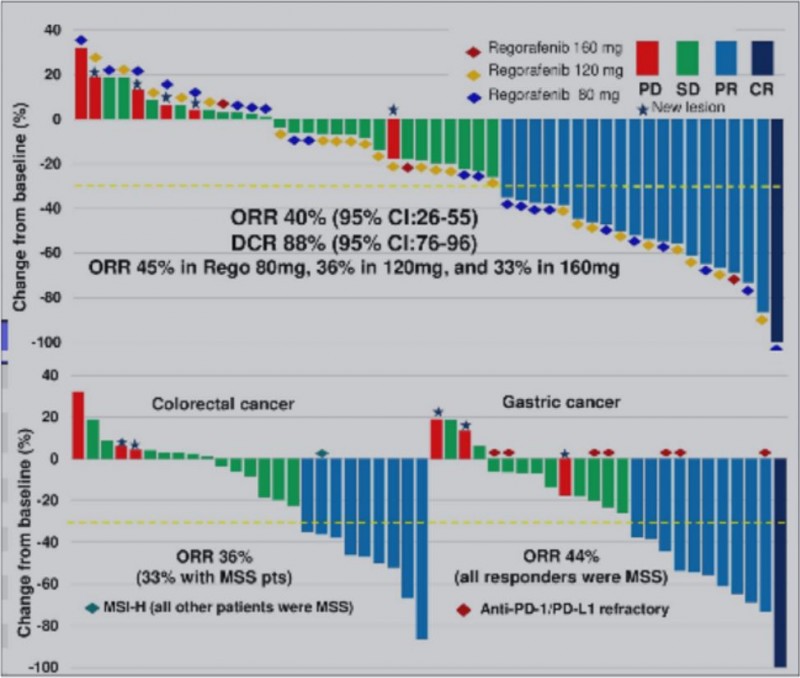
有持续数据显示抗VEGF治疗可能与PD-1阻断有协同作用。现在,这是MSS人群中的第一次,通过结合这两种治疗策略,看到了非常令人印象深刻的疗效。因此,通过将抗VEGF策略与免疫检查点抑制结合起来,MSS疾病患者将会有更大的生存获益。
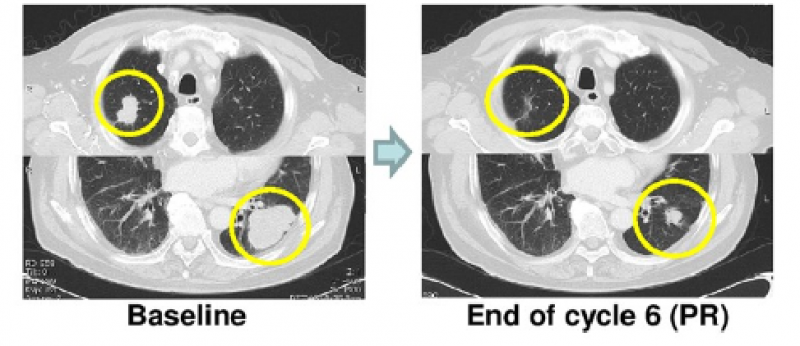
77岁男性,RAS野生型转移性直肠癌,MSS, PD-L1 CPS=0。FOLFIRI+Bevacizumab, FOLFOX, irinotecan+cetuximab,trifluridine/tipiracil后进展接受O药联合瑞戈非尼治疗后病情迅速缓解。
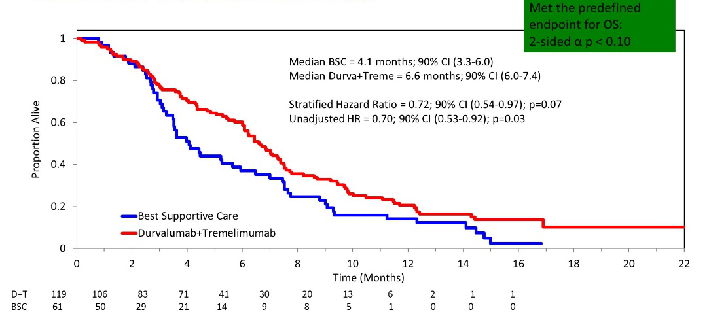
Durvalumab+Tremelimumab
一项研究分析了20例患者,有2例患者出现PR,疗效都持续了44周及44周以上,另外2例患者出现疾病稳定,DCR为20%。16例患者出现≥3级AE,1例患者出现死亡。对于后线难治性MSS型结直肠癌患者,治疗方案非常有限,该免疫联合方案展现了一定的疗效。
惊艳ASCO!PolyPEPI1018疫苗安全有效
PolyPEPI1018是一种现成的多肽疫苗,含有12种免疫原性表位,这些表位衍生自结直肠癌患者中经常表达的7种癌睾丸抗原(CTA)。
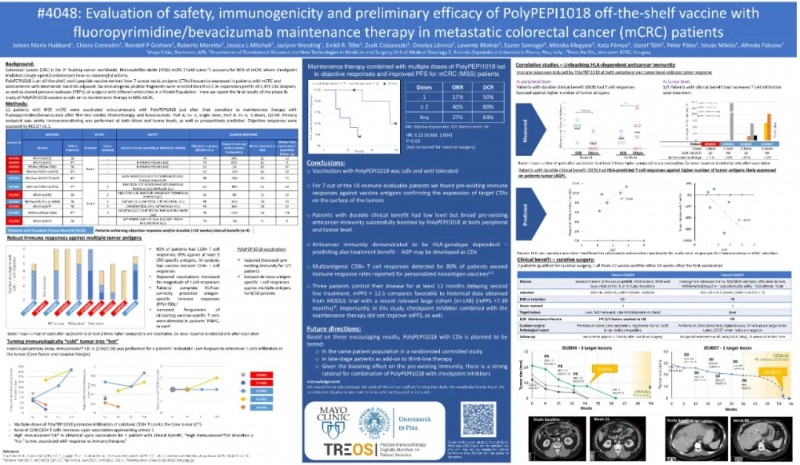
2020年6月的ASCO会议中,报告了PolyPEPI1018疫苗作为转移性结直肠癌患者(mCRC)维持治疗的补充的I期研究的最终结果。
结果显示:
入组的11名MSS(微卫星稳定)的患者对疫苗耐受性良好。最常见的副作用是轻微的皮肤反应。
其中三名患者出现了客观的肿瘤反应:其中两名患者均符合无进展生存性手术的条件,值得一提的是,其中一位患者在手术后的原发肿瘤中发现已经没有存货的肿瘤细胞,这说明,癌症疫苗已经将肿瘤细胞全部杀灭。
因此,PolyPEPI1018可有效恢复患者的免疫反应。用PolyPEPI1018疫苗进行的治疗和维持治疗是安全的,并初步证明了疫苗对MSS mCRC肿瘤具有早期临床活性的证据。
写给结直肠癌患者的话
进入靶向治疗时代,每个患有结直肠癌的患者都应该通过MSI检测、RAS和BRAF的突变分析,并且尽可能进行HER2扩增,NTRK等基因的检测,基因检测(NGS)将纳入大多数患者的初步检查标准。现在国内的患者可通过全球肿瘤医生网进行检测。
我们生活在结直肠癌治疗的分子革命中,我们已经了解了很多关于结肠癌的分子遗传学以及如何将它转化临床治疗决策。未来还将有更多。而关于结直肠癌的研究进展和 用药方案,只有国内外的癌症专家才具备丰富的临床经验.
参考资料:
https://news.cancerconnect.com/colon-cancer/treatment-of-stage-iv-metastatic-or-recurrent-colon-cancer-ZqkcCoOSTUiAphh-ZC0ikA
2. 备注【癌种】申请方舟援助金

患者咨询电话:400-666-7998


全球肿瘤医生网不具备药品销售资格,不售卖任何药物,也不帮助患者代购药物。网上药品代购存在假药等风险,且代购均为违法行为,请广大患者做好自我保护。

2020年,结直肠癌患者又有哪些新的治疗方案可用?有哪些新的药物即将上市,全球肿瘤医生网医学部整理了的信息,供大家参考。
晚期结直肠癌的整体药物治疗策略
一线治疗方案
晚期结直肠癌的治疗方案包括化疗,靶向和免疫治疗。在进行治疗前,一定要进行基因检测,因为医生会基于原发病灶的位置,基因突变及生物标记物检测情况制定治疗方案。
结直肠癌的化学通常选择多药联合,医生根据患者实际情况进行组合搭配,常用的初始标准组合方案如下:
1、FOLFOX(LV / 5-氟尿嘧啶+ 奥沙利铂)
2、CAPEOX(希罗达(卡培他滨)+ 奥沙利铂)
3、FOLFIRI(LV / 5-氟尿嘧啶+伊立替康)
4、FOLFOXIRI(LV / 5-氟尿嘧啶+伊利替康+ 奥沙利铂)
这些治疗方案通常与Avastin®(贝伐单抗)联合使用,可改善生存率,尤其是对于左侧结肠癌的治疗。
说到这里,也需要提醒大家,结直肠癌肿瘤病灶发生在左侧(降结肠、乙状结肠、直肠)与右侧(升结肠、横结肠、盲肠)的治疗方案和预后是完全不同的,切忌混为一谈。在确诊后,大家一定要找的专家制定治疗方案。
左半RAS/RAF野生型患者具体方案如下,I级推荐方案(首选):FOLFOX/FOLFIRI±西妥昔单抗II级推荐方案:FOLFOX/CapeOx/FOLFIRI±贝伐单抗;FOLFOXIRI±贝伐单抗
右半RAS/RAF野生型患者具体方案如下,I级推荐方案(首选):FOLFOX/CapeOx/FOLFIRI±贝伐单抗;FOLFOXIRI±贝伐单抗。与FOLFIRI + Avastin相比,FOLFOXIRI + Avastin的5年总生存率估计提高了一倍。II级推荐方案:FOLFOX/FOLFIRI±西妥昔单抗。
二线治疗治疗方案
在一线时,我们就会选用贝伐单抗联合化疗,如果治疗无效的话,可以换一个化疗方案,继续选用贝伐单抗。当然,也可以在换一个化疗方案的同时换另一个靶向药,换成阿柏西普,或者是雷莫芦单抗。
三线及后线治疗方案
结直肠癌一线和二线的药物方案选择,通常是一些比较标准的化疗药和靶向药。从三线治疗开始是属于后线治疗。后线治疗方案可以使用一些刚刚问世的口服化疗药,包括TAS-102,还有S-1(替吉奥)、瑞格菲尼或者一些免疫疗法,如派姆单抗(MSI-H)。
结直肠癌精准靶向治疗方案及进展
2017版的结直肠癌治疗指南中,关于基因检测的推荐只涉及到KRAS,NRAS,dMMR和MSI-H,而在2020年的治疗指南中,新纳入了BRAF,HER2,NTRK等新的靶点,通过基因检测,了解结直肠癌的更多分子信息,能够帮助我们找到更多的用药方案。患者平均存活率在3年以上,这是精准医学带来的巨大的进步。
确诊后,医生必须尽早对每位患有转移性结直肠癌(mCRC)的患者进行基因检测,以确定疾病中的亚组,因为这些信息可能会预测治疗预后,比如HER2扩增提示抗EGFR治疗耐药。以下基因是必须进行检测的!
MSI,BRAF,KRAS,NRAS,RAS,HER2,NTRK。
FDA批准的靶向治疗药物
VEGF:贝伐珠单抗、阿帕西普
VEGFR:雷莫芦单抗、瑞戈菲尼、呋喹替尼
EGFR:西妥昔单抗,帕尼单抗
PD-1/PDL-1:帕姆单抗、纳武单抗
CTLA-4:易普利单抗
BRAF:维莫非尼,康奈非尼
NTRK:拉罗替尼,恩曲替尼
| 研发公司 | 药物靶点 | 药物名称 | 上市时间 | 中国是否上市 | 医保报销 |
| 百时美施贵宝 | HER1(EGFR/ERBB1) | Cetuximab(西妥昔单抗)Erbitux | 2006 | 是 | 是 |
| 武田/安进 | HER1(EGFR/ERBB1) | Panitumumab(帕尼单抗) | 2005 | 否 | 否 |
| 拜耳 | KIT/PDGFRβ/RAF/RET | Regorafenib(瑞戈非尼) | 2012 | 是 | 是 |
| 和记黄埔 | VEGFR1/2/3 | Fruquinitinib(呋喹替尼) | 2018 | 否 | 否 |
| 赛诺菲 | VEGFA/B | Ziv-aflibercept(阿柏西普) | 2012 | 否 | 否 |
| 礼来 | VEGFR2 | Ramucizumab(雷莫芦单抗) | 2014 | 否 | 否 |
| 基因泰克 | VEGFR | Bevacizumab(贝伐珠单抗) | 2004 | 是 | 是 |
| 百时美施贵宝 | BRAF V600E | Encorafenib(康奈非尼) | 2020 | 否 | 否 |
| 百时美施贵宝 | PD-1 | Nivolumab(纳武单抗) | 2015 | 是 | 否 |
| 百时美施贵宝 | CTLA-4 | Ipilimumab(伊匹单抗) | 2011 | 否 | 否 |
EGFR靶向药
表皮生长因子受体 (EGFR)发生在约10%的结肠癌中,最常见于左侧。
西妥昔单抗和帕尼单抗分别于2004年和2006年被FDA正式批准用于治疗晚期结直肠癌。
西妥昔单抗(爱必妥 Cetuximab Erbitux )
2004年,FDA日前批准西妥昔单抗(cetuximab,Erbitux)治疗有远处转移的晚期结直肠癌。成为第一种获得FDA批准治疗结直肠癌的单克隆抗体,其治疗适应证为:①依立替康(irinotecan) 单独用药或依立替康与其他化疗药物联用效果不佳的晚期结直肠癌患者,可联合应用西妥昔单抗和依立替康;②不能耐受依立替康的患者可单独应用西妥昔单抗。
2019年10月,国家药品监督管理局正式批准西妥昔单抗用于RAS基因野生型转移性结直肠癌一线治疗,并且纳入医保(2290元/支)
帕尼单抗(panitumumab Vectibix)
2006年9月美国FDA批准帕尼单抗用于治疗表皮生长因子受体(EGFR)表达阳性且在含氟尿嘧啶,奥沙利铂和伊立替康的化疗方案后病情仍然进展或转移的结直肠癌.
2014年5 月 26 日,美国 FDA 批准帕尼单抗(Panitumumab)可与 FOLFOX 方案(氟尿嘧啶,亚叶酸钙,奥沙利铂)联用于 Kras野生型mCRC 患者的一线治疗。
BRAF V600E靶向药
7-10% 的结肠癌患者携带 BRAF V600E 突变。BRAF V600E 突变属于 BRAF 激活突变,是 BRAF 比例最高的变异形式。具有独特的临床特征:
主要出现在右半结肠;
dMMR比例高,达到20%;
BRAF V600E突变预后差;
不典型的转移模式;
具有BRAF突变基因的患者通常预后较差,一些新的精确抗癌药物已被证明可以使生存时间加倍。
研究发现 FOLFOXIRI+贝伐珠单抗可能成为 BRAF 突变患者的 治疗。
2019 V2版NCCN指南推荐BRAF V600E 转移性结直肠癌二线治疗方案:
维罗非尼+伊利替康+西妥昔单抗/帕尼单抗
Dabarafenib+曲美替尼+西妥昔单抗/帕尼单抗
Encorafenib+Cetux/Pan
好消息是,面对如此凶险的BRAF V600E突变转移性结直肠癌,2020年4月8日,辉瑞(Pfizer)公司宣布美国FDA已经批准Braftovi®(encorafenib,康奈非尼)和Erbitux®(cetuximab,西妥昔单抗)联合用药方案(Braftovi二药方案),用于治疗携带BRAF V600E突变的转移性结直肠癌(mCRC)患者。这些患者已经接受过一种或两种前期疗法。此次批准,也使Braftovi二药方案成为FDA批准的针对携带BRAF基因突变mCRC患者的首个靶向疗法。
Kras靶向药
KRAS突变是最致命的癌症生长和发展的初始驱动遗传因子之一。表现出这种突变的患者通常预后较差,并且对护理标准治疗的抵抗力很差。据统计,KRAS基因突变出现在近,30-40%的结肠癌中,至今没有获批的靶向治疗方案。
KRAS 突变或 NRAS 突变的患者不应使用西妥昔单抗或者帕尼单抗,可能对整体疗效产生负面影响。近两年,针对Kras的靶向治疗进展取得了重大突破,多款靶向药物显示出巨大的潜力。
AMG510
经过三十年的研究,AMG 510是第一个达到临床阶段的KRAS G12C抑制剂!
首次人体结果显示KRAS突变实体瘤的初步安全性,耐受性数据和抗肿瘤活性!
FDA批准AMG 510孤儿药物指定用于KRASG12C阳性非小细胞肺癌和结肠直肠癌,打开了历史性的缺口,让我们看到了希望。
好消息是,这款有望攻克KRAS的抗癌新星已经来到中国,即将正式开展临床试验。3月9日,CDE(国家药监局药品审评中心)官网公布,安进公司研发的KRAS G12C抑制剂AMG 510临床申请获药审中心承办,意味着将在不久后开始招募国内晚期肿瘤患者,全球肿瘤医生网将会密切关注,及时为大家提供招募信息。

MRTX849横空出世,对肺癌,结直肠癌初显成效
另一家公司Mirati在AACR期刊《癌症发现》上的一篇论文中也报告了令人鼓舞的人类成果。其KRAS(G12C)抑制剂MRTX849使六名肺癌患者中的三名以及四名结肠癌患者中的一名肿瘤缩小。
MRTX849是一款针对KRAS G12C突变体的特异性优化口服抑制剂。在名为MRTX849-001的1/2期临床试验中,MRTX849在治疗携带KRAS G12C基因突变的非小细胞肺癌(NSCLC)和结直肠癌(CRC)患者时表现出可喜的安全性和抗癌活性。

KRAS突变新药Onvansertib闪亮登场,已获FDA快速通道认定
PLK1是丝氨酸/苏氨酸激酶,是细胞有丝分裂的主要调节剂。PLK1在结直肠癌中过表达,与预后不良有关,但是研究人员发现在抑制PLK1后可以诱导癌细胞分裂周期停滞和凋亡,因此将PLK1鉴定为KRAS突变结直肠癌细胞中的理想靶标。在此提醒病友们在进行基因检测的时候可以关注下有没有这个突变,也可以联系全球肿瘤医生网医学部进行解读,推荐治疗方案。
Onvansertib是一种新型的,具有高度选择性的PLK1抑制剂,当与伊立替康联合使用时,效果更好。
onvansertib + FOLFIRI +贝伐单抗的组合可能成为结直肠癌的二线治疗选择。
2020ASCO公布的研究数据显示,入组9名患者,疾病控制率高达(DCR)89%(8/9),客观缓解率(ORR):44.4%(4/9);4例患者达到PR(部分缓解),4例患者达到SD(疾病稳定)。

HER2扩增靶向药
在2%~6%的晚期或转移性结直肠癌患者中发现HER2扩增或过表达。
帕妥珠单抗+曲妥珠单抗
帕妥珠单抗和曲妥珠单抗分别与不同HER2结构域结合而对肿瘤细胞产生协同抑制作用。
MyPathway是第一个探讨帕妥珠单抗+曲妥珠单抗治疗用于HER2扩增转移性结直肠癌患者疗效的临床研究(无论KRAS突变状态)。这项研究表明HER2双靶向治疗——帕妥珠单抗+曲妥珠单抗的耐受性良好,或可作为HER2扩增转移性结直肠癌患者的治疗方案。较早进行基因检测明确HER2突变并考虑早期使用HER2靶向治疗可能会给患者带来获益。
曲妥珠单抗+拉帕替尼
HERACLES研究了曲妥珠单抗(T)联合拉帕替尼(L)治疗HER-2阳性且KRAS野生型 mCRC患者。
结果显示,可评估的23例患者主要研究终点达到:客观缓解率35%(8/23 )。18例患者出现肿瘤缩小:18/23(CR+PR+缩小SD)生存结果显示,HER-2 copy数更高的患者接受抗HER-2治疗后的生存更好。
HER2靶点"广谱药"DS-8201或成结直肠癌后线治疗新选择
DESTINY-CRC01研究是一项开放、多中心、单臂的II期临床试验,旨在评估Trastuzumab deruxtecan(T-DXd;DS-8201)后线(≥3线)治疗HER2阳性/RAS野生型的转移性结直肠癌(mCRC)的疗效和安全性。共纳入78名HER2阳性、RAS野生型且至少经过2线及以上治疗后病情进展的mCRC患者。
研究结果显示DS-8201 6.4mg/kg q3w在标准治疗无效的HER2阳性mCRC的患者中显示出较好的疗效,其安全性与先前的结果一致,但ILD是一种严重的不良事件,需要及时准确的识别和干预。
NTRK靶向药
约1~5%的结肠癌患者出现NTRK融合,建议进行NGS检测。
拉罗替尼(Larotrectinib Vitrakvi)
2020年1月23日~1月25日,美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO-GI)上专门分析了携带NTRK融合蛋白的消化道肿瘤患者的临床用药效果。试验结果显示:消化道肿瘤亚组的总缓解率为43%,其中结肠癌患者的总体缓解率为50%。反应的持续时间差异较大,从3.5个月到超过14.7个月不等。

在中位随访期19个月之后,中位总体生存时间长达33.4个月,将近三年。一年的总生存率(OS)为69%。在数据截断时,四名结肠癌患者和一名胰腺癌患者仍然活着,而且病情没有恶化。并且拉罗替尼的安全性和耐受性是良好的。大多数不良反应为1级或2级。
恩曲替尼(Entrectinib Rozlytrek)
2019年8月,恩曲替尼获批上市,是一种具有中枢神经系统活性的酪氨酸激酶抑制剂(TKI),能够穿过血脑屏障,是临床上唯一一种被证明针对原发性和转移性脑疾病具有疗效的TRK抑制剂,并且没有不良的脱靶活性(off-target activity,未达到预先设定的目标);可以阻断ROS1和NTRK激酶活性,并可能导致ROS1或NTRK基因融合的癌细胞死亡。
VEGF靶向药
贝伐单抗(Avastin®)
贝伐单抗是重组的人源化单克隆抗体。2004年2月26日获得FDA的批准,是美国第一个获得批准上市的抑制肿瘤血管生成的药。贝伐珠单抗单药的无进展生存率较低,通常推荐与化疗联合使用。
联合化疗方案:IFL、FOLFIRI、FOLFOX及CapeOX;
使用剂量:5mg/kg(2周方案)及7.5mg/kg(3周方案)。
IFL方案联合贝伐珠单抗治疗晚期结直肠癌,将OS由15.6个月提高至20.3个月(AVF2107研究)。
贝伐珠单抗联合FOLFIRI方案作为一线治疗,其无进展生存率为58.7%,PFS为10.3个月(FIRE3研究)。
贝伐珠单抗分别联合FOLFOX或FOLFIRI作为一线治疗,PFS达到11.3个月,OS达到31.2个月(CALGB80405研究)。
瑞戈非尼(regorafenib)
瑞格菲尼是一种口服的激酶抑制剂,靶向RTK激酶。它通过抑制 VEGFR2-TIE2的活性来抑制肿瘤周边血管生成,也就抑制了肿瘤的营养供给,进而实现缩小肿瘤,并且控制肿瘤进展。2012年9月,瑞格菲尼被FDA批准治疗晚期结肠癌。2017年5月,我国CFDA也已经批准瑞戈非尼用于分别用于治疗既往接受过以氟尿嘧啶、奥沙利铂和伊立替康为基础的化疗,以及既往接受过或不适合接受抗VEGF治疗、抗EGFR治疗(RAS野生型)的转移性结直肠癌(mCRC)患者。
阿柏西普(Zaltrap ziv-aflibercept)
阿柏西普于2012年被美国FDA批准治疗晚期结直肠癌,它是一种嵌合蛋白药物,通过抑制人血管内皮生长因子VEGF来限制肿瘤营养供给,进而抑制肿瘤增殖。
雷莫芦单抗(ramucirumab Cyramza)
Cyramza是一种单克隆抗体药物,它主要通过和血管内皮生长因子受体(VEGFR2)结合,抑制肿瘤周边的新血管生成,抑制肿瘤的营养供给,进而达到抑制肿瘤增殖的效果。
2015年4月24日,FDA批准雷莫芦单抗与FOLFIRI方案联合使用,用于治疗在使用贝伐单抗、奥沙利铂和氟嘧啶治疗期间或治疗之后有疾病进展的转移性结直肠癌患者。
呋喹替尼(爱优特)
呋喹替尼是一种国产的高选择性VEGFR长效抑制剂,其作用机理和瑞戈菲尼类似。
2018年9月在中国获批用于治疗既往接受过氟尿嘧啶类、奥沙利铂和伊立替康为基础的化疗,以及既往接受过或不适合接受抗血管内皮生长因子(VEGF)治疗、抗表皮生长因子受体(EGFR)治疗(RAS野生型)的转移性CRC患者。
呋喹替尼在结直肠癌的三线治疗中的效果良好。因此既往治疗失败的结肠癌患者可以选择使用。
结直肠癌免疫治疗方案及进展盘点
预后优劣顺序:MSI-H 且 BRAF 野生型>MSI-H 且 BRAF 突变型>MSS 且 BRAF 野生型>MSS 且 BRAF 突变型。
MSI-H/dMMR转移性结直肠癌
微卫星不稳定性高(MSI-H)是预后良好的因素,而 MSI-H 的结直肠癌中 BRAF 突变率约 50%。
免疫检查点抑制剂是 MSI-H 的有效治疗方式。目前可以应用于 MSI-H 型 mCRC 患者的免疫检查点抑制剂有派姆单抗、纳武单抗及易普利单抗。
Opdivo(nivolumab 纳武单抗)
2017年8月,FDA加速批准静脉输注Nivolumab用于氟尿嘧啶、奥沙利铂、伊立替康治疗后疾病进展的高微卫星不稳定性(MSI-H)或错配修复缺陷(dMMR)成人或儿童(≥12岁)转移性结直肠癌(mCRC)患者。
Keytruda(帕姆单抗)
2020年6月29日,美国食品药品监督管理局(FDA)批准使用派姆单抗(KEYTRUDA,Merck&Co.)一线治疗无法切除或转移性微卫星不稳定性高(MSI-H)或错配修复缺陷(dMMR)结直肠癌的患者癌症。
Nivolumab +Ipilimumab
2018年7月10日,FDA加速批准ipilimumab(伊匹单抗)与nivolumab(纳武单抗)联合用于治疗12岁及以上、微卫星不稳定性高(MSI-H)或错配修复缺陷(dMMR)、使用氟嘧啶、奥沙利铂和伊立替康治疗后进展的转移性结直肠癌(mCRC)患者。
MSS结直肠癌
95%的结直肠癌患者都是MSS型,这类患者往往对免疫治疗的效果不佳,临床迫切需要更加有效的治疗方案。
Regorafenib(Stivarga)+Nivolumab
一项针对于微卫星稳定(MSS)疾病的患者,大约53名患者接受了[组合治疗]并且达到了40%的高反应率,这在这部分难治性患者中是闻所未闻的。

有持续数据显示抗VEGF治疗可能与PD-1阻断有协同作用。现在,这是MSS人群中的第一次,通过结合这两种治疗策略,看到了非常令人印象深刻的疗效。因此,通过将抗VEGF策略与免疫检查点抑制结合起来,MSS疾病患者将会有更大的生存获益。
77岁男性,RAS野生型转移性直肠癌,MSS, PD-L1 CPS=0。FOLFIRI+Bevacizumab, FOLFOX, irinotecan+cetuximab,trifluridine/tipiracil后进展接受O药联合瑞戈非尼治疗后病情迅速缓解。

Durvalumab+Tremelimumab
一项研究分析了20例患者,有2例患者出现PR,疗效都持续了44周及44周以上,另外2例患者出现疾病稳定,DCR为20%。16例患者出现≥3级AE,1例患者出现死亡。对于后线难治性MSS型结直肠癌患者,治疗方案非常有限,该免疫联合方案展现了一定的疗效。

惊艳ASCO!PolyPEPI1018疫苗安全有效
PolyPEPI1018是一种现成的多肽疫苗,含有12种免疫原性表位,这些表位衍生自结直肠癌患者中经常表达的7种癌睾丸抗原(CTA)。

2020年6月的ASCO会议中,报告了PolyPEPI1018疫苗作为转移性结直肠癌患者(mCRC)维持治疗的补充的I期研究的最终结果。
结果显示:
入组的11名MSS(微卫星稳定)的患者对疫苗耐受性良好。最常见的副作用是轻微的皮肤反应。
其中三名患者出现了客观的肿瘤反应:其中两名患者均符合无进展生存性手术的条件,值得一提的是,其中一位患者在手术后的原发肿瘤中发现已经没有存货的肿瘤细胞,这说明,癌症疫苗已经将肿瘤细胞全部杀灭。
因此,PolyPEPI1018可有效恢复患者的免疫反应。用PolyPEPI1018疫苗进行的治疗和维持治疗是安全的,并初步证明了疫苗对MSS mCRC肿瘤具有早期临床活性的证据。
写给结直肠癌患者的话
进入靶向治疗时代,每个患有结直肠癌的患者都应该通过MSI检测、RAS和BRAF的突变分析,并且尽可能进行HER2扩增,NTRK等基因的检测,基因检测(NGS)将纳入大多数患者的初步检查标准。现在国内的患者可通过全球肿瘤医生网进行检测。
我们生活在结直肠癌治疗的分子革命中,我们已经了解了很多关于结肠癌的分子遗传学以及如何将它转化临床治疗决策。未来还将有更多。而关于结直肠癌的研究进展和 用药方案,只有国内外的癌症专家才具备丰富的临床经验.
参考资料:
https://news.cancerconnect.com/colon-cancer/treatment-of-stage-iv-metastatic-or-recurrent-colon-cancer-ZqkcCoOSTUiAphh-ZC0ikA
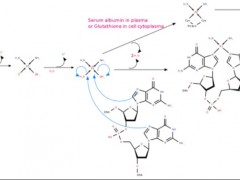
以临床最常用的化疗药物类型之一,铂类化疗药为例,铂类化疗药共分为三代,这些药物的适应症及不良反应之间有非常独特的区别,不同药物之间交叉耐药情况也有差异。
关于化疗,各种流言从未间断:化疗杀敌一千,自损八百癌症患者是死于化疗,而不是癌症本身化疗副作用极其痛苦且让人死得更快....

化疗不仅存在诸多不良反应,给人身带来不同程度的损伤,而且随着化疗疗程的加长,化疗的敏感性越来越差,甚至产生耐药,治疗效果

参的主要药理活性成分人参皂苷已被证明具有多种药用效果,包括突出的抗癌活性。
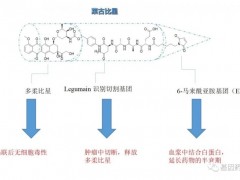
如果基因检测发现了突变自然是好的,意味着患者可以开始尝试各类靶向药物;但并非每位患者都能通过基因检测发现有药物的靶点,而且还有一部分患者,因为耐药等原因而陷入了无靶向药可用的境地。
人们可能因多种原因而免疫功能低下,包括高龄、代谢紊乱(如糖尿病)、癌症治疗,甚至癌症本身。

在癌症治疗领域,虽然靶向药和免疫疗法越来越普遍,但化疗、放疗还是很多癌症的首选治疗方案。由放化疗引起的副作用让很多患者的
1、研究发现能阻止乳腺癌转移的方法约翰斯霍普金斯大学的研究人员报告说,在实验室培养的小鼠组织中证实,乳房乳管周围的细胞层





