01
帕博西林是一种口服细胞周期素依赖性激酶(CDKs)4和6抑制剂。 CDKs 4和6是细胞周期的关键调节因素,其能够触发细胞周期进展。IBRANCE在美国的适应症为联合来曲唑用于治疗雌激素受体阳性,人类表皮生长因子受体2阴性(ER+/HER2-)绝经后晚期乳腺癌患者,作为初始的内分泌治疗为基础的方案治疗转移性疾病。IBRANCE尚未在美国以外的任何市场被批准任何适应症。
美国药品名称:IBRANCE
厂商:辉瑞
规格:125mg
2
FDA批准帕博西林
2017年3月31日:
联合芳香化酶抑制剂治疗激素受体(HR)阳性,HER2阴性晚期或转移性乳腺癌,作为绝经后妇女的初始内分泌治疗。
2016年2月19:
与氟维司群联合治疗激素受体(HR)、HER2阴性内分泌治疗后疾病进展的晚期或转移性乳腺癌。
2015年2月3:
加速批准治疗晚期(转移性)乳腺癌。
3
1.PALOMA-1
2015年2月3日,FDA给予IBRANCE突破性治疗认定和优先审评项目,此次获批是基于2期临床试验PALOMA-1研究最终结果提交的新药申请。
实验设计:
PALOMA-1试验是与Jonsson癌症中心的Revlon/UCLA妇科癌症研究项目合作执行,由Dr. Dennis Slamon领导。165例ER阳性HER2阴性晚期乳腺癌绝经后妇女中,未曾接受先前的治疗。临床研究参与者随机分配接受Ibrance联合来曲唑或来曲唑单独使用。
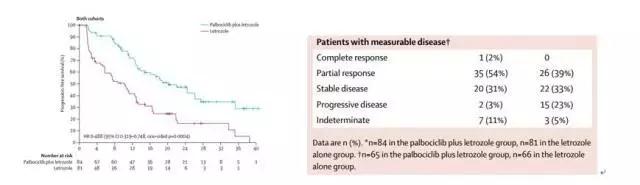
实验结果:
IBRANCE联合来曲唑治疗ER+/HER2-初治的局部晚期或转移性乳腺癌患者较单药来曲唑延长了患者PFS(无进展生存期)。IBRANCE联合来曲唑治疗ER+/HER2-初治的局部晚期或转移性乳腺癌患者较单药来曲唑延长了患者的PFS。接受IBRANCE联合来曲唑治疗实质性的改善了患者的PFS,联合组患者的中位PFS为20.2月,而接受来曲唑单药治疗患者PFS为10.2月。研究者评价的可测量病灶患者中,接受IBRANCE联合来曲唑治疗患者的总体缓解率显著高于来曲唑单药组(55.4% vs 39.4%)。
副作用:
中性粒细胞减少,白细胞低,疲劳,贫血,上呼吸道感染,恶心,脱发,腹泻,血小板减少症,食欲下降,呕吐,无力,周围神经病变和流鼻血。
2.PALOMA-3
2016年2月19日,美国食品和药物管理局批准palbociclib(IBRANCE胶囊,辉瑞公司)与氟维司群联合治疗激素受体(HR)阳性HER2阴性 内分泌治疗后疾病进展的晚期或转移性乳腺癌。
此次批准是基于一个国际的,随机,双盲,平行组,多中心研究比较palbociclib联合氟维司群与安慰剂联合氟维司群在无进展生存期(PFS)方面的改善。
实验设计:
入选的妇女在既往的辅助治疗或转移性内分泌治疗中或之后为HR阳性,HER2阴性晚期或转移性乳腺癌,并有疾病进展。 共521名绝经前和绝经后妇女被随机分配(2:1)到palbociclib联合氟维司群或安慰剂加fulvestrant直到疾病进展或出现不可接受的毒性。
研究结果:
palbociclib联合氟维司群和安慰剂联合氟维司群治疗的患者中位PFS分别为9.5和4.6个月。
副作用:
接受palbociclib联合氟维司群患者最常见的严重不良反应是感染,发热,中性粒细胞减少和肺栓塞。36%的患者因任何等级的不良反应而导致剂量减少,6%的患者发生永久性不良反应。
3
PALOMA-2
2017年3月31日,美国食品和药物管理局批准palbociclib(IBRANCE®,Pfizer Inc.)用于联合芳香化酶抑制剂治疗激素受体(HR)阳性,HER2阴性晚期或转移性乳腺癌癌症,作为绝经后妇女的初始内分泌治疗。此次获批是基于一项国际随机双盲安慰剂对照临床试验(PALOMA-2)的数据。
实验设计:
研究纳入666例绝经后既往未接受针对晚期系统性治疗的乳腺癌患者,按2:1随机分配到帕博西尼联合来曲唑或安慰剂联合来曲唑,28天一疗程,直至疾病进展,撤回知情同意或死亡。
研究结果:
至2016年2月26日,共发生331例PFS事件。两组基线特征相似。中位PFS为24.8月(P+L)比14.5月(安慰剂+L)(HR=0.58 [0.46–0.72], P<0.000001)。P+L组改善ORR(42.1%比34.7%, P=0.031; 可测量病灶者55.3%比44.4% [P=0.013])。OS数据尚未成熟,待进一步分析。
副作用:
最常见不良事件为严重的G3中性粒细胞减少(56.1%)及其他G1的不良事件。发热性中性粒细胞减少见于P+L组(2.5%)。因不良事件导致永久终止治疗的发生率为9.7%(P+L)比5.9%(安慰剂+L)。
5
28天一个疗程,第1-21天每天1次125mg,剩余8天不服用。
可与食物同服。不要挤压,溶解或打开胶囊。
用药期间,不要吃葡萄柚或喝葡萄柚汁。
使用时需要注意的事项有哪些?
服用palbociclib时,未经医生同意,不要接种任何种类的免疫或疫苗。
确保你告诉你的医生你服用的任何其他药物(包括处方药,非处方药,维生素,草药等)。除非医生明确允许,否则不要服用阿司匹林。
这种药不能给孕妇,用药期间避孕。
帕博西林常见的副作用有哪些?
如果您遇到以下任何症状,请立即与您的医护人员联系:
发烧(38ºC)或更高,发冷(可能有感染迹象)
突然胸痛和呼吸急促
以下症状需要医疗护理,但不是紧急情况。在发现以下任何情况后24小时内联系您的医护人员:
恶心(干扰吃药的能力和处方药缓解)
呕吐(24小时内呕吐4次以上)
腹泻(24小时内发作4次)
不寻常的出血或瘀伤
黑便或柏油样便,或便血
血液中的尿液
极度疲劳(无法进行自我照顾活动)
口疮(痛苦的发红,肿胀或溃疡)
腿或手臂肿胀,发红,疼痛和/或温暖触摸。
如果您遇到任何异常症状,请始终通知您的医护人员。
6
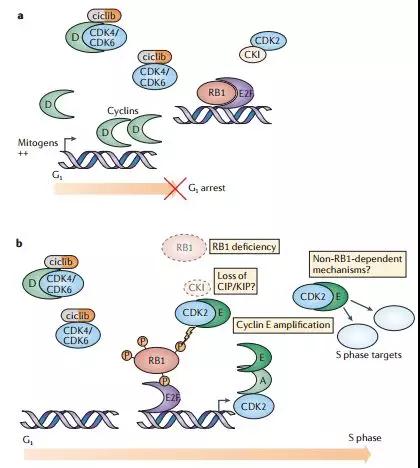
细胞周期蛋白依赖性激酶4/6(Cyclin-dependent kinases 4 and 6,CDK4/6)是细胞周期的关键调节因子,在G1期到S期(G1-to-S-phase)的过渡中发挥了关键的作用。CDK4/6在许多癌症中均过度活跃,导致细胞增殖失控。目前认为,CDK4/6抑制剂的作用是能够选择性抑制CDK4/6,恢复细胞周期控制,从而阻断肿瘤细胞增殖。还会刺激免疫系统攻击和杀死癌细胞。此外,当将这类药物与其它免疫疗法药物联合使用时,抗癌效果能够变得更强。患者需接受基因检测判定是否可以接受靶向药物治疗。
7
1、Palbociclib联合他莫昔芬一线治疗转移性激素受体阳性乳腺癌( NCT02668666 )
这是一项非随机,开放标签,单臂,多中心的II期研究,在HR(+)/ HER2( - )晚期乳腺癌患者中,palbociclib联合他莫昔芬治疗未曾接受过全身性抗癌治疗的晚期/转移性疾病。
实验地点:
1、威斯康星大学医院和诊所
2、明尼苏达大学癌症中心

立即申请
想参加本临床试验的患者可关注全球肿瘤医生网微信公众号,根据提示提交病历资料,医学部会初步评估是否适合,并尽快与您联系,也可致电400-666-7998咨询详情。
2、Palbociclib,来曲唑和曲妥珠单抗治疗雌激素受体阳性和HER2阳性II-III期乳腺癌患者( NCT02907918 )
该II期临床试验研究了palbociclib,来曲唑和曲妥珠单抗在治疗雌激素受体(ER)阳性和HER2阳性II-III期乳腺癌患者手术前的效果。Palbociclib可以通过阻断细胞生长所需的一些酶来阻止肿瘤细胞的生长。来曲唑等药物可以减少身体产生的雌激素的量。单克隆抗体如曲妥珠单抗可能干扰肿瘤细胞生长和扩散的能力。手术前给予palbociclib,来曲唑和曲妥珠单抗可能更好地治疗乳腺癌患者。
实验地点:
华盛顿大学斯特曼癌症中心

立即申请
想参加本临床试验的患者可关注全球肿瘤医生网微信公众号,根据提示提交病历资料,医学部会初步评估是否适合,并尽快与您联系,也可致电400-666-7998咨询详情。
CDK4/6为靶点的新药正在雨后春笋般的跟进。如果明年有更多能让乳腺癌患者用上的新药,这无疑是一个令人兴奋的消息。
2. 备注【癌种】申请方舟援助金

患者咨询电话:400-666-7998


全球肿瘤医生网不具备药品销售资格,不售卖任何药物,也不帮助患者代购药物。网上药品代购存在假药等风险,且代购均为违法行为,请广大患者做好自我保护。

适应症:2015年2月,Ibrance被加速批准联合来曲唑治疗绝经后HR +,HER2-转移性乳腺癌;2016年2月定期批准第二个适应症:联合氟维司群治疗经单独内分泌治疗后进展的HR +、HER2-晚期或转移性乳腺癌;2017年3月,FDA批准palbociclib联合来曲唑作为绝经后HR +,HER2-转移性乳腺癌一线治疗。...
厂家:辉瑞
美国价格: $11518.72 香港价格: ¥33440
规格:100mg/125mg
医保:
是否上市:

01
帕博西林是一种口服细胞周期素依赖性激酶(CDKs)4和6抑制剂。 CDKs 4和6是细胞周期的关键调节因素,其能够触发细胞周期进展。IBRANCE在美国的适应症为联合来曲唑用于治疗雌激素受体阳性,人类表皮生长因子受体2阴性(ER+/HER2-)绝经后晚期乳腺癌患者,作为初始的内分泌治疗为基础的方案治疗转移性疾病。IBRANCE尚未在美国以外的任何市场被批准任何适应症。
美国药品名称:IBRANCE
厂商:辉瑞
规格:125mg

2
FDA批准帕博西林
2017年3月31日:
联合芳香化酶抑制剂治疗激素受体(HR)阳性,HER2阴性晚期或转移性乳腺癌,作为绝经后妇女的初始内分泌治疗。
2016年2月19:
与氟维司群联合治疗激素受体(HR)、HER2阴性内分泌治疗后疾病进展的晚期或转移性乳腺癌。
2015年2月3:
加速批准治疗晚期(转移性)乳腺癌。
3
1.PALOMA-1
2015年2月3日,FDA给予IBRANCE突破性治疗认定和优先审评项目,此次获批是基于2期临床试验PALOMA-1研究最终结果提交的新药申请。
实验设计:
PALOMA-1试验是与Jonsson癌症中心的Revlon/UCLA妇科癌症研究项目合作执行,由Dr. Dennis Slamon领导。165例ER阳性HER2阴性晚期乳腺癌绝经后妇女中,未曾接受先前的治疗。临床研究参与者随机分配接受Ibrance联合来曲唑或来曲唑单独使用。
实验结果:
IBRANCE联合来曲唑治疗ER+/HER2-初治的局部晚期或转移性乳腺癌患者较单药来曲唑延长了患者PFS(无进展生存期)。IBRANCE联合来曲唑治疗ER+/HER2-初治的局部晚期或转移性乳腺癌患者较单药来曲唑延长了患者的PFS。接受IBRANCE联合来曲唑治疗实质性的改善了患者的PFS,联合组患者的中位PFS为20.2月,而接受来曲唑单药治疗患者PFS为10.2月。研究者评价的可测量病灶患者中,接受IBRANCE联合来曲唑治疗患者的总体缓解率显著高于来曲唑单药组(55.4% vs 39.4%)。

副作用:
中性粒细胞减少,白细胞低,疲劳,贫血,上呼吸道感染,恶心,脱发,腹泻,血小板减少症,食欲下降,呕吐,无力,周围神经病变和流鼻血。
2.PALOMA-3
2016年2月19日,美国食品和药物管理局批准palbociclib(IBRANCE胶囊,辉瑞公司)与氟维司群联合治疗激素受体(HR)阳性HER2阴性 内分泌治疗后疾病进展的晚期或转移性乳腺癌。
此次批准是基于一个国际的,随机,双盲,平行组,多中心研究比较palbociclib联合氟维司群与安慰剂联合氟维司群在无进展生存期(PFS)方面的改善。
实验设计:
入选的妇女在既往的辅助治疗或转移性内分泌治疗中或之后为HR阳性,HER2阴性晚期或转移性乳腺癌,并有疾病进展。 共521名绝经前和绝经后妇女被随机分配(2:1)到palbociclib联合氟维司群或安慰剂加fulvestrant直到疾病进展或出现不可接受的毒性。
研究结果:
palbociclib联合氟维司群和安慰剂联合氟维司群治疗的患者中位PFS分别为9.5和4.6个月。
副作用:
接受palbociclib联合氟维司群患者最常见的严重不良反应是感染,发热,中性粒细胞减少和肺栓塞。36%的患者因任何等级的不良反应而导致剂量减少,6%的患者发生永久性不良反应。
3
PALOMA-2
2017年3月31日,美国食品和药物管理局批准palbociclib(IBRANCE®,Pfizer Inc.)用于联合芳香化酶抑制剂治疗激素受体(HR)阳性,HER2阴性晚期或转移性乳腺癌癌症,作为绝经后妇女的初始内分泌治疗。此次获批是基于一项国际随机双盲安慰剂对照临床试验(PALOMA-2)的数据。
实验设计:
研究纳入666例绝经后既往未接受针对晚期系统性治疗的乳腺癌患者,按2:1随机分配到帕博西尼联合来曲唑或安慰剂联合来曲唑,28天一疗程,直至疾病进展,撤回知情同意或死亡。
研究结果:
至2016年2月26日,共发生331例PFS事件。两组基线特征相似。中位PFS为24.8月(P+L)比14.5月(安慰剂+L)(HR=0.58 [0.46–0.72], P<0.000001)。P+L组改善ORR(42.1%比34.7%, P=0.031; 可测量病灶者55.3%比44.4% [P=0.013])。OS数据尚未成熟,待进一步分析。
副作用:
最常见不良事件为严重的G3中性粒细胞减少(56.1%)及其他G1的不良事件。发热性中性粒细胞减少见于P+L组(2.5%)。因不良事件导致永久终止治疗的发生率为9.7%(P+L)比5.9%(安慰剂+L)。
5
28天一个疗程,第1-21天每天1次125mg,剩余8天不服用。
可与食物同服。不要挤压,溶解或打开胶囊。
用药期间,不要吃葡萄柚或喝葡萄柚汁。
使用时需要注意的事项有哪些?
服用palbociclib时,未经医生同意,不要接种任何种类的免疫或疫苗。
确保你告诉你的医生你服用的任何其他药物(包括处方药,非处方药,维生素,草药等)。除非医生明确允许,否则不要服用阿司匹林。
这种药不能给孕妇,用药期间避孕。
帕博西林常见的副作用有哪些?
如果您遇到以下任何症状,请立即与您的医护人员联系:
发烧(38ºC)或更高,发冷(可能有感染迹象)
突然胸痛和呼吸急促
以下症状需要医疗护理,但不是紧急情况。在发现以下任何情况后24小时内联系您的医护人员:
恶心(干扰吃药的能力和处方药缓解)
呕吐(24小时内呕吐4次以上)
腹泻(24小时内发作4次)
不寻常的出血或瘀伤
黑便或柏油样便,或便血
血液中的尿液
极度疲劳(无法进行自我照顾活动)
口疮(痛苦的发红,肿胀或溃疡)
腿或手臂肿胀,发红,疼痛和/或温暖触摸。
如果您遇到任何异常症状,请始终通知您的医护人员。
6
细胞周期蛋白依赖性激酶4/6(Cyclin-dependent kinases 4 and 6,CDK4/6)是细胞周期的关键调节因子,在G1期到S期(G1-to-S-phase)的过渡中发挥了关键的作用。CDK4/6在许多癌症中均过度活跃,导致细胞增殖失控。目前认为,CDK4/6抑制剂的作用是能够选择性抑制CDK4/6,恢复细胞周期控制,从而阻断肿瘤细胞增殖。还会刺激免疫系统攻击和杀死癌细胞。此外,当将这类药物与其它免疫疗法药物联合使用时,抗癌效果能够变得更强。患者需接受基因检测判定是否可以接受靶向药物治疗。

7
1、Palbociclib联合他莫昔芬一线治疗转移性激素受体阳性乳腺癌( NCT02668666 )
这是一项非随机,开放标签,单臂,多中心的II期研究,在HR(+)/ HER2( - )晚期乳腺癌患者中,palbociclib联合他莫昔芬治疗未曾接受过全身性抗癌治疗的晚期/转移性疾病。
实验地点:
1、威斯康星大学医院和诊所
2、明尼苏达大学癌症中心

立即申请
想参加本临床试验的患者可关注全球肿瘤医生网微信公众号,根据提示提交病历资料,医学部会初步评估是否适合,并尽快与您联系,也可致电400-666-7998咨询详情。
2、Palbociclib,来曲唑和曲妥珠单抗治疗雌激素受体阳性和HER2阳性II-III期乳腺癌患者( NCT02907918 )
该II期临床试验研究了palbociclib,来曲唑和曲妥珠单抗在治疗雌激素受体(ER)阳性和HER2阳性II-III期乳腺癌患者手术前的效果。Palbociclib可以通过阻断细胞生长所需的一些酶来阻止肿瘤细胞的生长。来曲唑等药物可以减少身体产生的雌激素的量。单克隆抗体如曲妥珠单抗可能干扰肿瘤细胞生长和扩散的能力。手术前给予palbociclib,来曲唑和曲妥珠单抗可能更好地治疗乳腺癌患者。
实验地点:
华盛顿大学斯特曼癌症中心

立即申请
想参加本临床试验的患者可关注全球肿瘤医生网微信公众号,根据提示提交病历资料,医学部会初步评估是否适合,并尽快与您联系,也可致电400-666-7998咨询详情。
CDK4/6为靶点的新药正在雨后春笋般的跟进。如果明年有更多能让乳腺癌患者用上的新药,这无疑是一个令人兴奋的消息。
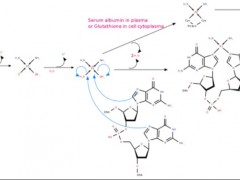
以临床最常用的化疗药物类型之一,铂类化疗药为例,铂类化疗药共分为三代,这些药物的适应症及不良反应之间有非常独特的区别,不同药物之间交叉耐药情况也有差异。
关于化疗,各种流言从未间断:化疗杀敌一千,自损八百癌症患者是死于化疗,而不是癌症本身化疗副作用极其痛苦且让人死得更快....

化疗不仅存在诸多不良反应,给人身带来不同程度的损伤,而且随着化疗疗程的加长,化疗的敏感性越来越差,甚至产生耐药,治疗效果

参的主要药理活性成分人参皂苷已被证明具有多种药用效果,包括突出的抗癌活性。
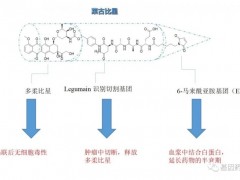
如果基因检测发现了突变自然是好的,意味着患者可以开始尝试各类靶向药物;但并非每位患者都能通过基因检测发现有药物的靶点,而且还有一部分患者,因为耐药等原因而陷入了无靶向药可用的境地。

在癌症治疗领域,虽然靶向药和免疫疗法越来越普遍,但化疗、放疗还是很多癌症的首选治疗方案。由放化疗引起的副作用让很多患者的
人们可能因多种原因而免疫功能低下,包括高龄、代谢紊乱(如糖尿病)、癌症治疗,甚至癌症本身。
1、研究发现能阻止乳腺癌转移的方法约翰斯霍普金斯大学的研究人员报告说,在实验室培养的小鼠组织中证实,乳房乳管周围的细胞层





